Schlankmacher Essig?
So wird die Essigsäure verdaut
In Werbungen für Apfelessig heißt es immer wieder: Wer viel Essig verputzt, wird schlank oder bleibt wenigstens, wie er ist. Das ist kaum glaubhaft. Denn Essigsäure ist nicht nur ein vorzüglicher Energieträger. Essig wird in vielen Stoffwechselreaktionen benötigt - unter anderem auch zur Synthese von gesättigten Fettsäuren und letztlich Fetten, die dann die bekannten Pölsterchen bilden. (Davon unten mehr.)
Vorneweg: Die ganzen Diät-Vorschläge kann man vergessen. Vor linearem Denken wird gewarnt: Alles ist sehr komplex und für Laien wenig überschaubar. Deshalb ist immer noch die beste Diät
FdH -> Friss (und vor allem: trink) die Hälfte
Der Schlüssel für alle Reaktionen: Acetyl-CoA
Essigsäure bzw. das Acetat (im Folgenden behandeln wir beide synonym), bilden zusammen eines der Zentren
des Stoffwechselgeschehens. Genau genommen handelt es sich dabei aber nicht um Essigsäure, sondern um ihre
aktivierte Form, genannt Essigsäure-CoA oder Acetyl-CoA.
Die Abkürzung CoA steht für Coenzym A. Das ist ein Faktor, der bei vielen enzymatischen Reaktionen mitwirkt.

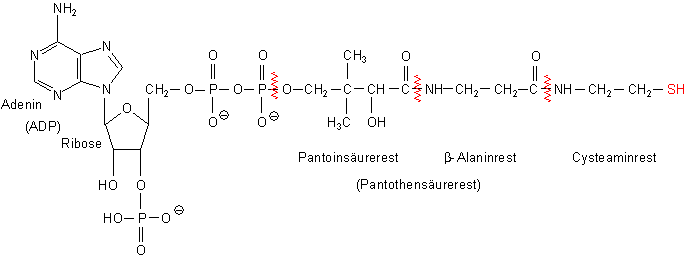
Struktur von Coenzym A (HS-CoA)
Wir erkennen in der Struktur neben einem B-Vitamin (Pantothensäure) eine Thiolgruppe, die auf einem Abkömmling der Aminosäure Cystein beruht: Cysteamin.
Die Formel HS charakterisiert sein aktives Zentrum, eine Thiolgruppe. Die ist analog zu einer HO-Gruppe, also einer Hydroxyl- oder Alkohol-Gruppe. Man kann auch von einem Schwefel-Alkohol sprechen.
Wie sieht die Bindung zwischen Essigsäure und HS-CoA aus?
Beim Acetyl-CoA handelt es sich um eine chemische Verbindung zwischen Essigsäure und Coenzym A. Hier zeigen
wir einen entsprechenden Ausschnitt aus der Strukturformel von Acetyl-CoA.
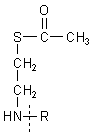
Thioester-Struktur von Acetyl-CoA
Nur in dieser Form kann das Acetat am weiteren biochemischen Reaktionsgeschehen teilnehmen. Das ist fast immer durch Enzyme katalysiert. Daher kommt die Bezeichnung "Coenzym".
Wir erkennen eine esterartige Bindung, eine Thioesterbindung (R-CO-S-R´). Die Thioesterbindung ist anders als eine normale Esterbindung (R-CO-O-R´) hochreaktiv. Um diesen Unterschied herauszustellen, zeichnete man früher die Bindung statt mit einer geraden Linie mit einer Schlangenlinie.

Eine Thioesterbindung befindet sich auf einem hohen energetischen Potential. Wir sprechen manchmal von einer "endothermen Verbindung". Zu deren Synthese muss viel chemische Energie aufgewendet werden. Diese wird durch simultane Hydrolyse von ATP bereitgestellt. Damit ist der erste Schritt der Verarbeitung von Essigsäure im Körper kostenpflichtig. Warum dieser Luxus?
Es geht hier zu wie im echten (Wirtschafts)Leben: Ohne Primärinvestition gibt es keinen Gewinn. (Ein anderes Beispiel für eine solche kostenintensive, sich letztlich aber lohnende Anfangsinvestition ist die zweimalige ATP-verschlingende Phosphorylierung der Glucose, die erforderlich ist, um den biochemischen Energieinhalt der Glucose - insgesamt 38 ATP / mol - auszuschöpfen.)
Von der freien Essigsäure zum Acetyl-CoA
In den Zellen befindet sich ein Enzym, die Acetat-Thiokinase. Diese koppelt Acetat bzw.
Essigsäure und den Thioalkohol HS-CoA. Dies ist die Gesamtreaktionsgleichung:

Dass besonders viel Energie benötigt wird, ist schon daran erkenntlich, dass ATP zwei Phosphatreste (Pi) gekoppelt als anorganisches Pyrophosphat (PPi) abspaltet.
Genau genommen handelt es sich bei der Bildung von Acetyl-CoA um eine Zweitschritt-Reaktion, die von einem Enzym katalysiert wird.
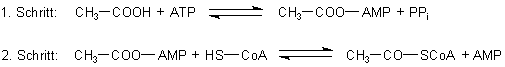
Intermediär wird Acetyl-Adenylat gebildet (Gleichung 1). Hierbei handelt es sich um ein so genanntes gemischtes Säureanhydrid aus dem Phosphorsäurerest des AMP und der Essigsäure.
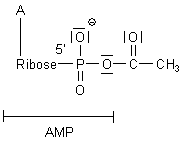
Acetyl-Adenylat
(Solche Anhydride spielen auch bei anderen Aktivierungen wie zum Beispiel der Aminosäuren zu Beginn der Proteinbiosynthese eine wichtige Rolle.)
Dieses Anhydrid wird in der Thiokinase nicht mit einem Wassermolekül, sondern mit einem Molekül HS-CoA gespalten (Gleichung 2). Das anschließend freigesetzte AMP wird in Folgereaktionen unter Energieaufwand (zum Beispiel aus der Glykolyse oder aus der Endoxidation von Essigsäure stammend) in ATP rückverwandelt. Auch hier gibt es eine Zwei-Schritt-Reaktion, da AMP nicht direkt phosphoryliert werden kann. Zunächst läuft eine Energie-Symproportionierung zwischen ATP und AMP ab.
ATP + AMP ———> 2 ADP
Das heißt, ein System auf hohem Energielevel bildet mit einem auf niedrigem Level ein System mittlerer Energie. Das gebildete ADP reagiert wie bekannt mit anorganischem Phosphat zu ATP. Die dazu notwendige Energie stammt zum Beispiel aus der Glykolyse, der Fettverbrennung oder aus der Atmungsketten-Phosphorylierung. Das Enzym, das hier mitwirkt, heißt ATP-Synthase.
2 ADP + 2 Pi + chemische Energie ———> 2 ATP
Die Thiokinase ist übrigens ein Beispiel für die Enzymgruppe der Ligasen: Ihr systematischer Name ist Acetat:CoA Ligase (AMP).
Stoffwechselschaltstelle Acetyl-CoA
Wenn Essigsäure einmal in Acetyl-CoA umgewandelt ist, kann die ganze Vielfalt ihrer biochemischen Nutzung
einsetzen. Dabei entpuppt sich Acetyl-CoA als eine wichtige Schaltstelle im Stoffwechsel.
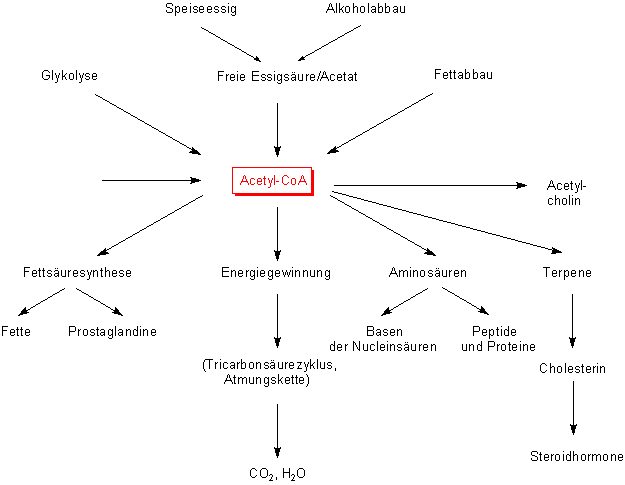
Wie Acetyl-CoA entsteht
Die Verbindung entsteht nicht nur aus Essigsäure oder Acetat, sondern auch beim Abbau von Kohlehydraten
(letztlich der Glucose) im Anschluss an die Glykolyse sowie beim Endabbau von Aminosäuren. Eine besonders
ergiebige Quelle für Acetyl-CoA bildet jedoch die Verwertung der Fette. Beim Abbau der Fettsäuren sowie
bei der Oxidation von Glycerin bilden sich große Mengen davon. Last but not least ist auch
beim biochemischen Abbau von Ethylalkohol (Bier, Wein und Schnaps) ein großer "Gewinn" an Acetyl-CoA
zu verzeichnen.
Acetyl-CoA ist wichtig für den Aufbau von Fettsäuren
Andererseits ist die aktivierte Essigsäure wiederum Grundbaustein für Fettsäuren. Das erkennen wir schon daran,
dass der allergrößte Teil der natürlichen Fettsäuren eine charakteristische Eigenschaft hat: Die Zahl ihrer C-Atome
lässt sich immer durch 2 teilen. Das liegt daran, dass in einem (wenn auch zugegebenermaßen komplizierten)
Reaktionsmechanismus ein Essigsäuremolekül an das andere gebunden wird.
Eine süße Likör-Praline wirkt - wie ersichtlich - somit aus mehreren Gründen fettpolstersteigernd. Das Glycerin für die Fettsynthese wird aus dem Abbau von Glucose, der Glykolyse, abgezweigt. Insgesamt offenbart sich hier der Zusammenhang zwischen zuviel Nahrung, Alkohol und dem Fettansatz.
Es gibt aber auch Lichtblicke: Aktivierte Essigsäure ist Grundbaustein für die Synthese von Cholesterin, Nebennierenrinden- und Sexualhormonen sowie von Gewebehormonen wie den Prostaglandinen.
Acetyl-CoA dient zur Energiegewinnung
Ein weiterer Lichtblick: Aktivierte Essigsäure ist nicht nur Synthesebaustein, sondern wird auch zur
Energieumwandlung oxidativ abgebaut. Auch dabei werden Reduktionsäquivalente [H] und daraus letztlich auch
ATP gebildet. Diese Oxidation von Essigsäure (bzw. Acetyl-CoA) wird durch die folgende Gleichung beschrieben:
CH3-COOH + 2 H2O ———> 2 CO2 + 8 [H] + Energie
Auch diese Oxidation läuft schrittweise ab, um die Energieausbeute zu optimieren. Dies geschieht mit Hilfe des Enzymapparats des Citronensäure-Zyklus. Die Reaktionssequenz ist einer der schönsten biochemischen Katalyse-Kreisläufe, den wir kennen.
Klick mich an!
Citronensäure-Zyklus
Das Reduktionsäquivalent 2 [H] steht für Verbindungen wie NADH/H+ sowie FADH2. Von ersterem
entstehen 3, vom zweiten 1. Diese Verbindungen werden in der Atmungskette letztlich mit Sauerstoff oxidiert.
Dabei wird Oxidationsenergie frei. Ein Mol NADH/H+ entspricht 3 Mol ATP, ein FADH2 entspricht
2 ATP. Darüber hinaus entsteht im Citronensäure-Zyklus ein Mol GTP, das dem schon bekannten ATP äquivalent ist.
Energiebilanz des Essigsäureabbaus
In der Endbilanz entstehen somit pro Mol Essigsäure 2 Mol CO2 sowie 12 Mol ATP.
CH3-COOH + 2 O2 + 12 (ADP + Pi ) ———> 2 CO2 + 2 H2O + 12 (ATP + H2O)
Berücksichtigen wir noch die Anfangsinvestition von 2-3 Mol ATP, so beträgt die Endausbeute etwa 10 Mol ATP pro Mol Essigsäure.
Essig - wohl kein Schlankmacher
Pro Mol ATP veranschlagt man etwa 50 kJoule, also 11-12 kcal. Ein Mol Essigsäure (das sind 60 g) bringt somit
etwa 500 kJoule auf die Waage. Das ist eine ganz propere Kalorien-Menge für einen Schlankmacher...
Hinzu kommt, dass Saures vor dem Essen noch als Appetitmacher gereicht und genossen
wird. Wie heißt es so richtig?: "Saures macht lustig" - das heißt es macht lüstern aufs Essen.
Weitere Texte zum Thema „Essig“