 |
 |
 |
 |
| Was es sonst noch so gab...
Merkwürdiges aus dem E-Mail-Korb von Professor Blume |
346 Betreff: Kontextorientierte Aufgaben
F: Ich habe dieses Jahr zum ersten Mal mündliches Abitur und brüte gerade über den Aufgaben.
Haben sie evtl. Anregungen oder irgendwelche Musterprüfungen zu den Themen Alkoholen und Aldehyde, Ketone... Säuren und Basen oder
Schmerzmittel, bei denen die Aufgaben in einen Kontext eingebettet sind? Das muss ja in RLP seit neustem so gemacht werden.
Falls sie mir weiterhelfen können, wäre das wirklich sehr nett von ihnen. Ich würde gerne Fragen zu Säuren und Basen stellen,
wo ich die Titration einbinde. Suche dazu aber noch einen geeigneten Kontext.
Es könnte auch eine Kursarbeitsfrage sein, die ich dann umformuliere.
Vielen Dank im Voraus.
LG (...)
A: Früher sprachen wir nicht von Chemie im Kontext, sondern von Alltagschemie. Die pflegte
früher jeder Lehrer bzw. jede Lehrerin schon immer einzubinden. Wie sagt man doch so richtig: „Alter Wein in neuen Schläuchen“.
Wenn ich es richtig verstehe, sind Sie Lehrerin. Gerade in den meisten von unseren Webseiten finden Sie Hinweise zu Ihrem Anliegen.
Zum Beispiel in meinen Tipps des Monats.
Speziell zur Titration:
1) Da wären einmal die Titration der Säure von Blutorangen, die ihren Indikator in sich tragen (Tipp Nr. 6).
2) Oder aber die Titration von Haushaltsessig (z. B. Überprüfung der Angaben auf dem Etikett). Zum letzten Thema klicken Sie hier:
Was ist Essig?. Falls Sie Schülerin sind, können Sie den Inhalt referieren und dazu noch ein schönes,
quantitatives Experiment machen.
Andere alltags-orientierte Themen finden Sie hier.
Viel Erfolg bei der Prüfung - egal, auf welcher Seite des Tisches Sie sitzen.
347 Neutralisation
F: Lieber blume
wir nehmen zur zeit Neutralisation in der Schule durch undich verstehe rein gar nichts mehr können sie mir be folgenden aufgaben behilflich sein??
1. Entwickle die Reaktionsgleichung für die Neutralisation von Kalilauge mit Schwefelsäure.
2. Antacida enthalten als Wirksame Bestandteile z.B. Magnesiumhydroxid und Alminiumhydroxid. Entwickle die Reaktionsgleichung für die Neutralisation von Salzsäure.
3. Petra behaubtet,eine Neutralisation kann auch stattfinden, ohne das eine neutrale Lösung entsteht. Diskutiere diese Ausage.
Das sind die Aufgaben über eine positive ntwort würde ich mich freuen denn ich verstehe wirklich nichts davon.
A: Ich will es versuchen.

Zu 3: Nein, Petra hat Unrecht. Neutrale Lösungen haben exakt den pH-Wert 7. Falls jedoch Petras Aussage als richtig erklärt werden sollte, meint dein Lehrer vielleicht Folgendes: Neutral sein bedeutet für ihn, wenn alle Protonen einer Säure mit den Hydroxid-Ionen zu Wasser reagiert haben. Manche Säuren wie die Essigsäure machen das aber erst bei höheren pH-Werten (Essigsäure zum Beispiel bei pH 8,8), also im Alkalischen. Das ist dann aber keine Neutralisation, sondern nur das völlige Abreagieren einer Säure oder deren völlige Umwandlung in ihr Anion.
Ansonsten mein Tipp: Setz dich mit anderen Schülern zusammen. Auf diese Weise lernt es sich besser.
348 Östrogene in der Schule
F: Wir sind eine Forschergruppe des (...)-Gymnasiums in (...) und suchen eine Methode um Östrogene
(im Abwasser) nachzuweisen.
Wir wären Ihnen sehr verbunden wenn Sie schnellstmöglich eine Antwort auf unser Problem finden könnten.
Wir bedanken uns schon im Vorraus.
A: Ich kenne keine Methode, die für die Schule geeignet ist, um Östrogene nachzuweisen. Es sei
denn, Sie verfügen über eine HPLC-Anlage und vor allem über Voranreicherungssysteme. Dazu wäre auch eine Vorrichtung zur GC/MS-Kopplung
wünschenswert.
Aber vielleicht haben Sie mit Ihrer Themenwahl nur etwas zu hoch gegriffen...
349 Rechtliche Grundlagen von experimentellen Hausaufgaben
F: Im Rahmen meiner zweiten schriftlichen Examensarbeit möchte ich die Motivation von
experimentellen Hausaufgabe untersuchen. Leider konnte ich trotz gründlicher Recherche noch keine Angaben zu den rechtlichen Grundlagen
hinsichtlich der Durchführung solcher Heimexperimente im Chemieunterricht finden.
Wissen Sie, wie die Durchführung von Heimexperimenten geregelt ist bzw. könnten Sie mir sagen, an wen ich mich sonst wenden könnte? Sie würden mir wirklich sehr weiterhelfen.
A: Das ist eine wirklich interessante Frage: Ist das Zuhause ein „Außerschulischer Lernort“?
Dazu gibt es keine mir bekannte Literatur. Es handelt sich hier in erster Linie wohl um eine Frage des Versicherungsrechts. Wenn beim häuslichen Experimentieren etwas passiert, sind Konflikte mit Hausrats-, Haftpflicht- und Krankenversicherungen vorprogrammiert. Letztlich kann es auch um Strafrechtliches gehen (z. B. § 310 StGB - betrifft Sprengstoffvergehen).
Letzteres ist nicht zu unterschätzen: Mir ist ein Fall bekannt, wo ein bislang unbescholtener Bürger (ausgebildeter Diplomchemiker!) wegen des simultanen Besitzes von Wasserstoffperoxid, Reinigungsbenzin und Pinselreiniger in den Ruch geraten ist, Terrorist zu sein...
Es ist auch daran zu denken, dass diejenige Lehrerperson, die einen Schüler auffordert, zu Hause ein bestimmtes Experiment zu machen, strafrechtliche Probleme bekommen können. Einen solchen Fall schildern wir hier.
Klären Sie das Rechtliche bitte mit einem Vertreter der für die Schule zuständigen Gemeindeversicherung.
350 Betreff: Möglichkeit verschiedener (Poly-)reaktionen
F: Hallo Herr Professor Blume,
wir haben im Chemieunterricht (Stufe 13) die verschiedensten Polyreaktionen mit den verschiedensten Eduktoren durchgesprochen.
Allerdings kann mir mein Lehrer nicht sagen ob und wie weit die 5 angehängten Reaktionen theoretisch richtig und logisch sind. Und
falls nicht was der Fehler daran ist.
Wenn sie uns damit helfen könnten wäre ich sehr froh, da ich sonst keine Antwort auf die Frage finde.
MfG (...)
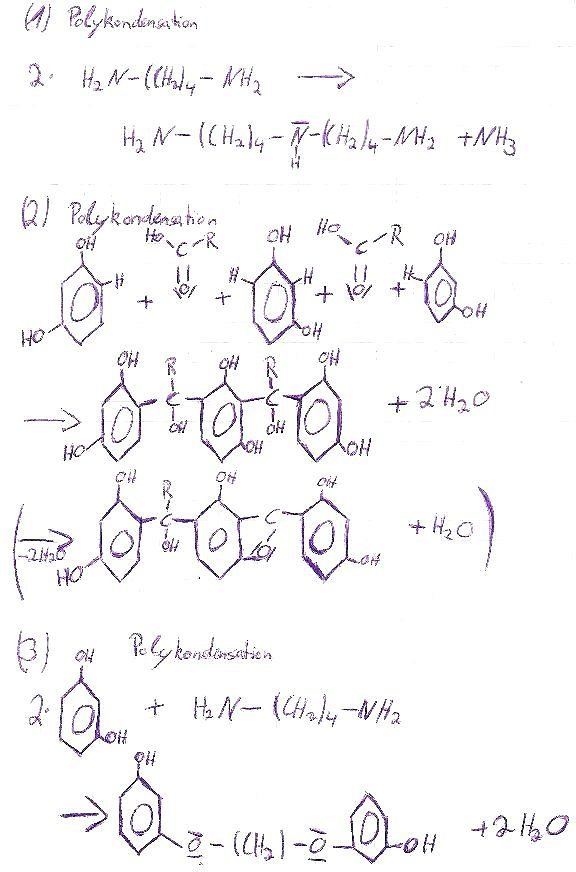
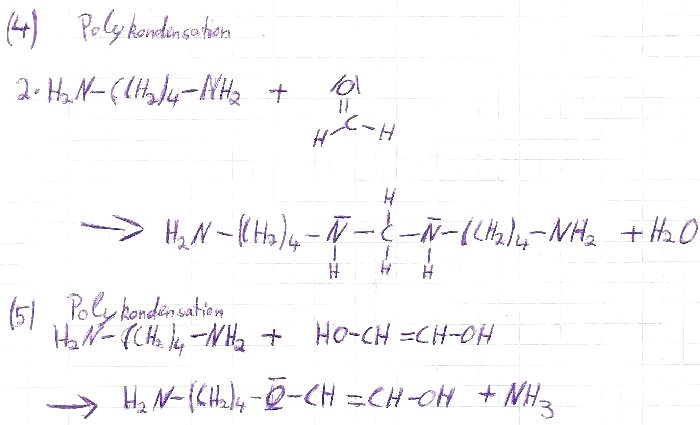
A: Es sind alle fünf Beispiele unmöglich. Im Einzelnen:
Zu 1) Amine verbinden sich nicht auf diese Weise. Nicht mal beim Erhitzen.
Zu 2) Carbonsäuren können auf diese Weise nicht den aromatischen Ring angreifen. Geschweige denn, zwei Ringe verbinden... In der 3. Zeile findet sich außerdem in der Brücke dreibindiger Kohlenstoff. Und wenn es eine C=O-Gruppe sein sollte: Wo sind R und H geblieben?
Zu 3) Das Abgangsprodukt müsste wohl NH3 sein. Aber diese Reaktion findet sowieso nicht statt: Denn Phenole sind Säuren. Deren Protonen bilden mit dem Amin Alkylammonium-Ionen, die nicht mehr als Basen angreifen können. Das Produkt Ihrer Mischung ist Alkylammonium-Phenolat.
Zu 4) Die Reaktion könnte begrenzt gehen. Allerdings entsteht sofort Wasser, das das Ganze ausbremst. Denn das Amin reagiert als Base
mit Wasser, wird dadurch positiv geladen und verliert als Alkylammonium das freie Elektronenpaar zur Bindung an Formaldehyd.
(Beim Harnstoff geht das, weil dessen Aminogruppen nicht basisch reagieren.)
Zu 5) Das geht auch nicht. Warum soll eine nicht aktivierte C-N-Bindung zugunsten einer C-O-Bindung geöffnet werden?
Sie dürfen nicht einfach spekulieren, sondern müssen überlegen, wie die Substanzen miteinander reagieren können. Mögliche Parallel-Reaktionen wie Salzbildung müssen Sie ausschließen können. Dazu müssen Sie sich auch überlegen, ob die Edukte ausreichend polarisiert sind. Hinzu kommt, dass die Bindung, die geöffnet werden soll, schwächer sein muss, als die neu zu schließende. Deshalb muss mindestens eines der Edukte sich energetisch auf hohem Potential befinden, z. B. durch eine stark polarisierte Doppelbindung (z. B. Formaldehyd) oder als Ester, Säureanhydrid oder Säurechlorid.