 |
 |
 |
 |
| Kurze Fragen - Kurze Antworten
Aus dem E-Mail-Korb von Professor Blume |
1316
F: Woher stammt der Begriff "Salzsäure"?
A: Dahinter steckt ein Verfahren aus den Anfängen der Chemie.
Das ist die "Säure, die aus Salz gewonnen wurde". Johann Rudolph Glauber behandelte um 1655 Kochsalz
("das Salz" schlechthin) mit Vitriolöl (also mit konzentrierter Schwefelsäure). Dabei entwich ein Gas
(Chlorwasserstoff), das mit Wasser eine Säure gab, eben die "Salzsäure".
2 NaCl (fest) + H2SO4 ———> Na2SO4 + 2 HCl (gasf.)
HCl (gasf.) + H2O ———> HCl (gelöst)
Zurück blieb eine Salzlösung, aus der man durch Auskristallisieren das auch heute noch viel genutzte Glaubersalz gewann: Na2SO4 · 10 H2O.
1317
F: Sehr geerhrter Herr Blume,
ich habe unterschiedliche Angaben zu dieser Frage gefunden. Im Chemie heute (Schrödel) steht, dass das Verhältnis von Hülle zum Atomkern 10000:1 ist und im Mortimer Chemie steht ein Wert, der um das 10-fache höher ist demnach 100000:1.
Ebenfalls findet man im Internet verschiedene Arbeitsblätter mit verschiedenen Angaben und Größenvergleichen.
Können Sie dies enträtsel?
Beste Grüße ...
A: Bedenken Sie, dass Atome und ihre Hüllen keine statischen
Kugeln sind wie jene, die man vom Billard her kennt! Sie sollten sich deshalb nicht an Werte klammern,
die bei diesen Dimensionen nur um den Faktor 10 variieren; es geht um Durchschnittliches, was die
Gesamtheit aller großen und kleinen Atome betrifft. Hinzu kommen Näherungen und mehr oder weniger
subjektive Abrundungen von Werten, so dass alle Angaben nur "Circa-Werte" sind.
Beispiel Wasserstoff: Sein Atomdurchmesser ist ca.
2,4 bis 2,8 · 10-10 m
oder 2,4 bis 2,8 Å (1 Ångström -> 10-8 cm oder
10-10 m)
oder 240 bis 280 pm (1 Picometer -> 10-12 m)
oder 240.000 bis 280.000 fm (1 Femtometer -> 10-15 m).
Der Atomkern hat einen Durchmesser von ca. 3 · 10-15 m (oder 3 fm).
Hier stimmt der Faktor 1:100.000 ziemlich genau. Bei schwereren Atomen weicht das schon kräftig ab.
Sagen Sie also: Der Radius des Atomkerns ist um den Faktor 104 bis 105 kleiner als der des gesamten Atoms.
1318
F: Woraus besteht eine Flamme?
A: Flammen sind Begleiterscheinungen von Bränden, bei denen
die Abgase aus der Verbrennung ionisiert vorliegen. Bei der Rekombination der Elektronen mit den Ionen
wird die Energie als Licht abgegeben.
Das ionisierte Gas nennt man auch Plasma.
1319
F: Wie ist ein Autoreifen aufgebaut. Ich habe gehört, dass man auch
Silcate einbaut.
A: Zunächst kommt das Gummi, dann die Nylonabdeckung, der
Stahlgürtel (ein Gewebe aus Stahldrähten) sowie die Cordlagen aus Polyester. Diese Lagen werden unter
hohem Druck (bis 22 bar) und bei 200 °C "zusammengebacken". Zuletzt wird das Profil eingeprägt.
Früher hat man viel Ruß zur Reifenmasse gegeben. Sie sollten die Reifen nicht nur färben, sondern
auch für besseren Zusammenhalt der Kautschukmoleküle sowie für bessere Haftung sorgen. Heute gibt man
aus den gleichen Gründen außerdem polymere Kieselsäureverbindungen hinzu ("Silica"), was auch immer man
darunter versteht. Sie bewirken besonders auf polaren Oberflächen bessere Haftung. Da diese wegen ihres
polaren Aufbaus in der Gummimatrix nicht haften, gibt man Organosiliciumverbindungen zu, die Organosilane.
Silane sind Si-H-Verbindungen, die den Kohlenwasserstoffen analog sind. Die technisch genutzten Silane
tragen anstelle von H-Atomen Methylgruppen (usw.), enthalten also direkte Si-C-Bindungen. (Nicht
verwechseln mit den Silikonen! Das sind die siliciumorganischen Polyetheranalogen.) Die Organosilane
wirken als physikalische Bindungsmittler zwischen den Silica-Verbindungen und der Gummimatrix.
1320
F: Bei Spektren werden auf der Abszisse statt Wellenlängen oft
Wellenzahlen abgetragen. Was ist der Unterschied?
A: Spektren sind im allgemeinen Darstellungen, bei denen
auf der Abszisse eine Energie oder eine energieproportionale Größe abgetragen wird. Auf die Ordinate
findet man Maße für die Häufigkeit entsprechender Energiezustände.
Bei Strahlungsspektren trägt man z. B. die Transmission oder Absorption der Strahlung gegen die Wellenlänge auf. Oder gegen die Wellenzahl. Um das zu verstehen, müssen wir etwas ausholen.
Die Energie der Strahlung ist
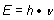
h ist das Plancksche Wirkungsquantum (erg · sec). n ist die Frequenz (sec-1 = Hz).
Man misst im allgemeinen Wellenlängen. Zwischen der Frequenz und der Wellenlänge l (cm) besteht folgender Zusammenhang:
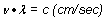
Eingesetzt in die o. a. Gleichung folgt
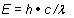
Wir sehen, dass die Energie umgekehrt proportional zur Wellenlänge ist - das ist insgesamt sehr unhandlich. Besser geeignet ist die reziproke Wellenlänge 1 / l; diese nennt man Wellenzahl.
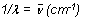
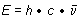
Der Wert der Wellenzahl ("nü-quer" gesprochen) gibt an, wie viele Wellenlängen auf einen Zentimeter kommen. Die Wellenzahl ist somit direkt proportional zur Energie der Strahlung und für Physiker und Chemiker viel aussagekräftiger als die Wellenlänge.