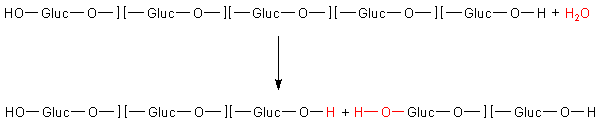
Versuch: Enzymatische Spaltung von Kartoffelstärke
Schülerversuch; 20 min.
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
Geräte
Becherglas (100 ml), 10 Reagenzgläser, Tropfpipetten, Dreifuß, Bunsenbrenner, Wasserbad.
Chemikalien
Kartoffelstärke, Iod-Kaliumiodid-Lösung (Xn),
Benedict-Lösung (C), Speichel, destilliertes Wasser.
Durchführung
a) Zunächst werden 50 ml eines 5%igen Stärkekleisters hergestellt.
Dazu werden 2,5 g Stärke in einem Becherglas in 50 ml destilliertem Wasser gerührt und
kurz aufgekocht, bis die Lösung verkleistert.
b) Dann werden 8 Reagenzgläser vorbereitet, die je mit 10 ml dest. Wasser und je einem Tropfen Iod-Kaliumiodid-Lösung gefüllt werden. Die Lösungen sind gelbbräunlich.
c) Eine Probe des Stärkekleisters wird mit 1 ml Benedict-Lösung versetzt und im Wasserbad erhitzt (Vorsicht! Schutzbrille tragen!) Die Lösung verfärbt sich nicht. Eine zweite Probe des Kleisters wird mit 1 Tropfen Iod-Kaliumiodid-Lösung versetzt. Die Lösung färbt sich intensiv blau.
d) 30 ml des Stärkekleisters werden mit 2 ml Speichel versetzt. Davon werden jede Minute etwa 0,5 ml in eins der aus Versuchsteil (b) vorbereiteten Reagenzgläser getropft. Die Lösung im ersten Reagenzglas färbt sich intensiv blau. Danach wird die Blaufärbung zunehmend schwächer. Sobald sich keine Blaufärbung mehr einstellt werden 2 ml des mit Speichel versetzten Stärkekleisters mit 1 ml Benedict-Lösung versetzt und im Wasserbad erhitzt (Vorsicht! Schutzbrille tragen!). Die Lösung färbt sich rot.
Auswertung
Stärke ist ein Polysaccharid, welches aus mehreren tausend Glucosebausteinen aufgebaut
ist. Bei Anwesenheit von Wasser und von Stärke spaltenden Enzymen, den Amylasen, werden
die Stärkemoleküle in einzelne Glucosemoleküle gespalten (hydrolysiert). Die normale Speichel-
und die Pankreas-amylase greifen als Endo-amylasen oder a-Amylasen
statistisch in die Ketten ein und knabbern nicht vom Ende her.
(C6H10O5)n + (n-1) H2O ———> n C6H12O6
Man könnte meinen, dass nur n H2O-Moleküle benötigt werden. Denn pro glykosidischer Bindung wird ja nur ein H2O-Molekül eingebaut.
Dass jedoch das (n-1)-Modell richtig ist, kann man an folgender Darstellung zeigen. In eckigen Klammern stehen die Baueinheiten des Stärkemoleküls. Die Zahl n ist hier also gleich 5.
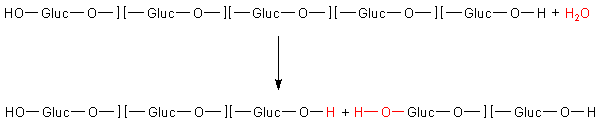
Wenn man das auf die ganze Kette anwendet, wird pro Mol Glucose nur ein Mol H2O
eingesetzt. Also stimmt das mit dem n?
Dazu muss man aber noch bedenken, dass ja der erste und der letzte Glucoserest zusammen formal
ein H2O mehr haben als die in eckigen Klammern stehenden Bausteine. Das wird deutlich,
wenn man ein Maltose-Molekül spaltet. Das Molekül vereinigt formal Anfang und Ende eines
Stärkemoleküls in sich. Hier ist n = 2.
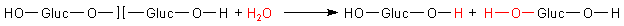
Grundsätzlich ist also (n-1) zu schreiben. Das gilt auch, wenn das Stärkemolekül aus 1000 Glucoseresten besteht. Dann benötigt man nur 999 Wassermoleküle zur Hydrolyse!
Aufgrund der Spaltung von Stärke ist diese immer weniger mit Iod-Kaliumiodid-Lösung nachweisbar. Nachdem sämtliche Stärkemoleküle zu Glucosemolekülen gespalten worden sind, lässt sich die Glucose mit Benedict-Lösung nachweisen.
Literatur
R. Blume, Chemie für Gymnasien, Organische Chemie Themenheft 3, Cornelsen Verlag, Berlin 1994, 46.