Informationen zu den Aromaten und Polykondensierten Aromaten (PAK) für Umweltwissenschaften
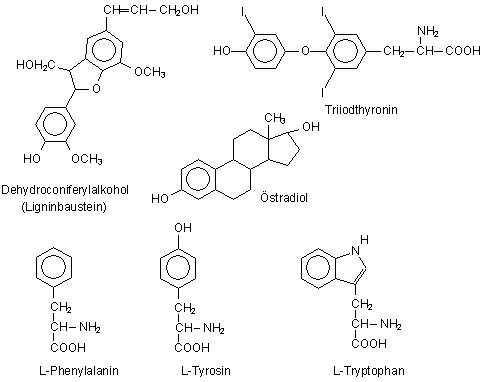
Aromatische Verbindungen sind nach den Kohlenhydraten die mengenmäßig wichtigste Stoffklasse der belebten Natur. So besteht der Gerüststoff des Holzes, das Lignin, aus verbrückten und mehrfach substituierten Benzolmolekülen. Damit ist ca. ein Viertel des organischen Kohlenstoffs fixiert. Weiter tragen eine Reihe essentieller Aminosäuren wie Phenylalanin, Tyrosin und Tryptophan aromatische Reste. Aromaten sind auch in vielen Vitaminen oder Hormonen wie Östrogen oder Triiodthyronin enthalten. Folglich sind auch in allen fossilen Brennstoffen von vornherein Aromaten zu finden.

Beispiele für biogene aromatische Verbindungen
Die Bezeichnung "aromatische Verbindungen" stammt aus der Frühzeit der Chemie, als man erkannte, dass viele Aromastoffe wie Vanillin, Anisol, Safrol oder Benzaldehyd letztlich auf Benzol zurückzuführen sind. Der Reihe der Aromaten sind auch viele Produkte der chemischen Industrie zuzuordnen, so etwa Kunststoffe wie Polystyrol oder die meisten Farbstoffe und viele Medikamente. Neben dem Erdöl ist vor allem der Steinkohlenteer Ausgangsmaterial zur Gewinnung aromatischer Verbindungen.
Der Grund: Zu den polykondensierten Aromaten gehört auch die Kohle. Deshalb entstehen beim Erhitzen der Kohle unter Luftabschluss sehr viele aromatische Verbindungen. Sie schlagen sich im hochtoxischen Steinkohlenteer nieder.
Hohe Konzentrationen von Benzol und seinen Homologen wie Toluol und Xylol sind in Treibstoffen für Verbrennungsmotoren enthalten. Die aromatischen Verbindungen entstehen vor allem bei der katalytischen Benzinveredelung (Platforming). Diese Verbindungen erhöhen die Klopffestigkeit des Benzins, da sie kaum Wasserstoff-Radikale bilden.
Bei der unvollständigen Verbrennung vieler organischer Substanzen entstehen geringe Mengen an Aromaten infolge von Crack- und Dehydrierungsreaktionen. Daher lassen sich in den Abgasen von Dieselmotoren und im Zigarettenrauch aromatische Verbindungen nachweisen.
1 Toxizität der Aromaten
Stadtkinder weisen einen um 70 % höheren Benzolgehalt im Blut auf als Kinder in Reinluftgebieten. Wie man besonders in den letzten Jahren erkannte, sind Benzol und einige seiner Substitutionsprodukte krebserregend. Von besonderer Bedeutung sind in diesem Zusammenhang polykondensierte Aromaten (PAK) wie das stark cancerogene 3,4-Benzpyren. Dieser Inhaltsstoff des Steinkohlenteers tritt aber auch in geringer Konzentration in Abgasen von Dieselmotoren, im Zigarettenrauch, im Schornsteinruß, in gegrillten und geräucherten Esswaren sowie in den Abgasen von Kraftwerken auf.
Die folgende Übersicht zeigt die am stärksten als Krebsauslöser wirkenden polykondensierten Aromaten (abgekürzt PAK, PAH oder PAh). Alle diese Verbindungen erzeugen bei Kontakt mit der Haut Hautkrebs. Bei Injektionen bildet sich in Versuchstieren Leber- und Lungen- sowie Knochenkrebs (Leukämie).
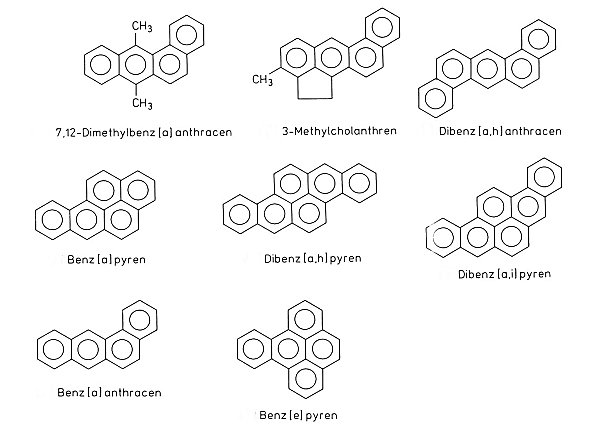
Die aktivsten Krebserzeuger unter den PAK
Für das Verständnis der Wirkung von Aromaten im Organismus ist es notwendig zu wissen, wie diese als nicht verwertbare und wasserunlösliche Nahrungsbestandteile im Stoffwechsel zur Ausscheidung über den Harn vorbereitet werden. Denn aromatische Kohlenwasserstoffe sind als meistens inerte Substanzen nicht von vornherein cancerogen, sondern werden erst im Organismus in Cancerogene umgewandelt. Zur Ausscheidung werden Aromaten durch spezifische Enzyme (unter Beteiligung von Cytochromen wie P 450) in Epoxide überführt und anschließend mit Glucuronsäure oder mit Aminosäuren sowie Glutathion oder Schwefelsäure verbunden, polar und damit wasserlöslich gemacht. Zu den genaueren Mechanismen der Epoxidbildung lies die Webseite zu den Dioxinen und Dibenzofuranen.
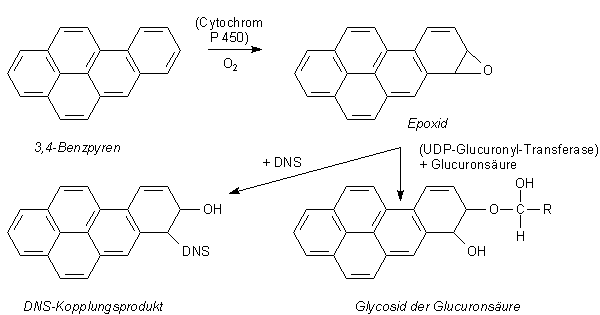
Bildung von Carcinogenen in der Zelle
Die intermediär gebildeten aromatischen Epoxide stellen im ungebundenen Zustand eine Gefahr für das Lebergewebe, Lungengewebe und für die Harnblase dar. Der Grund ist, dass die Epoxide mit Basen der DNS irreversible Bindungen eingehen, wodurch Allergien und sogar Krebs entstehen können. Dies ist ganz besonders dann der Fall, wenn die Epoxide zur DNS diffundieren und ankoppeln, bevor sie eine entgiftende Esterbindung eingehen. Die Wahrscheinlichkeit hierzu steigt mit zunehmender Konzentration von Aromaten in der Zelle, also auch mit der Aufnahme dieser Substanzen. Damit erklärt sich auch, dass nicht nur aktive Raucher, sondern auch Passivraucher ein erhöhtes Krebsrisiko aufweisen.
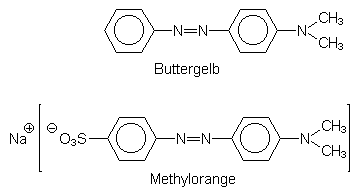
Formeln von Buttergelb und Methylorange
An dieser Stelle kann auch gedeutet werden, warum der Azofarbstoff Buttergelb stark cancerogen und deshalb seit 1938 verboten ist, während die ähnlich gebaute Verbindung Methylorange nicht cancerogen ist und sogar im Schulunterricht als Indikator verwendet werden darf. (Achtung: Methylorange ist trotzdem giftig und trägt das Gefahrensymbol (T) - aber nur als Feststoff.) Der Grund für die fehlende Cancerogenität ist, dass Methylorange wegen der polaren Sulfogruppe von vornherein wasserlöslich ist und in den Harn gelangt, während Buttergelb als fettlöslicher Farbstoff erst die oben geschilderten oxidativen Prozesse durchlaufen muss, um wasserlöslich zu werden. Dabei wird er in ein akutes, epoxidisches Cancerogen umgewandelt. Gleiches gilt auch für die Inhaltsstoffe von Nitritnachweisreagenzien: Lunges Reagenz (Naphthylamin, cancerogen) und Saltzmans Reagenz (N-(1-Naphthyl)-ethylendiamin-hydrochlorid, nicht cancerogen).
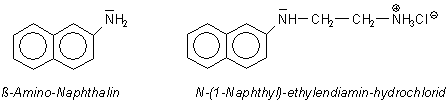 |
2 Aromaten und Umwelt
Mit Aromaten muss vorsichtig umgegangen werden. Auf einzelne unpolare Lösemittel wie Benzol (und neuerdings auch Toluol) verzichtet man gänzlich, obgleich diese Stoffe durch Verdunstung aus dem Benzin zu Zehntausenden von Tonnen in die Atmosphäre gelangen. Hier wirken sie als Treibhausgase und als Grundlage zur Bildung von Fotooxidantien und sogar von Nitrobenzol. Im Boden reichern sich die nicht flüchtigen PAK an, da sie als inerte Substanzen biologisch kaum abgebaut werden.
Als alternatives unpolares Lösemittel setzt man zunehmend das lipophile überkritische CO2 ein. Hierbei muss allerdings unter hohem Druck gearbeitet werden.
Beim Verbrennen der Aromaten werden auch deren Kohlenstoffgerüste letztendlich aufgebrochen. Da die Aromaten aber thermodynamisch äußerst stabil sind und deshalb deren Bildungsreaktion stark begünstigt ist, werden diese Verbindungen bei normalen Verbrennungsprozessen aus gesättigten Verbindungen häufig sogar erst gebildet. Dies betrifft vor allem Dioxine und Dibenzofurane. Auch Hochtemperaturverbrennung nutzt wenig, da in der Abkühlphase katalytisch an Metallkontakten (etwa im Staubfilter) die Aromatenbildung aus den CH-Radikalen erneut stattfindet.
Zur Entstehung von PAh bei Bränden und zur Analytik von belasteten Böden siehe unseren Tipp des Monats 02/2002, der sich mit einem konkreten Fall befasst.
Besonders bedenklich sind belastete Böden von Kokereien und anderen Industriebrachen. Die zur Reinigung vorgeschlagene Bodenverbrennung ist sehr aufwendig. Diese Böden können aber wie bei der Kontamination mit Kerosin durch speziell gezüchtete Mikroorganismen gereinigt werden. Besonders Pilze verfügen über Enzyme für ausgefeilte Ringöffnungsreaktionen, da sie vor allem von ligninhaltigem Holz leben. Durch die Oxidation der Abbauprodukte und deren Metabolisierung gewinnen die Mikroorganismen Energie und Baustoffe für die eigene Vermehrung.
Damit werden auch besonders stabile PAK zu CO2 und Wasser mineralisiert, wodurch der Kohlenstoffkreislauf aufrechterhalten wird.