Mehrfachbindungen - ganz einfach betrachtet
Das Besondere am Kohlenstoff ist, dass seine Atome Elektronenpaarbindungen zu anderen Kohlenstoffatomen eingehen können. Dabei gibt es nicht nur Einfachbindungen wie bei den Alkanen, sondern auch Doppelbindungen (bei den Alkenen und Aromaten) und sogar Dreifachbindungen beim Ethin.
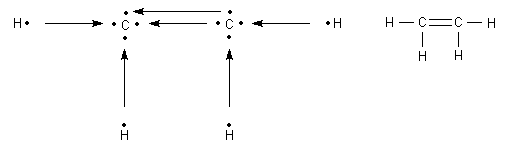
Auch diese Mehrfachbindung der ungesättigten Kohlenwasserstoffe lassen sich durch Elektronenpaarbindung über die vier Einzelelektronen des Kohlenstoffatoms beschreiben. Hier ist ein ganz einfaches Modell für die Entstehung einer Doppelbindung.

Die Darstellung des Ethenmoleküls ist noch nicht richtig. Da auch hier das Elektronenpaarabstoßungsmodell gilt und sich auch die Kerne der Wasserstoffatome abstoßen, muss man ebenfalls ein symmetrisches Molekül zeichnen.
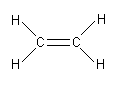
Das Molekül ist planar, alle Atome liegen in einer Ebene. Die Bindungswinkel betragen 360°/3=120°. Diese Symmetrie heißt "trigonal-planar".
Bei einem Alkin wie dem Acetylen bilden sich Dreifachbindungen zwischen den beiden C-Atomen aus.
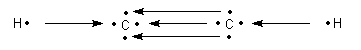
So findet man im Ethin die zwei Kohlenstoffatome mit den beiden Wasserstoffatomen in einer Linie hintereinander aufgereiht.
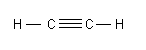
Weitere Texte zum Thema „Kohlenwasserstoffe“