| Klick mich an! |
 |
| HPLC-Anlage; rechts erkennt man die
25 cm lange Säule. Ihr Innendurchmesser beträgt nur 4 mm (Foto: Daggi) |
Bestimmung der Reinheit der Citronensäure durch
Chromatographie (HPLC)
Experimente:
Versuch: Herstellung von Calciumcitrat
Versuch: Gewinnung reiner Citronensäure mit Kationenaustauschern
Versuch: Dünnschichtchromatographische Analyse von Zitronensaft
Die Reinheit der hergestellten Citronensäure kann man chromatographisch untersuchen. Dazu bieten sich die Dünnschichtchromatographie (DC) (-> Versuch) sowie die Hochleistungs-Flüssigkeitschromatographie (HPLC) an. Letztere Abkürzung steht für High Performance Chromatography; es handelt sich also um ein hochauflösendes Chromatographieverfahren. Auf dieses soll hier genauer eingegangen werden.
Flüssigkeitschromatographie
Die Grundlagen der Chromatographie sind wohl jedem bekannt: Man füllt ein
Adsorbens (z. B. Kieselgel) in eine Trennsäule,
trägt eine Portion einer Lösung von verschiedenen Stoffen auf und desorbiert
(eluiert) durch kontinuierliche Zufuhr eines
geeigneten Lösemittels. Mit dem Durchwandern dieses Elutionsmittels gibt es ein
Gleichgewicht zwischen ständigem Desorbieren und erneutem Adsorbieren. Im Prinzip
handelt es sich also um eine kontinuierliche Extraktion. Da die gelösten Stoffe
unterschiedlich vom Adsorbens festgehalten werden, kommt beim Durchlaufen
der Säule zu einer Auftrennung. Die weniger gut adsorbierten Stoffe
werden als erste ausgespült, die am stärksten adsorbierten Stoffe verlassen als letzte
die Säule. Mit einem geeigneten Verfahren wie z. B. der Spektralanalyse oder mittels
der Messung der elektrischen Leitfähigkeit wird das Austreten der Stoffe verfolgt.
Diesen Apparateteil nennt man Detektor. Die Messsignale werden im
Signalwandler in Spannungsimpulse umgesetzt und dann auf einen Schreiber
geleitet. Man erhält ein Chromatogramm, wie es das folgende Bild zeigt.
Natürlich kann man die austretende Flüssigkeit auch portionsweise auffangen. Das Gerät heißt
Fraktionssammler.
Die HPLC-Methode
Es handelt sich bei der Flüssigkeitschromatographie um eine Wechselwirkung an den
Phasengrenzen, nämlich einer Verteilung eines Stoffes zwischen dem Adsorbens
und der eluierenden Flüssigkeit. Je größer man die Kontaktfläche zwischen den
Phasen macht, desto effektiver ist die Trennung. Das erreicht man, indem man das
Adsorbens besonders fein verteilt, also z. B. gut mörsert und fein aussiebt. Aus der
Praxis weiß man jedoch: Je feiner das Füllmaterial einer Säule ist, desto leichter
verstopft sie. Die Flüssigkeit wandert dann nicht mehr hindurch. Und man erhält
natürlich auch keine Auftrennung der gelösten Stoffe mehr.
Man kann sich aber mit einem Trick behelfen. Zur Vermeidung der Säulen-Verstopfung
muss man einfach den Lösemitteldruck erhöhen. Statt dem Luftdruck von
1,013 bar bei der normalen Chromatographie arbeitet man hier mit Drücken um 250
bar. Es sind sogar Drücke bis 350 bar möglich. (Manche übersetzen HPLC deshalb
auch mit High Pressure Liquid Chromatography.) Dafür sorgen gute Pumpensysteme.
Dann müssen aber auch Säulen und Leitungen besonders stabil sein. Deshalb fertigt
man diese aus Stahl. Es muss aber unbedingt Edelstahl "vom Feinsten" sein, denn
unter dem hohen Druck gibt es leicht Korrosionsprobleme.
Das Verfahren wirft eine Menge Probleme auf. Deshalb ist eine HPLC-Anlage (-> Bild) eine teure High-Tech-Anlage, die soviel kostet wie ein guter Mittelklassewagen. Beispielhaft nur ein kleines Problem: Die Messzelle des Detektors hält den hohen Druck nicht aus. Deshalb wird dort nicht mehr mit vollem Druck gearbeitet, sondern die Flüssigkeit muss vor Eintreten in die Messzelle, z. B. eine UV-Küvette, entspannt werden. Nun enthält jedes Lösemittel gelöste Luft; die Löslichkeit nimmt bekanntlich mit dem Druck zu. Beim Entspannen werden aber die unter Druck gelösten Gase freigesetzt; es kommt zur Bildung von großen Gasblasen. (Das ist bei Tauchern ein gefürchtetes Phänomen, das sich bei zu raschem Auftauchen in ihren Adern abspielt und zu Herz-, Gehirn- oder Lungenversagen führen kann: Caissonsche Krankheit.) Man erhält im Detektor keine vernünftigen Signale mehr. Vor dem Einsatz als Elutionsflüssigkeit muss man deshalb das Lösemittel entgasen. Man kennt das von der Sektflasche: Schüttelt man sie, gast und schäumt sie ganz besonders schön... Bei der HPLC schüttelt man eine halbe Stunde mit Ultraschall. Das rüttelt besonders effektiv. Es funktioniert auch mit einer Bierflasche...
| Klick mich an! |
 |
| HPLC-Anlage; rechts erkennt man die
25 cm lange Säule. Ihr Innendurchmesser beträgt nur 4 mm (Foto: Daggi) |
HPLC-Untersuchung der Citronensäure
Für jedes Problem gibt es spezielle Säulenfüllungen, also Adsorbentien. Wichtig ist,
dass die zu adsorbierenden Moleküle alle im gleichen Zustand vorliegen. Im Falle der Citronensäure
erreicht man das, indem man das Elutionsmittel (hier Wasser) sauer puffert. Dann
liegt die Citronensäure undissoziiert vor.
Die Bedingungen der Chromatographie waren:
Säule: Nucleosil® 100-5 C18 HD, 250 mm x 4 mm
Detektion: UV, 210 nm
Fließmittel: wässrige Lösung von NaH2PO4, c = 50 mmol/l, pH 2,8
Probenvolumen: 5 ml
Ausflussgeschwindigkeit: 0,7 ml/min
Durch einen Vorversuch mit reiner Citronensäurelösung wurde ermittelt, dass Citronensäure eine Retentionszeit von etwa 7,6 min hat.
Die Messungen lieferten folgende Chromatogramme:
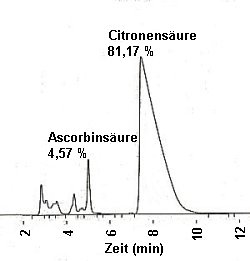
Chromatogramm von Zitronensaft |
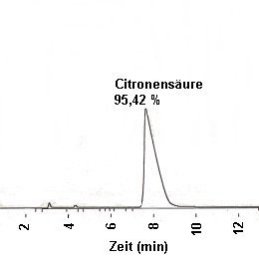
Chromatogramm von selbst hergestellter Citronensäure |
Man erkennt, dass unsere mit Hilfe eines sauren Kationenaustauschers (->
Versuch) hergestellte Citronensäure einen Reinheitsgrad von 95,42 % hat. Die
unterschiedliche Peakhöhe in beiden Abbildungen ist unwichtig; es kommt vielmehr auf das
Verhältnis der Peakflächen (ausgedrückt in %) an.
Weitere Texte zum Thema „Zitrone“