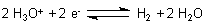
Die Standardwasserstoffelektrode
Elemente ordnet man entsprechend ihrer Redoxeigenschaften ein. Das kann man
aber nur relativ machen. Kupfer ist zum Beispiel edler als Eisen, aber unedler als
Silber. Zur genauen Beschreibung misst man die Spannung zwischen den jeweiligen
Elementen in den Lösungen, die ihre Ionen enthalten. So entstand die
Spannungsreihe der Elemente.
Worauf aber soll man die Spannungen beziehen? Schließlich kann man ja nicht jede
Elektrode gegen jede andere vermessen.
Man hat sich international auf das Wasserstoffsystem als Bezugspotential geeinigt.
Man definiert sein Potential als Null Volt. Dessen Redoxgleichgewicht beschreibt die
folgende Reaktionsgleichung.
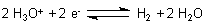
Zur Messung benötigt man eine genormte Elektrode. Das ist die so genannte
Standardwasserstoffelektrode, eine mit feinem Platin überzogene ("platinierte")
Platinelektrode, die man in eine Salzsäure mit der Konzentration (genau: Aktivität) c
= 1 mol/l (genau: mit der Aktivität 1)
taucht. Sie wird von gasförmigem Wasserstoff, der unter dem Normaldruck
von 1,013 bar steht, umströmt. Die Temperatur des Systems beträgt 25 °C.
Diese Elektrode schaltet man über eine Salzbrücke gegen die zu untersuchenden
Elektroden. Mit der Salzbrücke vermeidet man, dass sich die Elektrolytlösungen der
beiden Elektrodenräume vermischen. Die damit gemessenen Spannungswerte sind
diejenigen, die man in den Tabellen ("Spannungsreihe") als Standardpotentiale der
jeweiligen Elemente oder Verbindungen aufgelistet findet.
Ein negatives Potential bekommen diejenigen Elemente und Verbindungen, die
Elektronen auf Wasserstoff-Ionen übertragen und diese entladen können.
Zn + 2 H3O+ ———> Zn2+ + H2 + 2 H2O
Ein positives Potential haben dagegen die Elemente und Verbindungen, die nicht von Wasserstoff-Ionen oxidiert werden. Dazu gehören Kupfer und alle Edelmetalle wie Gold und Platin.
Wir sehen also, dass die Definition des Wasserstoffsystems als Bezugspunkt sinnvoll ist. Denn er trennt die unedlen von den edlen Metallen. Erstere reagieren mit Wasserstoffsäuren unter Wasserstoffentwicklung und Salzbildung, letztere dagegen nicht. Zur Zersetzung von Silber, Gold oder Platin müssen stärkere Oxidationsmittel wie die Anionen der Salpetersäure oder Königswasser (eine Mischung von Salpeter- und Salzsäure) gewählt werden.
Weitere Texte zum Thema „Elektrochemie“