
Aufklšrung der Struktur des EssigsšuremolekŁls
Experimente:
Versuch: Die Verbrennungsprodukte der Essigsšure
Versuch: Iodoformprobe
Versuch: Wie viele Protonen setzt ein EssigsšuremolekŁl frei?
Die Elementarzusammensetzung
Wenn wir Essigsšure verbrennen, erhalten wir als Verbrennungsprodukte Kohlenstoffdioxid bzw. RuŖ sowie
Wasser (-> Versuch). Essigsšure ist also eine Kohlenwasserstoffverbindung.
Genaue Analysen zeigen, dass das MolekŁl auch noch gebundenen Sauerstoff enthšlt.
Die Elementaranalyse ergibt
| Masseprozent | Atommasse | Quotient % / M | |
| Kohlenstoff | 39,80 % | 12 | 3,32 |
| Wasserstoff | 6,85 % | 1,008 | 6,8 |
| Sauerstoff | 53,34 % | 16 | 3,33 |
Die Ermittlung der chemischen Formel
Hierzu werden die Quotienten in der obigen Tabelle verglichen:
C : H : O = 3,32 : 6,8 : 3,33 » 1 : 2 : 1
Die einfachste Formel wšre demnach
CH2O
Als 1814 Berzelius die erste Formel der Essigsšure aufstellte, war dies tatsšchlich seine Annahme.
Die Formel kann aber noch ein Vielfaches davon sein, zum Beispiel C2H4O2.
Wir benŲtigen also ein Verfahren, um die Molmasse der Essigsšure zu bestimmen. Dazu verdampft man in einem Volumen Essigsšure und bestimmt die Dichte des Dampfes. Daraus kann man mit Hilfe der Avogadrozahl die Molmasse bestimmen. Sie liegt bei 60 g / mol. Das spricht also fŁr die Formel
C2H4O2
Mit Hilfe der Gefrierpunktserniedrigung hat man ebenfalls die MŲglichkeit, die Molmasse zu bestimmen. Da man dazu aber unpolare LŲsemittel wie zum Beispiel Benzol nimmt, in denen die EssigsšuremolekŁle als Dimere vorliegen, bekommt man als Formel C4H8O4. Auch diese Formel begegnet einem hier und da, wie zum Beispiel in einem alten franzŲsischen Schulbuch von 1875.
Die Struktur der EssigsšuremolekŁle
Die einfache Iodoformprobe (-> Versuch) sollte genaueren Einblick in die
Struktur der MolekŁle geben. Sie hat zur Voraussetzung, dass eine aktivierte Methylgruppe vorhanden ist. Beispiele fŁr
solche MolekŁle sind Ethanol, Acetaldehyd und Aceton.
CH3-CH2OH CH3-CHO CH3-CO-CH3
Es bildet sich bei dieser Probe das nach Krankenhaus duftende, weiŖgelbe feste Iodoform CHI3.
Mit Essigsšure oder Acetat verlšuft die Reaktion leider nicht eindeutig, so dass wir sie nicht empfehlen wollen. Die LŲsung wird nur gelb, und man stellt nur ab zu den typischen Geruch fest. Dabei sollte man beachten, dass Iodoform wie Chloroform Nerven betšubt und den Geruchssinn stŲrt. Deshalb darf man vorher keine Geruchsprobe mit hochkonzentriertem Iodoform machen, wenn man Spuren schnuppern will!
Trotzdem halten wir fest: Auch die Essigsšure tršgt eine Methylgruppe.
CH3-COOH

(Foto: Blume)
Welche Wasserstoffatome gibt Essigsšure als Protonen ab?
Hierzu kommen zwei MŲglichkeiten in Frage: Drei Wasserstoffatome befinden sich in der Methylgruppe, eines in der
Carboxylgruppe.
Zur Klšrung tršgt eine einfache Titration bei (-> Versuch). Da ein Mol Natronlauge
mit einem Mol Essigsšure reagiert, ist nur folgende MŲglichkeit richtig: Essigsšure ist eine einbasige Sšure.
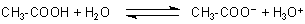
Weitere Texte zum Thema ĄEssigď