 |
 |
 |
 |
| Kurze Fragen - Kurze Antworten
Aus dem E-Mail-Korb von Professor Blume |
1621
F: Bei uns steht eine große Eisenbahnbrücke. Wenn ich bei schwachem Wind unter der
Brücke durchgehe, wird es plötzlich stark windig, so dass es einem fast den Atem nimmt. Nachdem ich unter der Brücke durch
bin, ist der Wind wieder kaum spürbar. Wie kommt das?
A: Das ist zwar eine physikalische Frage, aber ich will´s versuchen.
Ihnen strömt Luft entgegen. Auf dem freien Feld kann sie ungehindert fließen. Wenn dem Wind als Hindernis eine Brücke im Weg steht, muss er ja trotzdem die Luftportion durchdrücken, die der auf freiem Feld entspricht. Das heißt, dass die Luft in der Verschmalung oder „Taille“ schneller fließen muss. Also ist es dort windiger! Hier ist das Bild einer Doppelbrücke, bei der man das deutlich spürt.

Die Talbrücke in Bielefeld-Schildesche (Foto: Blume)
Dieser Effekt wird durch das Gesetz von Bernoulli beschrieben. Eine seiner Aussagen ist: Durch jeden Querschnitt strömt pro Zeiteinheit die gleiche Luftmenge.
Man kann den Effekt auch beim fließenden Wasser, z. B. bei der Steinernen Brück in Regensburg beobachten: Wenn ein Fluss schmaler wird, fließt er einfach schneller! Der Effekt spielt auch beim Fliegen eine Rolle. Schnelles Fließen bedeutet Erzeugung von Unterdruck. Die Flügel normaler Flugzeuge (und auch die Vogelflügel!) sind so gewölbt, dass die Luft über ihnen schneller fließt als darunter. Deshalb gibt es einen Saugdruck, der nach oben wirkt und das Flugzeug so lange oben hält, wie die Strömung nicht abbricht. Auch die Wasserstrahlpumpen im Labor wirken letztlich so.
Ob der Saugdruck unter der Brücke allerdings ausreicht, auch Ihre Atembeschwerden, die Sie unter der Brücke spüren, zu erklären, kann ich nicht beurteilen.
Zu einer anderen, erstaunlichen Abwendung des Gesetzes von Bernoulli klicke hier.
1622
F1: Salzlösungen und Salzschmelzen leiten bekanntlich den elektrischen Strom. Dabei
sind Ionen für den Stromtransport verantwortlich. Tritt dabei in jedem Fall eine Elektrolyse ein?
Mir ist nicht klar, wie sonst ein Stromkreis zustande kommen sollte, wenn die Ionen nicht an den jeweiligen Elektroden
entladen würden. Bitte um Aufklärung.
A1: Interessante Frage!
Es tritt tatsächlich immer eine Elektrolyse ein – wenn man mit Gleichstrom arbeitet.
Bei Salzschmelzen wie Bleichlorid sind davon immer die Ionen des geschmolzenen Salzes betroffen. Es bilden sich augenblicklich Blei und Chlor.
Bei Salzlösungen werden oftmals nicht die Salz-Ionen entladen, sondern eher die Ionen des Wassersystems, wobei Wasserstoff und/oder Sauerstoff entstehen. Das ist aber eine Frage a) der Ionenarten und b) der Konzentration.
Ein Beispiel: Bei der Elektrolyse von konzentrierten Kupfer(II)-chlorid-Lösungen bilden sich Kupfer und Chlor. Verdünnte
Lösungen ergeben daneben schon eine Menge an Wasserstoff und Sauerstoff.
Konzentrierte Kupfer(II)-sulfat-Lösungen dagegen ergeben Kupfer und Sauerstoff, da Sulfat die anodische Sauerstoffbildung
aus Wasser katalysiert.
Für Schmelzen von Salzhydraten gilt das Gleiche wie für sehr konzentrierte Lösungen.
Die sofort einsetzende Elektrolyse führt dazu, dass die Leitfähigkeit rasch absinkt. Denn die Elektrodenoberflächen werden belegt, die Ionen müssen durch die Lösung wandern (quasi „gezerrt werden“). Damit steigt der Widerstand, die reziproke Leitfähigkeit nimmt ab.
Um diese störende Elektrolyse zu vermeiden, arbeitet man deshalb bei Leitfähigkeitsmessungen mit hochfrequentem Wechselstrom – mit weit über 1000 Hertz. Da werden die Ionen hin- und hergeschickt, ohne dass sie viel wandern müssen oder sich gar abscheiden.
Für Schulzwecke reicht es aus, mit Wechselstrom (50 Hz) zu arbeiten. Aber den darf man nur wenige Sekunden einwirken lassen! Sonst gibt es Knallgasexplosionen!
F2: Herzlichen Dank für die schnelle und sehr hilfreiche Beantwortung!
A2: Das war mir ein Vergnügen und hält dazu noch mein Gehirn fit.
1623
F: Zu Silvester sieht man immer wieder Raketen. Oder man sieht sie im Fernsehen, wenn mal
wieder eine Weltraumfähre startet. Gibt es ein kindgerechtes Modell für eine Rakete?
A: Die meisten Leute meinen, es sei der Rückstoß des ausströmenden Gases bzw. seiner
Teilchen, der den Ballon vorantreibt. Das stimmt leider nicht!
Um das zu verdeutlichen, nehmen Sie einen Luftballon, blasen Sie den richtig auf und lassen Sie ihn dann los. Er wird sofort mit hohem Tempo und lautem Zischen in die Richtung wegfliegen, in die Sie ihn gehalten haben.
Wie kommt das? Im Ballon sind Luftteilchen eingeschlossen. Diese „Moleküle“ bewegen sich sehr rasch (mit weit über Schallgeschwindigkeit, also über 1000 km/Stunde!). Sie stoßen auf die Ballonwand und üben darauf Kräfte aus. Stellen Sie sich vor, dass im Ballon eine Gruppe Kinder ständig Fußbälle gegen die Ballonwand schießt. Aus diesem Grund bleibt der Ballon überhaupt aufgebläht.
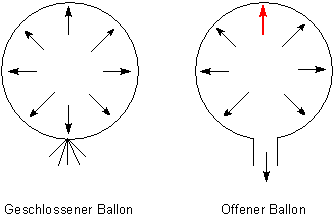
Wenn der Ballon geschlossen ist, heben sich die Kräfte, die auf gegenüberliegenden Seiten wirken, gegenseitig auf. Zum Beispiel drücken die Moleküle auf der einen Seite nach rechts und auf der gegenüberliegenden Seite nach links. Oder sie stoßen nach oben und unten, nach vorn und nach hinten. Also bleibt der Ballon insgesamt liegen.
Ist der Ballon aber hinten offen, so kann die Luft an der Öffnung keine Kraft mehr auf die Innenseite der Ballonwand ausüben und strömt nur aus. Auf der gegenüberliegenden Seite des Ballons jedoch stoßen die Luftmoleküle fleißig weiter auf die Ballonhülle. Das wirkt sich nun so aus, dass der Ballon von innen vorwärts gedrückt wird. Der Ballon zischt in diese Richtung weg.
Es ist also keineswegs der Rückstoß der ausströmenden Teilchen, der den Ballon vorantreibt, sondern es ist die Kraft der verbleibenden Moleküle, die auf diejenige Seite stoßen, die der Ausström-Öffnung gegenüberliegt. Das erzeugt den „Schub“, der den Ballon vorwärts schiebt. Leider werden durch den Druck der gedehnten Ballonhülle nach und nach alle Luftmoleküle herausgedrückt - letztlich auch diejenigen, die den Ballon vorantreiben. Dann stürzt der Ballon ab.
So ist es auch in der richtigen Rakete. Nur werden hier die ausströmenden Gase durch Verbrennung explosiver Substanzen wie Schwarzpulver oder Sauerstoff/Wasserstoffmischungen erzeugt. Weil die Gase äußerst heiß sind, sind auch die Moleküle sehr viel schneller als die der kalten Luft. So können sie ein so schweres Gerät wie die Weltraumfähre ins Weltall wuchten. Es wird solange geschoben, wie Brennstoffe neue Gase erzeugen. Dann ist auch hier Schluss - eben Brennschluss.
Für Fachleute sei gesagt, dass es bei all dem Geschilderten um die Begriffe Impuls und Gegenimpuls geht. Das ist aber für Anfänger zu schwierig.
1624
F: Wie funktionieren die nachts im Scheinwerferlicht hell leuchtenden Reflektorenstreifen für
Radfahrer oder Rettungskräfte?
A: Diese Reflektoren bestehen aus kleinsten Glaskügelchen, die in einer dünnen Schicht auf
einer Trägerfolie fixiert sind. Die Kügelchen sind so klein, dass etwa 25.000 von ihnen auf einen Quadratzentimeter passen.
Dass sie bei Beleuchtung so hell leuchten, beruht auf einem physikalischen Trick. Licht, das in so ein Kügelchen einfällt, wird
zunächst gebrochen, dann an der Rückwand reflektiert und anschließend erneut gebrochen. Wenn der Lichtstrahl das Kügelchen verlässt,
hat er die gleiche Richtung wie die, aus der er kam.

Das führt dazu, dass derjenige, der das Objekt anstrahlt, dieses auch am hellsten wahrnimmt. Man spricht von Retroreflexion.
1625
F: Zunächst einmal möchte ich Ihre Seite loben, sie hat mir schon oft geholfen! Nun habe
ich aber eine Aufgabe in der ich erklären soll, warum Purin ein Aromat ist. Überall finde ich dieses, komme selbst aber nur auf
8 Elektronen und nicht auf 10. Können Sie mir da helfen?
A: Purin ist planar gebaut und tatsächlich eine aromatische Verbindung.
Zwar erkennen Sie auf den ersten Blick nur 4 Doppelbindungen und somit nur 8 p-Elektronen – was nicht der Hückelregel entsprechen würde. (Die Hückelregel („4n + 2“) beschreiben wir hier.)
Sie müssen jedoch die nichtbindenden Elektronen des NH-Stickstoffs im Seitenring mit einkalkulieren. Aufgrund der Tautomerie des H-Atoms von NH nimmt das nichtbindende Elektronenpaar an der Mesomerie des Gesamtsystems teil. Somit ist Purin ein Aromat mit 10 p-Elektronen, welcher der Hückelregel folgt (Hückelzahl 2). Man spricht von einem elektronenreichen Aromaten.
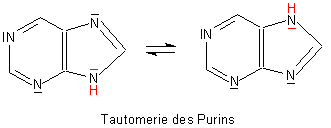
Die nichtbindenden Elektronenpaare der anderen N-Atome sind nicht an der Mesomerie beteiligt, sind also nicht delokalisiert. Ein Tipp: Wenn Sie die mesomeren Grenzstrukturen des Purins entwerfen, müssen Sie Ladungstrennungen vornehmen (also NH+ und N- sowie C-).
Vergleichen Sie das Ganze mit Imidazol (Hückelzahl 1) mit seinen 6 (genau genommen: 4 vom Kohlenstoff und 2 vom NH) p-Elektronen. Schließlich ist Purin ja nichts anderes als Imidazo[4,5-d]pyrimidin.
Wenn wir schon dabei sind: Pyrimidin ist anders als Purin ein elektronenarmer Aromat. Das liegt daran, dass die stärkere Elektronegativität der N-Atome die Delokalisierung der p-Elektronen der Kohlenstoffatome erschwert.