Wann ist eine Verbindung ein Aromat?
Es ist oftmals bei der Betrachtung einer Strukturformel gar nicht so einfach zu entscheiden, ob es sich bei dem Molek³l um einen Aromaten oder eine andere Verbindung handelt.
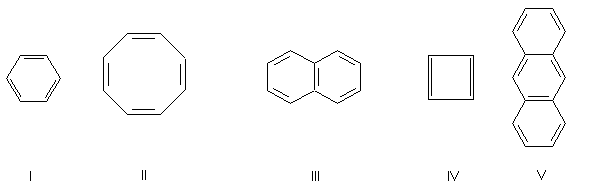
Handelt es sich bei folgenden Molek³len um Aromaten?

Zum Gl³ck gibt es einige Regeln, ³ber die ein aromatisches Molek³l eindeutig als solches zu erkennen ist.
Erkennungskriterien von Aromaten
Die H³ckel-Regel
Die H³ckel-Regel besagt, dass eine ungesõttigte, ringf÷rmige Substanz nur dann ein Aromat ist,
wenn f³r die Zahl der π-Elektronen in ihrem konjugierten Ringsystem folgende Beziehung gilt.
(4n + 2) π-Elektronen mit n = 0, 1, 2, 3,...
Das Symbol n ist eine positive, ganze Laufzahl. (n ist ³brigens nicht die Zahl der Ringe! Darauf wird gern geschlossen, weil dies ausgerechnet bei Benzol, Naphthalin und Anthracen zutrifft.)
Ein Beispiel f³r n = 0 ist eine exotische Verbindung, das Cyclopropenylium-Kation.
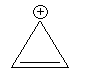
Hier ist kein System von konjugierten Doppelbindungen vorhanden. Die H³ckel-Regel gilt aber f³r n = 0; dann ist nõmlich 4 x 0 + 2 = 2. Diese zwei π-Elektronen sind tatsõchlich im Ring delokalisiert. Damit ist das Cyclopropenylium-Kation ein Aromat.
Aromaten sind also planare carbocyclische Verbindungen mit 2, 6, 10, 14, 18 (usw.) π-Elektronen im Ring. Nur diese k÷nnen mesomeriestabilisiert sein.
Was ist ein Antiaromat?
Eine carbocyclische Verbindung mit einer geraden Anzahl an π-Elektronenpaaren nennt man Antiaromat.
Solche Verbindungen entsprechen nicht der H³ckel-Regel. Antiaromaten k÷nnen, m³ssen aber nicht planar sein.
Ein Beispiel ist das Cyclobutadien.

Sein Molek³l ist zwar planar gebaut, seine Doppelbindungen sind konjugiert. Das spricht f³r das Vorliegen eines
Aromaten.
Die Zahl seiner π-Elektronen betrõgt 4. Wenden wir also die H³ckel-Regel an. Ist das m÷glich: (4n + 2) => 4?
Nein. Es gibt somit keine Zahl n, f³r die, wenn man sie in die H³ckel-Formel einsetzt, 4 herauskõme!
Cyclobutadien ist tatsõchlich kein Aromat. Denn die Doppelbindungen im Ring sind fest fixiert. Man muss
sogar Energie hineinstecken, damit diese ihre Position im Ring wechseln. Letztlich ist Cyclobutadien ein Alken
- genau ein Alk-dien.
Pseudo- oder Quasiaromaten
Viele denken, dass der Begriff der Aromatizitõt nur die Organische Chemie betrifft. Es gibt jedoch auch in der Anorganischen
Chemie Beispiele f³r aromatische Verbindungen, die auch ohne das Element Kohlenstoff auskommen.
Ein bekanntes Beispiel ist das Schwefel-Kation S42+. Es hat 6 delokalisierte Elektronen. Es erf³llt damit formal die H³ckel-4n+2-Regel und ist damit als aromatisch zu bezeichnen. Um "klassische" (also organische) Aromaten wie das Benzol von den anorganischen zu unterscheiden, hat man die Begriffe pseudo- oder quasiaromatisch eingef³hrt.
Hier sind zwei wichtige Grenzstrukturen der mesomeren Zustõnde des Schwefel-Kations.
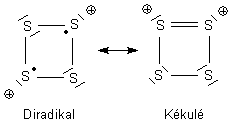
Es gibt noch eine weniger wahrscheinliche co-ionische Struktur, bei der ein S-Atom zwei positive Ladungen trõgt.
Literatur:
Ralf Alsfasser, H. J. Meyer: Moderne Anorganische Chemie, de Gruyter, 2007
Mit diesen Informationen ausgestattet k÷nnen wir uns die obigen Stoff-Beispiele
genauer betrachten
Wie alle Regeln in der Chemie hat auch diese Regel ihre Grenzen
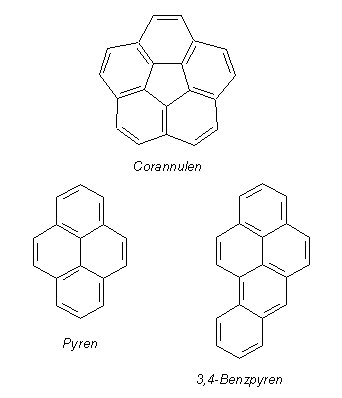
Will man z. B. klõren, ob Corannulen oder Pyren
bzw. 3,4-Benzpyren Aromaten sind, so sind die o. a. formulierten Erkennungskriterien nicht besonders hilfreich.
Pyren hat 16 π-Elektronen. Corannulen und Benzpyren haben die π-Elektronenzahl 20, also 10 Elektronenpaare.
Die H³ckel-Regel sagt "Nein". Hinzu kommt, dass Corannulen nicht einmal planar ist. Dennoch haben die drei
Verbindungen die spektroskopischen und chemischen Eigenschaften von aromatischen Verbindungen. Man nennt sie ³brigens
auch polykondensierte Aromaten (PAK).
Weitere Texte zum Thema äKohlenwasserstoffeō