 |
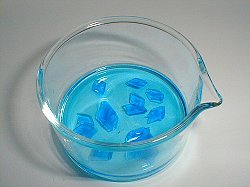
| Kupfersulfat-Impfkristalle
(Foto: Daggi) |
Vorbereitungen zur Kristallzüchtung
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
|
Besonders viel Spaß macht das Kristallzüchten. Leider gelingt das gerade mit den gängigen Haushaltschemikalien Kochsalz und Zucker (Saccharose) nicht, so dass man auf Salze wie Kupfersulfat (Kupfervitriol), Seignettesalz oder Alaun zurückgreifen muss. Diese sind mindergiftig, so dass man beim Arbeiten aufpassen muss. Vor allem ist Sauberkeit gefragt. Verschüttete Lösungen werden sofort aufgewischt (usw.). |
Stelle dir eine gesättigte Lösung (Lösung mit Bodensatz) aus Kupfersulfat, Seignettesalz oder Alaun in etwa 100 ml destilliertem Wasser her.
Für einen Liter einer bei Zimmertemperatur gesättigten Lösung brauchen wir etwa:
(Die Salze bekommst du in der Apotheke. Auch kann dir die Schule bei der Beschaffung über den Chemikalienhandel behilflich sein.)
Beachte, dass das Herstellen einer gesättigten Lösung lange dauern kann und einfaches Einrühren
meistens nicht ausreicht. Deshalb ist es gut, wenn du die zuvor gut gerührte Lösung mit
Bodensatz einige Tage stehen lässt und erneut ab und zu gut umrührst.
Filtriere die Lösung durch einen Kaffeefilter und fülle dann davon 1-2 cm hoch in eine flache,
saubere Schale.
Die Schale wird anschließend an einen gleichmäßig temperierten Ort gestellt. Der Kühlschrank
eignet sich hierfür am Besten.
Darauf achten, dass kleine Kinder nicht an die Lösung gelangen können.
Nach einiger Zeit scheiden sich am Boden allmählich Kristalle ab, die je nach Stoffart über einen cm groß werden können. Je erschütterungsfreier die Lösung steht, desto schönere Kristalle bilden sich.
 |
| Kupfersulfat-Impfkristalle
(Foto: Daggi) |
Zur Züchtung größerer Kristalle suchst du die schönsten mit einer Pinzette aus, filtrierst die
Lösung in eine neue Schale und gibst die ausgelesenen Kristalle zum weiteren Wachstum wieder
hinein. Die schönsten Kristalle dienen als Impfkristalle für die folgenden
Versuche.
Wichtiger Hinweis
Viele in den Geschäften und Supermärkten käufliche Speisesalzarten enthalten Zusatzstoffe, die die
völlige Lösbarkeit verhindern. Aus solchen trüben Lösungen könnt Ihr natürlich keine Kristalle züchten!
Deshalb müsst ihr reines Natriumchlorid beschaffen. Testet aber erst einmal alle Salzprodukte, die
ihr zu Hause findet. Vielleicht ist eine Sorte dabei, die sich völlig lösen lässt. Denkt auch an
große Streusalzkristalle, die Ihr auslesen könntet!
Zur schlechten Löslichkeit des Speisesalzes und der Trübung seiner Lösung sagen wir etwas in einem
Tipp des Monats. Aber es sei gleich vorneweg gesagt: Durch Zusatz von
einigen Tropfen Essigsäure (verrühren!) lässt sich das Problem (fast immer) beseitigen.