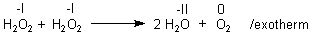
Eine Reaktion - verschiedene Katalysatoren
Experimente:
Versuch: H2O2-Zerfall und verschiedene Katalysatoren
Versuch: Verschiedene Wege zur Hydrolyse von Stärke
Versuch: Verschiedene Wege zur Hydrolyse von Proteinen
Ein und dieselbe Reaktion kann durch verschiedene Katalysatoren unterschiedlich
beeinflusst werden. Hierfür gibt es viele Beispiele.
Wasserstoffperoxid reagiert je nach Umgebung als Oxidations- und als
Reduktionsmittel. Deshalb neigt es besonders zur Selbstzersetzung.
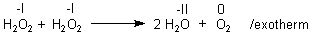
Hydrolysen von Kohlehydraten wie Stärke oder Cellulose lassen sich durch
Protonen katalysieren. Effektiver sind jedoch auch Enzyme, die Amylasen oder
Cellulasen. Im Versuch stellt man fest, dass die enzymatische Spaltung
der Stärke durch das Enzym Amylase bei Zimmertemperatur abläuft, während die
Säurekatalyse Siedetemperaturen erfordert. Die Amylase senkt also die
Aktivierungsenergie kräftig ab.
Gleiches gilt auch für Proteasen (-> Versuch).
Wie die Kenngrößen einer chemischen Reaktion, nämlich
zusammenhängen und durch Katalysatoren beeinflusst werden, beleuchten wir in einer besonderen Webseite für Spezialisten.
Zur Chemie mit Wasserstoffperoxid haben wir eine große
Webseitengruppe.
Weitere Texte zum Thema „Katalyse“