Versuch: Potentiometrische Titration von Chlorid
Schülerversuch; 45 min.
Beim Experimentieren den Allgemeinen Warnhinweis unbedingt beachten.
Geräte
Becherglas (50 ml), vor Licht geschützte Bürette (Braunglas, 50 ml), Magnetrührwerk,
Millivolt-Meter, Silberstabelektrode. Als Bezugselektrode nimmt man am
besten eine Mercurisulfatelektrode (wie wir es in unserer Messung
getan haben). Es geht aber auch mit einer Kalomel- oder einer Silberchloridelektrode.
Allerdings sollte man dann etwas schnell arbeiten, um den Fehler, der durch die aus dem
Diaphragma austretende Chloridlösung entsteht, gering zu halten.
Chemikalien
NaCl-Lösung (c = 0,01 mol/l); frisch zubereitete AgNO3-Lösung (c = 0,01 mol/l)
(Xi) (im Dunkeln aufbewahren!), verdünnte Schwefelsäure (w = 1 %) (Xi).
Durchführung
In das Becherglas füllt man 25 ml der NaCl-Lösung und tropft etwas Schwefelsäure zu.
Dann taucht man beide Elektroden in die Lösung ein und schließt sie an das Voltmeter an.
Anschließend misst man den Start-Spannungswert. Man tropft 2 ml AgNO3-Lösung zu,
wartet, bis der Spannungswert konstant ist und notiert den Wert. So verfährt man bis in die Nähe
des erwarteten Äquivalenzpunkts, erkenntlich am deutlichen Potentialsprung. In diesem Bereich
titriert man in kleineren Schritten. Danach gibt man wieder in größeren Schritten mindestens
noch 20 ml Silbernitratlösung hinzu.
Nach dem Ende der Titration muss die restliche Silbernitratlösung aus der Bürette auslaufen. Sehr gut mit destilliertem Wasser nachspülen!
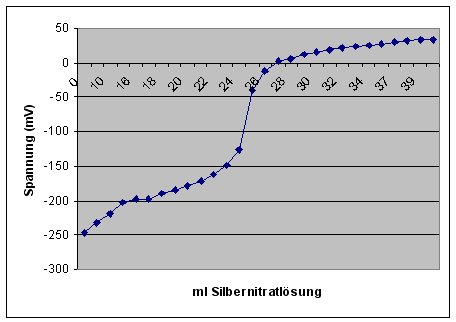
Man zeichnet in ein Diagramm die Spannungswerte gegen die ml-Zahl der Silbernitratlösung.
Ergebnis
Die gemessene Kurve hat erwartungsgemäß einen steilen Wendepunkt bei 25 ml. Hier liegt der
Äquivalenzpunkt.

Verwendete Elektroden: Silberstab gegen Mercurisulfat
Weitere Experimente zum Thema „Salz“
Weitere Texte zum Thema „Salz“