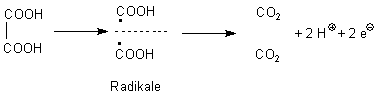
Reduzierende Eigenschaften des Oxals‰uresystems
Experimente
Versuch: Oxals‰ure als Reduktionsmittel
Versuch: Bestimmung einer unbekannten Oxals‰urekonzentration mit
Kaliumpermanganat
Eine der hervorstechenden Eigenschaften der Oxals‰ure ist ihre Reduktionswirkung. Darauf
beruhen nicht nur einige Nachweisreaktionen, sondern auch viele
ihrer technischen Verwendungen, so zum Beispiel als Bleichmittel
oder in der Analytik (Oximetrie; insbesondere bei der Manganometrie).
Die Oxidation der Oxals‰ure
Das Molek¸l der Oxals‰ure hat sozusagen eine Sollbruchstelle zwischen den beiden C-Atomen.
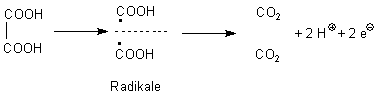
Bei der Spaltung ‰ndert sich die Oxidationszahl der C-Atome von (+III) nach (+IV). Somit ist die Oxals‰ure ein Reduktionsmittel.
Oxidation: ÝHCOOC-COOH ———> 2 CO2 + 2 H+ + 2 e- E0 = -0,49 V
Das gleiche gilt f¸r die Salze der Oxals‰ure, die Oxalate.
Es gibt eine Reihe von Oxidationsmitteln f¸r die Oxals‰ure
Am meisten wird Kaliumpermanganat verwendet.
Reduktion: MnO4- + 8 H+ + 5 e- ———>ÝMn2+ + 4 H2O
ƒhnlich verl‰uft die Reaktion mit Chromat und Dichromat.
Reduktion: CrO42- + 8 H+ + 3 e- ———>ÝCr3+ + 4 H2O
Hexacyanoferrat(III) (Rotes Blutlaugensalz) wird unter Lichteinwirkung zu Hexacyanoferrat(II) reduziert.
Reduktion: [Fe(CN)6]3- + e- ———> [Fe(CN)6]4-
Mit ammoniakalischer Silbernitratlˆsung bildet sich ein schwarzer Niederschlag von Silber.
Reduktion: ÝAg+ + e- ———> Ag
Die bekannte Fehling-Reaktion mit Kupfer(II) als Oxidationsmittel ist jedoch negativ.
Weitere Texte zum Thema "Oxals‰ure"