Zur Chemie der Phthalsäure
Experimente:
Versuch: Synthese von Phenolphthalein
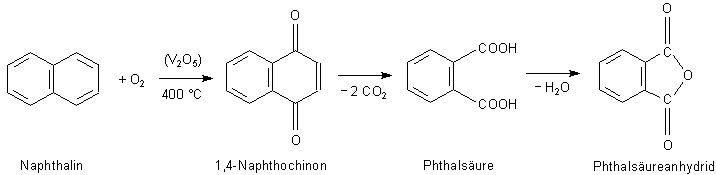
Der Name der Phthalsäure kommt vom Naphthalin. Denn bei dessen Oxidation entsteht
es. Naphthalin ist der einfachste Vertreter der polykondensiertenAromaten
(PAK). Man gewinnt es zum Beispiel aus dem Steinkohlenteer oder aus dem Erdöl (griech. naphtha,
Erdpech).
Naphthalin wird mit Luftsauerstoff in Gegenwart des klassischen Oxidationskatalysators Vanadin(V)-oxid oxidiert.

Zunächst ensteht 1,4-Naphthochinon (ein geschätzter Stoff, der zum Beispiel in der Farbenindustrie
eine wichtige Rolle spielt). Durch Decarboxylierung entsteht daraus auf Grund der Hitze von 400 °C, bei der
die Reaktion durchgeführt wird, Phthalsäure. Aber auch die ist nicht stabil, denn sie spaltet beim Erwärmen
zum Eindampfen der Lösungen Wasser ab, wodurch spontan ihr innermolekulares Anhydrid entsteht. Die Ursache
ist die enge Nachbarschaft der beiden Carboxyl-Gruppen.
Als Anhydrid ist die Substanz auf hohem chemischen Potential und deshalb besonders reaktiv. So kann man leicht Ester mit langkettigen und verzweigten Alkoholen herstellen, die vor allem als Weichmacher in der Kunststoffindustrie genutzt werden („Phthalate“).
Phthalsäureanhydrid ist sogar in der Lage, Aromaten wie Phenol elektrophil zu substituieren. Das bekannteste Beispiel ist die Synthese von Phenolphthalein. Dazu muss der Anhydrid-Ring durch Anlagerung von Protonen aktiviert werden.
Weitere Texte zum Phenolphthalein