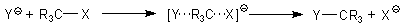
SN 1- und SN 2-Reaktionen:
Nucleophile Substitutionen - kinetisch betrachtet
Experimente:
Versuch: Nucleophile Substitution von Chlorkohlenwasserstoffen mit Hydroxid-Ionen
Aus vielen Anfragen wissen wir: Es gibt für viele Schüler eine eigentlich unnötige
Hürde im Chemieunterricht. Das sind die vertrackten Definitionen für SN 1-
und SN 2-Reaktionen. Was bedeuten die?
Substitutionen sind Reaktionen, bei denen Teile eines Moleküls gegen andere, von außen hinzutretende Teile ausgetauscht werden. Ein Beispiel ist die alkalische Hydrolyse von Methylhalogeniden (-> Versuch):
CH3-Cl + OH- ———> CH3-OH + Cl-
Das N steht für nucleophil. Das heißt übersetzt kernliebend und bedeutet Angriff einer negativ polarisierten Gruppe auf ein positiv polarisiertes C-Atom. Es kann sich auch um Reaktionen zwischen Ionen handeln.
Die Ziffern bedeuten die Molekularität der Reaktion, die die Substitution einleitet.
SN 2-Reaktion
Sind daran zwei Moleküle im Sinne einer simultan ablaufenden Verdrängungsreaktion beteiligt, so heißt es
SN 2-Reaktion; übersetzt: bimolekulare nucleophile
Substitution.
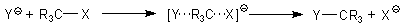
Es gibt hierbei einen Übergangszustand, bei dem die beiden Substituenten (Ein- und Austrittgruppen) am betroffenen C-Atom gebunden sind. Die restlichen drei Substituenten sind am betroffenen C-Atom planar angeordnet. Diese Substitution führt zu einem Umklappen der Substituenten am C-Atom - wie bei einem Regenschirm im Wind... (Walden-Umkehr). Die Reaktion verläuft eindeutig, und man erhält deshalb nur ein Produkt. Ein Beispiel für den SN 2-Typ ist die alkalische Verseifung von Chloroform (Versuch).
SN1-Reaktion
Beginnt die Reaktion dagegen mit dem langsamen Zerfall eines einzigen Moleküls,
worauf dann rasch der Austausch der Substituenten folgt, so handelt es sich um
eine SN 1-Reaktion, also um eine monomolekulare nucleophile Substitution.
Dieser Reaktionstyp setzt Verbindungen voraus, deren restliche Substituenten Elektronen schiebend wirken, also zum Beispiel Alkylreste (+I-Effekt). Unter dem Elektronendruck der Alkylgruppen auf das zentrale C-Atom geben die auszutauschenden Substituenten quasi freiwillig nach... So eine Ausgangssubstanz wäre beispielsweise t-Butylchlorid.
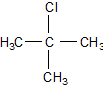
Diese Reaktion läuft in zwei Schritten ab:
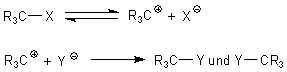
Die erste Teilreaktion (Bildung eines Kations, eines Carbenium-Ions) ist ein chemisches Gleichgewicht. Da das gebildete, planare Carbenium-Ion frei herum schwimmt, kann es auch von beiden Seiten vom neuen Substituenten angegriffen werden. Es bilden sich deshalb zwei spiegelbildliche Isomere. Das sind oftmals Enantiomere, wenn es sich um C-Atome mit vier verschiedenen Substituenten handelt. Im Allgemeinen bildet sich dann ein Racemat.
Was reagiert wie?
Hat man früher gedacht, dass die Reaktionsrichtung nur davon abhängt, inwieweit
sich ein Carbenium-Ion bilden und über eine gewisse Zeit hinweg stabilisieren kann,
so ist man heute schlauer geworden: Eine Voraussage, welche Substanz wie mit
welcher reagiert, ist nicht immer möglich. Welcher von den beiden Reaktionstypen
abläuft, hängt somit von vielen Faktoren ab. (Auch ist die Bildung eines 50:50-Racemats
bei der SN 1-Reaktion nicht immer zu beobachten.) Es bedarf einer
gründlichen kinetischen Analyse, um herauszufinden, welcher der Reaktionsschritte
geschwindigkeitsbestimmend ist. Komplizierend ist weiterhin, dass die kinetischen
Geschwindigkeitsgesetze Reaktionsordnungen ergeben, die durchaus nicht der
Molekularität entsprechen. (Beides müssen wir ja bekanntlich sauber
auseinander halten!)
Aussagen ermöglichen allein die Reaktionsdiagramme
Bei der SN 2-Reaktion erkennen wir das Bild einer
klassischen bimolekularen Reaktion: Die Edukte bilden unter Aufwand einer Aktivierungsenergie einen
aktivierten Übergangszustand, aus dem heraus sich das Produkt bildet, wobei die Aktivierungsenergie
wieder frei wird - zusammen mit der Reaktionsenergie.
|
|
Reaktionsdiagramm der SN 2-Reaktion
Bei der SN 1-Reaktion wird zunächst der Zerfall des
Edukt-Moleküls eingeleitet. Dazu ist eine größere Aktivierungsenergie notwendig. Die Kurve geht aus
dem aktivierten Übergangszustand in das Energie-Minimum des Gleichgewichtszustands, in dem alle drei
Reaktanden-Ionen nebeneinander vorliegen. Anschließend wird unter Aufwand einer weiteren Aktivierungsenergie
der Produkt-Übergangszustand eingenommen, aus dem heraus die Produktbildung erfolgen kann.
Die Reaktion läuft nur deswegen in Richtung auf Produktbildung, weil die Aktivierungsenergie für die
Bildung des Übergangszustands II kleiner ist als die für die Bildung von Übergangszustand I. Im anderen
Fall würde sie aus dem Gleichgewichtszustand auch wieder in Richtung auf die Edukte laufen.
|
|
Reaktionsdiagramm der SN1-Reaktion
Weitere Texte zum Thema „Reaktionskinetik“