Technische Verfahren zur Schwefelherstellung
Experimente:
Modellversuch zum Claus-Prozess
Die technischen Verfahren zur Herstellung von Schwefel aus seinen Verbindungen sind
allesamt auch in der Umwelttechnologie gebräuchlich - zur präventiven und sekundären
Verhinderung von Schwefelemissionen.
1 Symproportionierung von SO2 und H2S
(Claus-Prozess)
Um die Emission von Schwefeldioxid zu vermeiden, werden Brennstoffe vor ihrem
Einsatz durch besondere Verfahren entschwefelt.
Ein Beispiel ist die katalytische Druckentschwefelung, die mit dem
Claus-Prozess gekoppelt wird. Hierbei lässt man auf
die Brennstoffe (vor allem Erdölprodukte wie Diesel- oder Heizöl sowie Kerosin) Wasserstoff
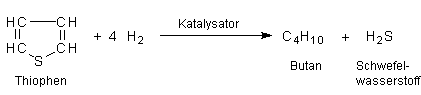
in Gegenwart eines Katalysators einwirken. Es entstehen Schwefelwasserstoff und Kohlenwasserstoffe;
aus dem typischen Erdölbestandteil Thiophen wird so Butan:

Schwefelwasserstoff entsteht dabei in großen Mengen. Ein Drittel davon verbrennt man in geschlossenen Räumen zu Schwefeldioxid.

Dieses leitet man zusammen mit den restlichen zwei Dritteln Schwefelwasserstoff über einen Cobalt-Molybdän- und anschließend über einen Aluminiumoxid-Katalysator. Man kann die Gasmischung auch in Wasser einleiten (siehe Versuch zum Claus-Prozess) oder mit Aktivkohle in Kontakt bringen. Folgende Reaktion läuft ab:

Hiermit wird weltweit ein großer Anteil des Industrieschwefels gewonnen. Schwefelwasserstoff tritt auch in großen Mengen im Erdgas auf, so z. B. mit 15 Vol% in Südfrankreich.
Die diesem technischen Verfahren zugrunde liegenden Vorgänge sind übrigens auch Ursache für die Entstehung der großen Schwefellager vulkanischen Ursprungs. Vulkane emittieren nämlich Schwefelwasserstoff, Schwefeldioxid und Wasserdampf, also eine ideale Mischung für die Schwefelbildung.
2 Reduktion von SO2 durch Erdgas
Beim sog. Wellmann-Lord-Verfahren wird SO2 durch Methan katalytisch
zu Schwefel reduziert. Die Gleichung der Gesamtreaktion ist:
2 SO2 + CH4 ———> 2 S + CO2 + 2 H2O
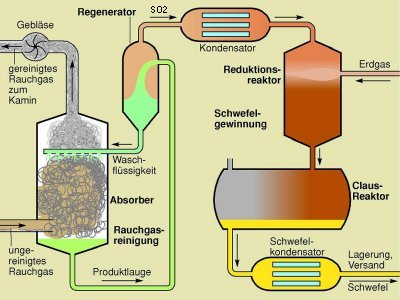
Das Wellmann-Lord-Verfahren als Variante des Claus-Prozesses
(Quelle: Cornelsen)
Die Rauchgase werden in einem Absorber durch eine Waschflüssigkeit aus Natriumsulfitlösung
(Na2SO3) geleitet. Dort reagiert das Schwefeldioxid aus dem Rauchgas mit dem
Natriumsulfit zu Natriumhydrogensulfit.
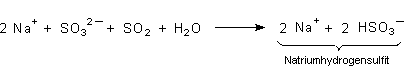
Die Waschlauge, Produktlauge genannt, kommt in den Regenerator. Dort wird sie durch Erwärmung
vom Schwefeldioxid befreit. Die Reaktion verläuft nun in Gegenrichtung. Die zurückbleibende
Natriumsulfitlösung wird anschließend wieder in den Absorber zurückgeführt (Kreislaufverfahren).
Aus dem konzentrierten Schwefeldioxidgas wird in zwei Reaktoren sehr reiner Schwefel gewonnen.
Dabei dient Erdgas (Methan, CH4) als Reduktionsmittel.
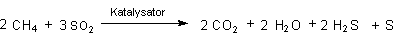
Die zweite Reaktion beschreibt den Claus-Prozess, den wir schon kennen.

Weitere Texte zum Thema „Schwefel“