Dithionit und Indigoküpe
Experimente:
Versuch: Küpenfärbung mit Indigo
Viele in Wasser unlösliche Farbstoffe bringt man auf die Faser, in dem man sie zuvor in eine lösliche und meist mehr oder weniger farblose "Leukoform" überführt. Dies geschieht z. B. durch Reduktion in einer Lösung ("Küpe"). Ein Beispiel ist das Indigo, dessen phenolische Form Indigweiß bzw. das sich im alkalischen Milieu daraus bildende Anion löslich ist. Früher dienten als Reduktionsmittel anaerobe Bakterien.
Auf einer Gastwebseite schildert Georg Stark, wie man früher, als man das Dithionit noch nicht kannte, mit Indigo gefärbt hat. Er nimmt zur Bereitung seiner Küpe wie um 1750 Kalkstein als Alkali und Eisen(II)-sulfat (Eisenvitriol) als Reduktionsmittel ("Vitriolküpe").
Heute nimmt man als Reduktionsmittel zur Bereitung der Küpe technisch hergestelltes
Natriumdithionit (-> Versuch).
Bei dieser Verbindung handelt es sich um eine Schwefelverbindung: Na2S2O4.
Dithionit ist das Salz der Dischwefel(III)-säure H2S2O4.
In der hat der Schwefel die Oxidationszahl +III.
Dithionit wird hergestellt, indem man eine Hydrogensulfit-Lösung reduziert. Formal gilt:
2 SO2 + 2 e- ———> S2O42-
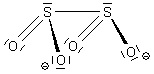
Das Anion hat folgende bemerkenswerte Struktur:

Die Sauerstoffatome stehen auf Deckung. All das führt dazu, dass auch die Bindungslänge zwischen den S-Atomen extrem groß ist. Das Molekül muss einfach rasch zerfallen. Man erkennt, dass darin quasi schon zwei SO2-Moleküle enthalten sind. Wegen der beim Zerfall "übrigbleibenden" Elektronen ist Dithionit ein hervorragendes Reduktionsmittel.
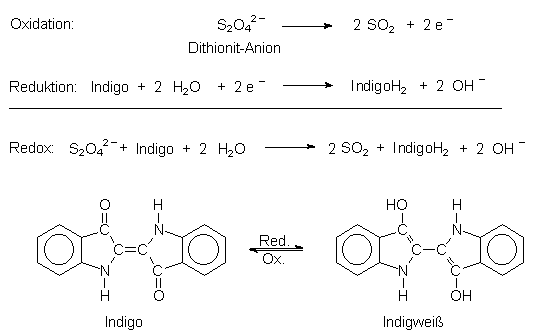
Reaktion zur Bildung von Leukoindigo, dessen Anion und Rückreaktion zu Indigo
Nach dem Bad in der Lösung des Leukoindigos wird die Textilie in der frischen Luft mit Sauerstoff
in Kontakt gebracht ("Verhängen"), wodurch sich der Farbstoff zurückbildet.
Weitere Texte zum Thema „Schwefel“