Prof. Blumes Tipp des Monats Mai 1999 (Tipp-Nr. 23)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Spielerei mit Bleioxiden
Mit Schwermetalloxiden kannst du schön experimentieren. Nehmen wir einmal das Bleidioxid PbO2. Dieses tiefbraune Pulver zeigt, wenn du es richtig behandelst, eine Menge Farben und gleicht darin eigentlich den Verbindungen des Chroms, welches seinen Namen schließlich vom giechischen chroma, Farbe erhielt. Der Name Blei klingt dagegen richtig plump, stammt er doch vom lateinischen plumbum. Wenn du seine Oxide aber richtig behandelst, kannst du rasch das Herz deines Chemielehrers erobern - auch wenn er nicht national gesinnt ist!
Der wissenschaftliche Hintergrund: Es gibt im Wesentlichen drei Bleioxide, die sich durch Sauerstoffgehalt und in ihrer Farbe unterscheiden:
- Blei(II)-oxid PbO (Bleiglätte) gelb
- Blei(II,IV)-oxid Pb3O4 (Mennige) orangerot bis leuchtendrot
- Blei(IV)-dioxid PbO2 schwarzbraun
Die ersten zwei Oxide kannst du leicht aus dem dritten, Bleidioxid, herstellen. Dazu musst du dieses nur vorsichtig erhitzen. Mennige entsteht, wenn du etwa 500 °C einhältst. Bleiglätte bildet sich beim Erhitzen auf noch höhere Temperaturen. Achte dabei darauf, dass die heißen Oxide eine tiefere Farbe aufweisen als die kalten. Man spricht hier von Thermochromie, also "Farbveränderung durch Hitze".
Sicherheitshinweis: Bleioxide sind giftig!
|
Versuch 1: Herstellen von Mennige aus Bleidioxid
|
Es sind etwa 100 ml Sauerstoff entstanden. Wir wollen nachprüfen, ob die Menge
stimmt. Dazu müssen wir zunächst ausrechnen, wie viel Gas bei quantitativem, also
völligem Umsatz zu Mennige zu erwarten ist.
Wenn du nach dem Abkühlen zuviel Gas erhältst, war das Schiffchen nicht trocken
genug oder die Oxide enthielten adsorbiertes Wasser. Der Fehler ist aber gering.
Nun wollen wir die Mennige in Bleiglätte, PbO, überführen. Hierzu müssen wir kräftiger erhitzen.
|
Versuch 2: Herstellen von Bleiglätte aus Mennige
|
Mit den drei Oxiden des Bleis können wir leicht die deutsche Flagge zaubern.
|
Versuch 3: Schwarz-Rot-Gold im Reagenzglas
Ergebnis: Wenn du alles richtig gemacht hast, bilden sich innerhalb der nächsten drei Minuten
beim Abkühlen drei deutlich voneinander getrennte Farbzonen aus: Oben
Schwarz, in der Mitte Rot und unten Gelb. Dein Lehrer wird dich loben. Manche
behaupten sogar, dass die Burschenschaftler, die 1848 die Schwarz-Rot-Gold-Flagge
einbrachten, Chemiestudenten waren...
|
 |
| Public Viewing in Hameln 2006
(Foto: Blume) |
Hier sind noch die Reaktionsgleichungen für den gesamten Versuchsablauf:
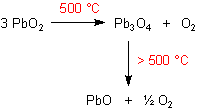
Entsorgung
Die Bleioxide werden zum Schwermetallabfall gegeben.
Rüdiger Blume
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 16. Mai 2011, Dagmar Wiechoczek