Prof. Blumes Tipp des Monats September 2011 (Tipp-Nr. 171)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Pilzgifte: Beispiel Knollenblätterpilze
Es ist wieder Pilzzeit. Und da gilt es aufzupassen: Viele Pilze sehen toll aus, duften gut und sind trotzdem ungenießbar. Sagenhaft ist der dem Steinpilz ähnliche Gallenröhrling, der - wie wir es selbst am letzten Sonntag erlebt haben - ein ganzes Pilzgericht nachhaltig verderben kann.

Bild 1: Bittere Pilzmischung - zufällig vor dem Zubereiten fotografiert.
Neben den leckeren Braunkappen befinden sich darin zwei Gallenröhrlinge, erkennbar an der hellen
Kappe und den rosa Röhren
(Foto: Blume)
Wichtiger aber ist: Viele Pilze sind giftig. Wir kennen bereits den Fliegenblätterpilz,
den wir im Tipp des Monats Nr. 139 vorgestellt haben.
Aber wehe, wenn sich in die Pilzmischung statt eines letztlich ungiftigen Gallenröhrlings ein hochgiftiger Knollenblätterpilz einschleicht!
Wir wollen vor allem die Knollenblätterpilze beleuchten
Im Wesentlichen findet man in unseren Wäldern den Grünen Knollenblätterpilz (Amanita phalloides).
Der ist oft gar nicht grün, sondern weiß - wie der auf dem folgenden Bild.

Bild 2: Grüner Knollenblätterpilz (weiße Variante)
(Foto: Blume)
Diese weiße Abart erinnert gerade ausländische Mitbürger an unbedenkliche Pilze, die sie aus ihrer Heimat kennen.
Sie sammeln diese und essen sie vertrauensvoll - mit schrecklichen Folgen...
Es gibt dazu einen Spruch unter Pilzsammlern:
Man hüte sich im Walde vor allen Pilzen, die weiß sind...
Inzwischen habe ich auch einen wirklich grünen Grünen Knollenblätterpilz gefunden. Klicke hier.
Der Knollenblätterpilz gehört zur Gattung der Wulstlinge (Amanita) und ist deshalb mit dem Fliegenpilz (Amanita muscaria) verwandt. Beide enthalten jedoch stofflich völlig unterschiedliche Giftstoffe: Ist es beim Fliegenpilz das niedermolekulare Alkaloid Muscarin, so finden wir beim Grünen Knollenblätterpilz ungewöhnlich gebaute Peptide, Amatoxine und Phallotoxine genannt. Die kann man entsprechend der Definition von Alkaloiden als stickstoffhaltige Verbindungen mit physiologischer Wirkung natürlich auch zu dieser physiologisch wirksamen Naturstoffklasse zählen.
Die Moleküle dieser Peptide sind bicyclisch aufgebaut, bestehen also aus zwei Ringen. Die Giftmoleküle enthalten entweder 7 Aminosäuren (Heptapeptide wie das Phalloidin) oder 8 Aminosäuren (Octapeptide wie das Amanitin).
Je nach Typ sind die Aminosäurereste unterschiedlich substituiert. Hier ist die Struktur des am einfachsten gebauten Gifts, des Heptapeptids Phalloidins.
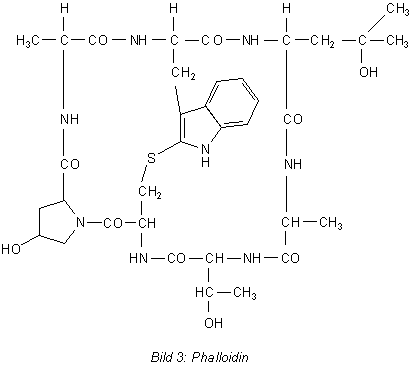
Das scheint eine ziemlich unübersichtliche Formel zu sein! Wenn man jedoch die Namen der Aminosäuren bestimmt,
erhält man die folgende, wesentlich einfachere Formulierung:
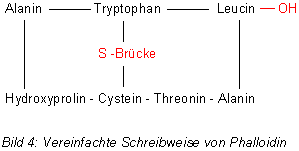
Zum Doppelring müssen wir noch etwas sagen: Dessen Bildung ist die Folge einer ungewöhnlichen Schwefelbrücke,
die von der Aminosäure Cystein ausgeht und zum Indolring des Tryptophans führt.
Diese Peptide sind bemerkenswert stabil. So werden sie beim Kochen nicht zerstört, also nicht „denaturiert“. Bemerkenswert ist auch, dass diese Peptide resistent gegen unsere Magenenzyme sind, also nach dem Verzehr nicht verdaut werden können.
Dem Vernehmen nach sollen übrigens Schweine Knollenblätterpilze ohne Gefahr der Vergiftung fressen können. Das liegt wohl daran, dass sie eine wesentlich stärkere Magensäure haben als wir Menschen, so dass die Ringe hydrolytisch geöffnet werden und so dem Zugriff von Magen- und Darm-Peptidasen ausgesetzt sind.
Kann man mit dem Knollenblätterpilzgift einfache Chemie betreiben?
Man kann, aber in der Schule ist das wohl verboten... Hier ist z. B. ein alter, fast alchimistisch anmutender Nachweis
[2; Seite 764]:
Es sei aber dringendst darauf hingewiesen, dass dieser Versuch nicht geeignet ist, um einen Knollenblätterpilz sicher zu erkennen!
Man findet Knollenblätterpilze am besten in Buchen- sowie in Eichenwäldern oder in Parkanlagen. Hier zeigen wir ein schönes Exemplar von diesem Wochenende:
Klick mich an!
Bild 5: Mit diesem Knollenblätterpilz wurde der folgende Versuch durchgeführt
(Foto: Blume)
|
Versuch: Nachweis von Knollenblätterpilzgiften
Lösungen und Papier nachhaltig vernichten! Gefäße reinigen! |

Bild 6: Versuchsergebnisse zur Knollenblätterpilzuntersuchung.
Links Kontrollversuch ohne Knollenblätterextrakt. Mitte und rechts: Versuch mit Knollenblätterextrakt.
Mitte kurz nach Zugabe der Salzsäure. Rechts nach etwa 15 Minuten
(Fotos: Blume)
Der Versuch beruht auf einer unübersichtlichen Kopplungsreaktion zwischen Indol und Lignin; er erinnert an die
Nachweisreaktionen für Lignin.
Wie wirkt das Knollenblätterpilzgift?
Die LD50-Dosis beträgt bei Mäusen etwa 1 mg/kg Körpergewicht. (Das ist die Dosis, bei der 50 %
einer Mäusegruppe, die das Gift fressen mussten, sterben.) Angaben für Menschen findet man kaum. Aber es reicht bekanntlich
schon ein Stück eines Pilzes aus, um nachhaltig gesundheitliche Schwierigkeiten zu bereiten.
Die Latenzzeit beträgt 6-24 Stunden - wenn man es dann merkt, ist es oft schon zu spät.
Molekularer Wirkort ist die zellinterne Proteinbiosynthese. Das Gift hemmt hochspezifisch die Bildung der mRNa („Boten-RNA“), indem es mit einer RNA-Polymerase einen Komplex bildet, wodurch dieses Enzym gehemmt wird. Dadurch kommt es zur Störung der Ablesemechanismen der DNA und folglich zum raschen Zelltod. Aus diesem Grunde werden besonders solche Organe angegriffen, die eine besonders hohe Syntheserate aufweisen, also Leber und Niere. Leider ist das aber auch der Grund dafür, dass man erst relativ spät merkt, dass man Knollenblätterpilze gegessen hat.
Wie ist das mit dem Gelben Knollenblätterpilz?
Im Walde findet man öfter auch den Gelben Knollenblätterpilz (Amanita citrina).

Bild 7: Gelber Knollenblätterpilz
(Foto: Blume)
Der ist keineswegs so giftig wie sein grüner (bzw. weißer) Bruder. Probieren sollte man ihn aber nicht; schließlich
gilt er immerhin als ungenießbar. Denn er enthält eine Mischung aus niedrigmolekularen, halluzinogenen Alkaloiden, die
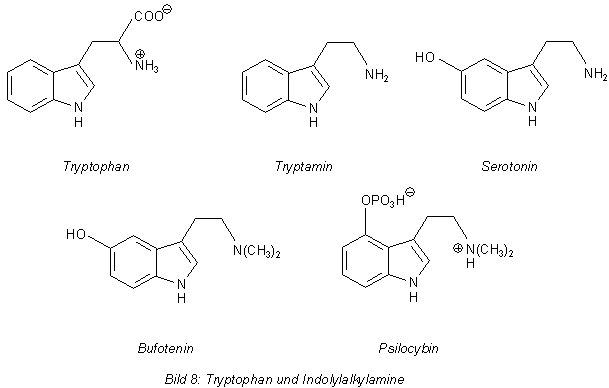
zur Gruppe der Indolyl-alkyl-amine gehören. Beispiele sind Bufotenin und Serotonin.
Die Giftigkeit des Gelben Knollenblätterpilzes ist allerdings kaum merkbar, da seine Giftstoffe nur in geringem Umfang kaum die Blut-Hirn-Schranke passieren. Sie sind immerhin verwandt mit Substanzen wie dem Psilocybin, einem altindianischem Pilz-Rauschgift. Serotonin ist ein Gewebshormon des Gehirns. Alle Indolylalkylamine leiten sich von der Aminosäure Tryptophan ab. Startsubstanz ist deren Decarboxylierungsprodukt Tryptamin.
Was unterscheidet den Grünen Pilz vom Pils?
In der Wirkung letztlich nichts - beide schädigen nachhaltig die Leber…
Rüdiger Blume
Literatur:
[1] H. E. Laux: Der große Kosmos-Pilzführer. Franckh-Kosmos Verlag, Stuttgart 2010.
[2] E. Teuscher und U. Lindequist: Biogene Gifte. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2010.
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 24. November 2012, Dagmar Wiechoczek
