Prof. Blumes Bildungsserver für Chemie
Tipp des Monats Mai 2025 (Tipp-Nr. 330)
Beim Experimentieren den Allgemeinen
Warnhinweis
unbedingt beachten.
An Kerzen länger Freude haben – Teil 2: Wenn Salz das Feuer zähmt
Dennis Dietz
Die Brenndauer von Kerzen kann dadurch verlängert werden, dass sie vorab im Tiefkühlfach gelagert werden. Allerdings sind die Kerzen durch die
Tiefkühllagerung in der Regel optisch weniger ansprechend. Tiefgekühlte Kerzen sind optisch weniger ansprechend
Das wirft die Frage auf, ob es Alternativen zur Tiefkühllagerung gibt, um die Brenndauer von Kerzen zu
verlängern. Im Internet findet man häufig den Tipp, dass die Zugabe von Salz die Brenndauer von Kerzen
erhöhen solle [u.a. 1,2]. Darüber hinaus gibt es sogar Krimiserien, in denen die Brenndauer von Kerzen
angeblich mit Hilfe von Salz verlängert wurde, um einen Mord zu verschleiern [3].
Ob die Brenndauer von Kerzen wirklich mit Salz verlängert werden kann, wird im Rahmen dieses Monatstipps
untersucht. Wiederum andere behaupten, dass durch die Zugabe von Salz die Siedetemperatur des Kerzenwaches erhöht
würde [2]. Dadurch brauche das Kerzenwachs länger zum Sieden, bevor es verbrannt werden kann. Ein
bekannter thermodynamischer Effekt stellt den Hintergrund für die zweite Begründung dar. Wird in einer
reinen Flüssigkeit ein Stoff gelöst, dann nimmt die Unordnung (Entropie) der flüssigen Phase im
Vergleich zum reinen Lösungsmittel zu [4]. Der Dampfdruck, der aus dem Bestreben nach zunehmender
Unordnung (Entropie) im System resultiert, nimmt dadurch ab und die Siedetemperatur steigt [4, S. 210].
Dies wird auch als ebullioskopischer Effekt bezeichnet [4]. Für verdünnte Lösung beträgt die
Siedepunkterhöhung (Ke: ebullioskopische Konstante des Lösungsmittels, mB: Molalität der Lösung,
also die Stoffmenge des
gelösten Stoffs pro Kilogramm Lösungsmittel [4, S. 211]) Die Temperaturdifferenz hängt dabei von der Art des Lösungsmittels ab, nicht aber von der Art des
gelösten Stoffs [4]. Entscheidend für den ebullioskopischen Effekt ist, dass sich der Stoff auch in dem
Lösungsmittel löst.
Im Folgenden wird zunächst einmal experimentell überprüft, ob Kerzen wirklich länger brennen, wenn man
Salz hinzugibt. Versuch: Untersuchung der Brenndauer von Kerzen mit und ohne Salz Im ersten Schritt werden Teelichter des gleichen Herstellers gewogen und jeweils gleich schwere
Teelichter zu Paaren zusammengestellt. Die paarweise zusammengestellten Teelichter werden
zeitgleich entzündet. Nachdem sich eine ausreichende Menge an Kerzenwachs um den Docht herum
sichtbar verflüssigt hat, wird jeweils zu einem der beiden Teelichter eine Spatelspitze
Speisesalz direkt in das flüssige Kerzenwachs gegeben. Es wird die Zeit bestimmt, bis die beiden
Teelichter abgebrannt sind. Das Experiment wird insgesamt drei Mal durchgeführt. Teelichter mit und ohne Salz im Kerzenwachs nach einer Brenndauer von
20 Minuten
Beobachtung: Die Teelichter, zu denen Salz gegeben wurde, brennen deutlich
länger. Gut zu sehen ist, dass sich das Salz nicht im Kerzenwachs löst. Teelichter ohne Salz brennen sichtbar schneller ab.
Die gemessenen Massen der Teelichter (m) vor dem Abbrennen und die jeweiligen Brenndauern (t)
sind in der folgenden Tabelle dargestellt:
Tab. 1: Tabellarische Darstellung der Messwerte aus der experimentellen
Bestimmung des Einflusses von Salz auf die Brenndauer von Teelichtern
Wie der Tabelle 1 eindeutig zu entnehmen ist, ist die Brenndauer von Teelichtern, zu denen Salz gegeben
wurde, deutlich höher, als von Teelichtern, zu denen kein Salz gegeben wurde. Doch was ist nun der Grund für die längere Brenndauer? Der ebullioskopische Effekt kann es nicht sein,
da sich das Natriumchlorid nicht im Kerzenwachs löst. Der ebullioskopische Effekt tritt aber nur in
Systemen auf, in denen sich ein nicht-flüchtiger Stoff in einem Lösungsmittel löst. Dementsprechend muss
die erhöhte Brenndauer auf einen oder mehrere andere Effekte zurückzuführen sein. Eine potenzielle
Ursache für eine gleichmäßigere und ruhigere Flamme und damit für eine längere Brenndauer stellt ein
durch das Salz verändertes Dochtverhalten dar.

(Foto: Dietz)
Theoretische Vorüberlegungen zum Salz in der Kerze
Warum sollte die Zugabe von Salz die Brenndauer von Kerzen überhaupt erhöhen können? Hierzu findet
man im Internet unterschiedliche Begründungen. Die einen behaupten, dass sich das Salz an den Docht
anlagert. Die Kerzen sollen dadurch insgesamt sparsamer brennen, sodass die Brenndauer erhöht würde [1].
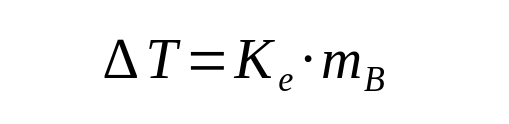
Zur experimentellen Überprüfung: Brennen Kerzen mit Salz wirklich
länger?
Auch in diesem Modellversuch war es wichtig, das Prinzip der Variablenkontrolle zu beachten. Es
werden also wieder Kerzen des gleichen Herstellers genutzt, um eine identische
Kerzenwachszusammensetzung und eine gleiche geometrische Form der Kerzen zu garantieren.
Um die Forschungsfrage beantworten zu können, also um eine potenziell unterschiedliche Brenndauer
zweifelsfrei auf die Zugabe von Salz zurückführen zu können, werden die Teelichter vor dem Abbrennen
gewogen und gleich schwere Kerzenlichter zu Paaren zusammengestellt. Nachdem sich ausreichend
Kerzenwachs verflüssigt hat, wird zu jeweils einer Kerze eine Spatelspitze handelsübliches Speisesalz
hinzugegeben. Die Brenndauer der Teelichter wird mit einer Stoppuhr gemessen.

(Foto: Dietz)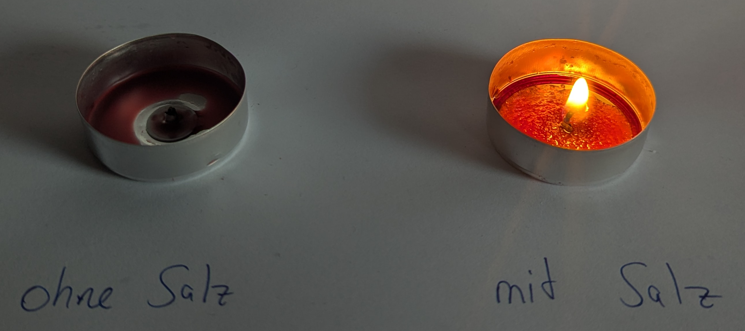
(Foto: Dietz)
Zugabe von Salz
Masse Teelicht m vor dem Abbrennen in g
Brenndauer t in min
Kerzenpaar 1
nein
11,6
230
Kerzenpaar 1
ja
11,6
253
Kerzenpaar 2
nein
11,5
226
Kerzenpaar 2
ja
11,5
245
Kerzenpaar 3
nein
11,7
241
Kerzenpaar 3
ja
11,7
266
Fazit
Das hier vorgestellte Experiment bietet die Möglichkeit, im Themenfeld „Thermodynamik“ wichtige
Kompetenzen aus dem Bereich der Erkenntnisgewinnung zu fördern und dabei quasi en passant den kritischen
Umgang mit Behauptungen aus dem Internet zu üben.
Literatur:
[1] https://www.focus.de/wissen/wer-eine-prise-salz-ueber-seine-kerzen-gibt-hat-schon-bald-freude-daran_ba1ca595-eb6d-43bb-a80c-0719375e9a4a.html,
letzter Zugriff: 11.04.2025
[2] https://www.chip.de/nachrichten/haushalt-garten,135994/so-brennen-sie-laenger-das-sollten-sie-in-ihre-teelichter-streuen_5f006a96-0cbd-421a-9926-8d65ddf41368.html,
letzter Zugriff: 11.04.2025
[3] https://tv.apple.com/ch/episode/im-schein-der-kerze/umc.cmc.48ndxolyzclzodonno2jxpfpj,
letzter Zugriff: 11.04.2025
[4] Atkins, P. W. (2004). Physikalische Chemie. 3. korrigierte Auflage, Wiley-VCH.
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 28. April 2025, Fritz Franzke