
Der Stechapfel – Alkaloide im häuslichen Garten

Bild 1: Stechapfelblüten und unreife Frucht (Foto: Blume)
In vielen naturbelassenen Gärten (so auch in unserem) stehen prächtig-grüne Pflanzen. Ihr
wissenschaftlicher Name ist Datura. Man erkennt sie nicht nur an den trompetenartigen
weißen Blüten, sondern auch an den von vornherein unangenehm stacheligen Früchten, die ihr auch
den Namen gegeben haben: Stechapfel.

Bild 2: Früchte des Stechapfels (Foto: Blume)
Alle Pflanzenteile sind giftig. Hierin ähnelt die Datura der Tollkirsche,
ebenfalls eine Verwandte aus der Gruppe der Nachtschattengewächse und Mitbewohnerin unseres Gartens.
Die Verwandtschaft gilt nicht nur für die Blütenform, sondern auch sogar für die Gifte: Beide Gattungen
enthalten Hyoscyamin und Scopolamin, die zur Stoffgruppe der
Alkaloide gehören. Genau genommen sind es Tropanalkaloide.
Die Struktur von Tropan kann man auf verschiedene Weise zeichnen. Aufschluss über die tatsächlichen Bindungsverhältnisse gibt nur die Konformationsformel.
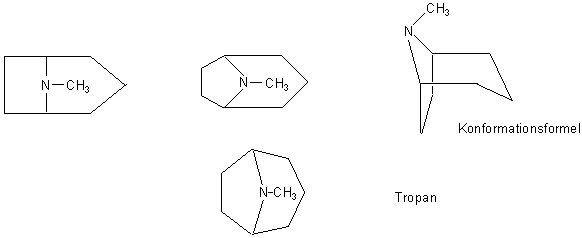
Bild 3: Verschiedene Darstellungen des Tropans (vergleiche auch Bild 4)
Es wird deutlich, dass es sich beim Tropan um ein Doppelringsystem handelt. Man kann aber auch sagen,
dass der zugrunde liegende Ring, über den eine Stickstoffbrücke ragt, aus sieben C-Atomen besteht.
Nun zu den Alkaloiden des Stechapfels
Hier ist zunächst das Hyoscyamin. Es ist benannt nach dem Bilsenkraut (Hyoscyamus
niger) – ebenfalls ein Nachtschattengewächs.
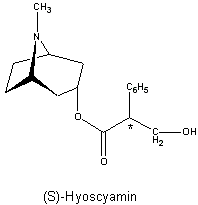
Bild 4
Das sieht eigentlich genauso wie die Struktur des Atropins aus! Man muss
aber wissen, dass Hyoscyamin optisch aktiv ist. Denn das mit einem Sternchen gekennzeichnete C-Atom trägt vier
verschiedene Substituenten. Deshalb nennt man es auch asymmetrisches C-Atom.
Das linksdrehende Enantiomere ist das natürlich auftretende (S)- bzw. (-)-Hyoscyamin. Beim Aufarbeiten in saurem Milieu kann es an diesem C-Atom zu einer Bindungsinversion kommen; dabei bildet sich das (R, S)-Racemat – und diese Mischung nennt man - Atropin! Atropin besteht also genau genommen aus zwei Substanzen, aus (R)- und (S)-Hyoscyamin. Diese verhalten sich zueinander wie Bild und Spiegelbild und sind somit Enantiomere.
Scopolamin ist das Epoxid des (-)-Hyoscyamins.
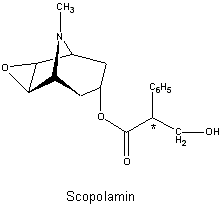
Bild 5
Ganz geringe Dosen dieser Gifte sollen bewusstseinserweiternd wirken. Die Gefahr, sich selbst zu vergiften,
ist allerdings recht hoch. Die letale Körperdosis von Scopolamin beträgt für Erwachsene 50 mg; aber
schon bereits wesentlich niedrigere Mengen können den Tod durch Atemlähmung herbeiführen. Ein Grund für
Vergiftungsfälle ist, dass der Alkaloid-Gehalt der Pflanzen stark variieren kann. Aber das ist halt das Risiko
der Schamanen und Junkies, die sich dafür halten…
In diesem Zusammenhang ist auch interessant, dass die Alkaloide des Stechapfels und der Tollkirsche chemisch verwandt sind mit dem Cocain. Der Cocastrauch gehört aber nicht zu den Nachtschattengewächsen.
Nicht alle Tiere scheinen das Gift fürchten zu müssen. Unsere Stechapfelpflanzen werden kräftig von Raupen oder Schnecken heimgesucht. Sie sehen deshalb ganz zerrupft und zerfressen aus.
Last but not least
Der Stechapfel ist nur entfernt verwandt mit der Engelstrompete (Brugmansia) - die man fälschlicherweise
ebenfalls als Datura bezeichnet. Sie ist aber trotzdem genauso giftig wie der Stechapfel…
Bleibt noch die Frage nach der Herkunft der Bezeichnung „Nachtschattengewächse“. Einige Leute beziehen das auf die psychedelische Wirkung der Alkaloide: Die machten in der Nacht schwere Träume. Das Wort Nachtschatten stand aber früher im Ganzen für Dunkelheit. Deshalb sagen die Sprachwissenschaftler (Etymologen), dass die Herkunft der Bezeichnung im Dunkeln liegt. Vielleicht bezieht sich der Name aber nur darauf, dass einige dieser Gewächse wie der Stechapfel (aber auch die Engelstrompete) in der Nacht blühen und duften, um so ihre Bestäuber, die Nachtfalter mit den langen Saugrüsseln, anzulocken.
Weitere Texte zum Thema „Ammoniak, Amine und Säure-Amide“