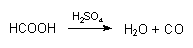
Kohlenstoffmonooxid
Experimente:
Versuch: Herstellung von CO
Versuch: Brennbarkeit von CO
Versuch: Reduktionswirkung von CO
Versuch: CO reduziert Eisenoxid
Versuch: Nachweis von Kohlenstoffmonooxid im Zigarettenrauch
Versuch: Nachweis von CO2 und CO in Auspuffgasen
Sicherheitshinweis
CO ist geruchlos, giftig und bildet mit Luft und Sauerstoff hochexplosive
Gemische !
Bei unvollständiger Verbrennung kohlenstoffhaltiger Materialien entsteht Kohlenstoffmonooxid, kurz Kohlenmonoxid oder CO. Es findet sich deshalb in fast allen Abgasen wie Heizungsrauch, Auspuffgasen von Kraftfahrzeugen mit Ottomotor und auch im Zigarettenrauch. (Die leicht betäubende Wirkung von Zigarettenrauch rührt vom Kohlenmonoxid her.) In der Atmosphäre bildet es sich bei der atmosphärischen Oxidation von Kohlenwasserstoffen (vor allem Methan), Aldehyden und Lösemitteln.
Im Labor stellt man es durch Zersetzung von Ameisensäure oder deren Salzen, den Formiaten, mit konzentrierter Schwefelsäure her (-> Versuch).
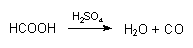
Dieser Prozess ist autokatalytisch und kann auch ohne Schwefelsäure spontan ablaufen. Daher neigt Ameisensäure zu explosionsartiger Selbstzersetzung. Vor Licht und Wärme schützen!
Das Gas brennt gut und bildet mit Luft knallgasartige Gemische (-> Versuch). Früher war es Bestandteil vom Stadtgas. CO ist also ein Reduktionsmittel; so reagiert es mit Silber-Ionen (-> Versuch):
2 Ag+ + CO + H2O ———> 2 Ag + CO2 + 2 H+
Zum Verschieben der Lage des Redox-Gleichgewichts verwendet man eine
ammoniakalische Lösung. Auf dieser Reaktion beruht ein Nachweis des Gases (->
Versuch und Versuch).
In der Eisenherstellung dient
CO als das eigentliche Reduktionsmittel (-> Versuch),
das ständig in der Hitze des Hochofens aus Kohle nachgebildet wird:
Fe2O3 + 3 CO ———> 2 Fe + 3 CO2
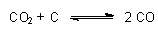
Das letztere Gleichgewicht heißt Boudouard-Gleichgewicht. Es spielt eine wichtige Rolle bei der Funktion des Dieselmotors. (In einer anderen Webseite wird das Gleichgewicht unter Anwendung des Prinzips von Le Chatelier genauer analysiert.)
CO ist sehr giftig und besonders tückisch, da es geruchlos ist. So sind viele Unglücke mit nicht gut belüfteten Ofen darauf zurückzuführen. Ein prominentes Opfer einer CO-Vergiftung aufgrund eines nicht ziehenden Kamins wurde vor hundert Jahren übrigens Emile Zola (1840-1902), der große französische Romancier, bekannt geworden auch als Mahner in der Dreyfus-Affäre ("J'accuse!"). Man meint, dass er ermordet worden ist, indem sein Kamin manipuliert worden ist. Hierzu eine Zeitungsmeldung aus diesen kalten Tagen:
| Castellón/Spanien Ein defekter Gasofen hat den Vergiftungstod
von 18 Gästen einer Geburtstagsparty verursacht. Sie starben sehr wahrscheinlich an Kohlenmonoxid. Die Herberge hatte zwar eine Zentralheizung; diese war aber ausgefallen, so dass die Gäste wegen der Kälte tragbare Gasheizkörper eingesetzt hätten. |
Ob der Ofen wirklich defekt war? Es war wohl eher der Luftmangel, der zur CO-Bildung führte!
Ein untrügliches Zeichen für CO-Vergiftung ist, wenn dir bei offener Heizung (Ofen,
Gasherd, Kamin...) plötzlich der Kopf zu schmerzen beginnt. Dann kann CO im Spiel
sein. In diesem Fall sofort gut lüften und in frischer Luft gut durchatmen. Denn die
Giftwirkung beruht auf Komplexbildung mit Hämoglobin, wobei CO die Bindungsstelle
für den Sauerstoff besetzt. Der Komplex ist 325 Mal stabiler als mit O2. Man rettet
mit CO vergiftete Menschen, indem man sie unter ein Sauerstoffzelt legt. Dies ist eine
weitere Anwendung des Le Chatelierschen Prinzips: Verschieben eines chemischen
Gleichgewichts, hier durch Konzentrationsänderung eines beteiligten Stoffes.
Die Bildung von CO findet typischerweise auch bei Zimmerbränden statt. Das ist ein
Grund dafür, dass du nicht versuchen solltest, einen solchen Brand selbst zu löschen,
ohne die Feuerwehr zu benachrichtigen. Plötzlich fällst du um, und es heißt dann
lapidar: Starb an Rauchvergiftung - statt sich in Sicherheit zu bringen.
Einige Zahlen (Vol-%) zum Vorkommen von Kohlenstoffmonooxid:
| Ottomotor: | Leerlauf | 3-10 |
| Volllast | 1 | |
| Dieselmotor: | Leerlauf | 1 |
| Volllast | 0,1 |
Kohlenmonoxid ist nicht nur giftig, sondern es spielt auch als Quellgas bei der bodennahen
Ozonbildung eine indirekte, aber sehr bedeutende Rolle. Deshalb
darf CO nicht in den Abgasen enthalten sein.
Als Primärmaßnahmen zur Verhinderung der Emission von Kohlenmonoxid gelten
die Regelung von Luftzufuhr und Verbrennungstemperatur, wodurch die CO-Bildung eingeschränkt
werden kann.
Die wichtigste Sekundärmaßnahme zur nachträglichen Entfernung von Kohlenmonoxid
aus Abgasen ist die katalysierte Nachverbrennung, bei der
z. B. Stickoxide Kohlenmonoxid zu Kohlendioxid oxidieren:
2 NO2 + 4 CO ———> N2 + 4 CO2
Als Oxidationsmittel dient auch Sauerstoff.
Welche Bedeutung ein Schornstein für die Ofenfunktion hat, beschreiben wir auf einer besonderen Webseite.
Weitere Texte zum Thema „Auto“