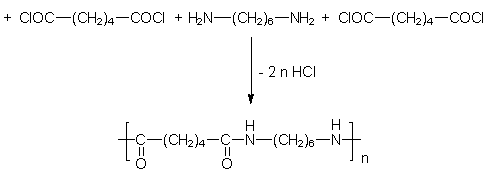
Beispiele f³r die Verfahren zur Herstellung von klassischen Kunststoffen
Experimente:
Versuch: Ein Tischtennisball brennt
Versuch: Herstellung von Nitrocellulose
Versuch: Herstellung von Nylon
Versuch: Herstellung von Phenolharzen
Versuch: Herstellung eines Polyurethans
Versuch: Herstellung eines Polyesters
Versuch: Herstellung von Polystyrol
Versuch: Herstellung von Cellophan
Hinweis: Einige der Kunststoffbezeichnungen sind «-gesch³tzte Namen. Dass nicht extra darauf
hingewiesen wird, berechtigt nicht dazu, den Namen verwenden zu d³rfen.
Celluloseester: Nitrocellulose und Celluloseacetat
Diese Celluloseester werden hergestellt, indem man Cellulose mit Sõuren behandelt.
Im ersten Fall setzt man Salpetersõure/-Schwefelsõure-Gemische ein (->
Versuch), im anderen Essigsõureanhydrid (->
Versuch). Nitrocellulose ist auch unter dem Namen
Celluloid bekannt. Gef³rchtet ist seine leichte Brennbarkeit,
die man an den Tischtennisbõllen demonstrieren kann (->
Versuch). (Nitrocellulose findet als
initiierender Sprengstoff z. B. im Airbag Verwendung.)
Celluloseacetat oder Acetylcellulose ist als Cellitfilm
Grundstoff f³r Sicherheitsfilme. Aber auch Zigarettenfilter bestehen daraus.
Polyester
Es gibt verschiedene M÷glichkeiten, Polyester herzustellen. Im Allgemeinen wõhlt
man eine reaktive Sõurekomponente wie ein Sõuredichlorid oder ein Sõureanhydrid
wie das der o-Phthalsõure aus (-> Versuch).
Polyurethane
Diese meistens schaumig hergestellten Kunststoffe kennt man als Dichtungsmasse. Sie gewinnt
man durch Einwirkung von Diisocyanaten auf binõre Alkohole (->
Versuch). Im Allgemeinen gibt man einen
Katalysator wie Triethyldiamin (DABCO) zu. Zum Schõumen ist der Zusatz von etwas
Wasser n÷tig, da sich dann etwas Diisocyanat unter CO2-Bildung zersetzt.
Polyamid Nylon
Ausgangsstoffe f³r Nylon sind Adipinsõuredichlorid und Hexamethylendiamin (->
Versuch).
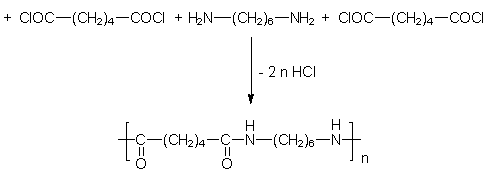
Ersteres gewinnt man aus Cyclohexanol, das reduktiv aus Phenol gebildet wird. Ausgangsstoff f³r die andere Komponente sind Butadien und Blausõure. Die Bausteine werden auch aus Hemicellulosen, also Nachwachsenden Rohstoffen gewonnen. Diese fallen bei der Celluloseherstellung aus Holz als Nebenprodukte an.
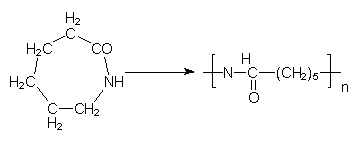
Polyamid Perlon
Perlon gewinnt man aus dem cyclischen e-Caprolactam, dessen Edukt
ebenfalls Phenol ist. Der Kunststoff bildet sich unter katalytischer Einwirkung von Wasser in
einer ring÷ffnenden Kettenreaktion:
Formaldehydharze
Setzt man Formaldehyd katalytisch mit Phenolen oder Harnstoff um, bilden sich Duroplaste
(-> Versuch):
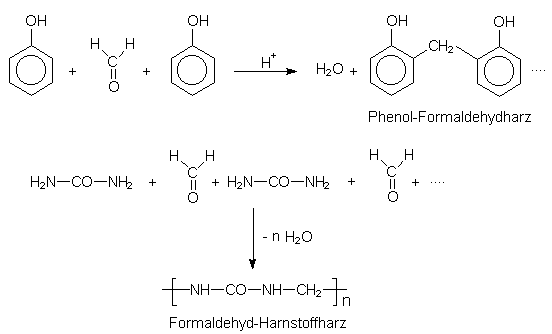
Typisch f³r Formaldehydharze ist, dass sie noch lange Zeit Formaldehyd ausdunsten. Beim Erwõrmen emittieren diese Harze auch Phenol oder fischartig riechende Amine (typischer Geruch von ³berhitzten Lampenfassungen).
Polyethylen
Ethylen ist ein Gas, das in gro▀en Mengen bei der Erd÷lverarbeitung durch den
Crackprozess, bei dem langkettige Molek³le zu kleineren umgewandelt werden,
freigesetzt wird. Fr³her fackelte man die Crackgase ab. Heute hat man daf³r
Verwendung gefunden. Durch Zusatz eines Radikalbildners und unter hohem Druck
polymerisiert es zu PE.
Man unterscheidet entsprechend der Reaktionsbedingungen Hochdruck-
und Niederdruckethylen. Ersteres ist fester und schwerer.
Polypropylen
Polypropylen ist ebenfalls ein Abfallprodukt bei der Erd÷lraffination. Die
Polymerisationsprodukte sind kaum von PE zu unterscheiden und werden ebenfalls als
Hostalentypen klassifiziert. Durch Zusatz bestimmter anorganischer Katalysatoren
(Ziegler-Natta) lassen sich Kettenlõnge und sterischer Aufbau und die
Eigenschaften variieren.
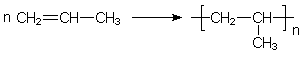
Teflon
Das Monomere von Teflon ist Tetrafluorethylen. Es wird wie Ethen polymerisiert:
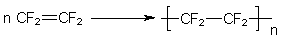
Teflon ist ein hitzestabiles und wasserabweisendes Polymer, das allerdings beim Verbrennen toxische Fluorverbindungen emittiert. Es ist feinstgewebt Bestandteil von Gorextextilien. Diese lassen sich so fein verspinnen, dass ihre Oberflõchenspannung den Durchtritt von Wasser verhindert, den von Wasserdampf dagegen erlaubt (Verwendung zur Herstellung von regenabweisenden Textilien).
Polyacrylate wie z. B. Polymethacrylsõuremethylester (PMMA)
Polyacrylate sind polymere Ester der Acrylsõure. Das Monomere von PMMA, Plexi- oder
Acrylglas, ist Methacrylsõuremethylester. Die Polymerisationsreaktion ist:
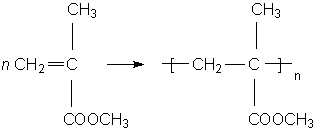
Im Auto findet man PMMA vor allem als Material von R³cklichtabdeckungen. Aus Polyacrylaten bestehen besonders viele Chemiefasern. Auch in Adhõsionsklebern spielen sie eine zentrale Rolle.
Polyacrylnitril
Bei der Addition von Blausõure HCN an Ethin bildet sich Acrylnitril:
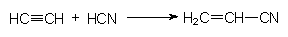
Acrylnitril ist auch als Sekundenkleber bekannt. Bei dessen Verfestigung lõuft folgende Reaktion ab:
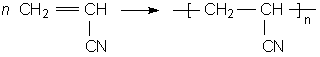
Polystyrol
Das Monomere von Polystyrol ist Styrol (Vinylbenzol). Die Polymerisationsreaktion ist:
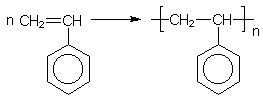
Die Reaktion wird durch Peroxide eingeleitet (-> Versuch).
Polyvinylchlorid
Das Monomere von Polyvinylchlorid PVC ist Vinylchlorid:
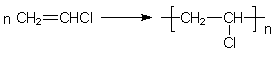
Dieser Kunststoff hat auch im Auto ein weites Anwendungsspektrum gefunden. So werden beispielsweise die Ummantelungen von Kupferkabeln aus diesem Material gefertigt. Sein Chloranteil betrõgt ca. 56 Masse%.
Polybutadien
Die Polymerisation von Butadien erfolgt nach õhnlichen Mechanismen wie die von PE
und PP. Ausl÷ser der radikalischen Reaktion kann metallisches Natrium sein (daher der
Name Buna).
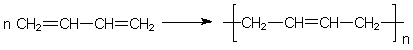
Bei der Polymerisation bleibt wie auch im Naturkautschuk eine Doppelbindung erhalten. Deshalb kann man Polybutadien wie Kautschuk vulkanisieren. Es dient als Ausgangsstoff f³r Kunstgummi und findet in der Autoreifen- sowie in der Dichtungsherstellung eine breite Verwendung.
Polyether
Diese Kunststoffe werden u. a. durch Polymerisation von Epoxiden (Oxiranen) wie Ethylenoxid oder Propylenoxid hergestellt.
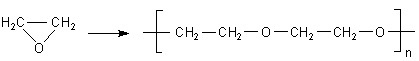
Epoxide verhalten sich letztlich wie Alkene, also wie Kohlenwasserstoffe mit Doppelbindung. Ursache ist die gespannte Bindung in diesem heterozyklischen Oxiran-System.
Zur Herstellung von Kunststoffen, die unter Verwendung von
Nachwachsenden Rohstoffen hergestellt werden, gibt es die Webseiten
Kunststoffe - Grundlagen und Definitionen
und Kunststoffe aus Nachwachsenden
Rohstoffen.
Weitere Texte zum Thema äKunststoffeō
Weitere Texte zum Thema äAutoō