 |
 |
 |
 |
| Kurze Fragen - Kurze Antworten
Aus dem E-Mail-Korb von Professor Blume |
361
F: Zu folgendem hätte ich zwei Fragen (1.): Wie kann man selbst
Rubine bzw. Saphire herstellen? Einige Laborgerätschaften stehen mir zur Verfügung, Al2O3
und CrO2 zu bekommen dürfte auch nicht das Problem sein, nur an der Umsetzung bin ich bisher
gescheitert. Der entstehende Kristall muss nicht zwingend absolut rein und auch nicht sonderlich groß sein.
Grund: Nicht Geldgier. Ich habe mir vorgenommen, einer besonderen Person in meinem Leben einen Anhänger
aus Silber, das ich ebenfalls selbst hergestellt habe, und einem Edelstein zu schenken.
(2.) Wie verhindert man das beim Schmelzen bzw. Abkühlen von Silber auftretende "Spratzen".
A: Eine nette Idee! Rubine zu synthetisieren erfordert vor
allem hohe Temperaturen zum Sintern und Schmelzen der Tonerde. Die erreichen Sie mit einem Knallgasbrenner,
am besten in der Ausführung als Spiegelbrenner. Man lässt (wie auch immer das gemacht wird) die
Reaktionsmischung durch diese Flamme rieseln. Technisch sicherlich nicht einfach... Zum Spratzen:
Befragen Sie dazu am besten einen Goldschmied.
362
F: Ich habe eine kniflige Hausaufgabe im Chemie-Profilkurs aufgekriegt!
und zwar die Anwendungsgebiete der Titration (Fällungs- , Säure-Base- und Redoxtitration) herauszukriegen!
Doch leider bin ich nirgens fündig geworden. Nun bin ich auf ihre tolle Homepage gekommen doch auch hier
habe ich keine Antwort auf meine Frgae gefunden...könnten Sie mir da bitte weiterhelfen???
A: Die Frage ist von deinem Lehrer so allgemein gefasst, dass
man auch fragen könnte: Wo kannst du mit einem Auto überall hin fahren? Gehe auf die Startseite meiner
Homepage und -> Server-Suchmaschine. Gib das Stichwort "Titration" als Suchbegriff ein. Dann hast du mehr
als genügend Beispiele!
363
F: Wieso verdampfen die Terpene ebenfalls bei der Destillation
(keine Wasserdampfdestillation), obwohl die Temperatur bei 100 °C bleibt und die Siedetemp von Terpenen
höher liegt?
Wieso wird bei dem Terpen Limonen von einer Aldehyd-Gruppe gesprochen? (Und
wo und wie bildet sie sich?)
Wie können Terpene (ebenfalls speziell Limonen (alternativ Terpentin)) Lacke lösen?
A: 1 Jede Flüssigkeit - auch Wasser - verdunstet, bevor sie
den Siedepunkt erreicht hat. Siedepunkt heißt: Deutliche Bildung von Dampfblasen, da der Dampfdruck
gleich dem Luftdruck ist.
2 Das ist mir neu. Wenn allerdings der cyclische Kohlenwasserstoff Limonen oxidativ aufgespalten wird,
entstehen Aldehyde: Citral B und Citronellal.
3 Aufgrund ihrer kugeligen Struktur können sie sich zwischen die Lackmoleküle schieben und van der
Waals-Bindungen aufbauen.
Schauen Sie in unsere Webseiten zur Chemie der Zitrone.
364
F: Bezüglich des Versuchs "Nachweis von Stärke in Lebensmitteln"
möchte ich einen kleinen Korrekturvorschlag machen. Sie schreiben, dass sich Iod-Atome in die Stärkemoleküle
einlagern. Elementares Iod kommt als Element-Moleküle vor. Müsste es daher in der Auswertung nicht heissen:
"Gelöste Stärke ergibt mit verdünnter Iod-Kaliumiodid-Lösung eine Blaufärbung, da sich Iod-Moleküle in die
Stärkemoleküle einlagern."?
A: Ja und nein. Es ist noch komplizierter: Es lagern sich weder
Iod-Atome noch -Moleküle oder gar lange Iod-Ketten (wie in vielen Schulbüchern zu lesen steht), sondern
Iod-Iodid-Komplexe wie [I5]- ein! Denken Sie daran, dass in der Lugolschen
Lösung vorrangig diese Komplexe vorliegen. Aber man kann in einer Arbeit, die sich auch an Schüler und Laien
wendet, nicht alle Feinheiten bringen/berücksichtigen.
365
F: Dank SPIEGEL bin ich auf Ihre Seite gekommen. Eine tolle Idee,
Chemie populär zu machen. Leider habe ich zu dem aktuellen Stichwort ACRYLAMID keinen Eintrag gefunden.
A: Sie haben recht, dass dies Thema fehlt. Die Leute interessiert
bei Acrylamid fast immer nur, wo ist es drin und wie viel davon. Das steht sowieso schon in den Zeitungen.
Für Sie speziell: Acrylamid bildet sich beim Erhitzen von Biomasse aus der Aminosäure Asparagin. Zwischen
den beiden besteht nämlich eine starke Ähnlichkeit.
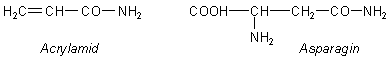
Solche Abbaureaktionen sind unter dem Begriff Maillard-Reaktionen bekannt. Allerdings reicht die Temperatur nicht aus, um Asparagin allein zu zersetzen. Man weiß, dass Stärke bzw. Glucose daran beteiligt sind. Es bilden sich komplizierte zyklische Zwischenverbindungen zwischen den Kohlenhydraten und dem Asparagin aus, aus denen sich Acrylamid auch bei niederen Temperaturen bilden kann.