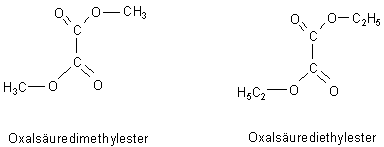
Derivate der Oxalsäure
Oxalsäure ist eine organisch-chemische Dicarbonsäure, von der es eine Reihe Derivate gibt.
Ester der Oxalsäure
Oxalsäure löst sich leicht in Ethanol oder Methanol. Der Zusatz eines sauren Katalysators ist
für die Estersynthese nicht notwendig. Denn die Konzentration
an freien Protonen der Oxalsäure ist auch im Alkohol so hoch, dass die Estersynthese schon beim
Herstellen der Lösungen einsetzt. Hierzu muss man bedenken, dass Alkohole in Gegenwart von Säuren
durchaus als Brönstedbasen wirken.
Der Dimethylester ist ein Festkörper (Schmelzpunkt 54 °C). Seine relativ kugeligen Moleküle können nämlich leicht Kristalle bilden.
Der Diethylester ist ein durchaus gebräuchliches Lösemittel. Der Siedepunkt dieser öligen Flüssigkeit liegt bei 185 °C.
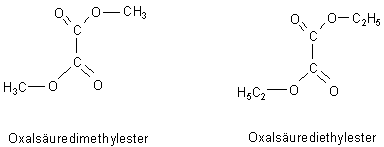
Oxalsäurederivate in der Biochemie
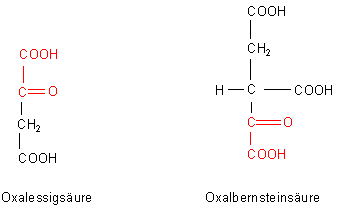
Aber gerade auch in der Biochemie begegnet einem der Name immer wieder. So findet man im
Citronensäurezyklus eine Oxalessigsäure
(als Oxalacetat) und eine Oxalbernsteinsäure (als Oxalsuccinat). Man muss sich
diese Verbindungen so vorstellen, als wäre ein Oxalsäurerest an die Essigsäure bzw. Bernsteinsäure
gebunden.
Aus diesen beiden Säuren (bzw. ihren Anionen) entsteht auf biochemischem Wege Oxalsäure.
Gerade bei der Oxalessigsäure sollte man noch etwas zur Herkunft des Namens sagen. Denn der ist mehr als doppelt gemoppelt! Klicke hier.
Weitere Texte zum Thema "Oxalsäure"