Saure Sulfate im Haushalt
Experimente:
Versuch: Die Rolle von Hydrogensulfat in manchen sauren WC-Reinigern
Jeder kennt sie, die Haushaltsreiniger. Darunter sind einige Produkte, die so gefährlich
sind, dass Chemiker und ihre Mitarbeiter diese nur mit Sonderausstattung händeln dürften: Schutzbrille
oder sogar Gesichtsschutzschirm, alkalien- oder säurefeste Schutzhandschuhe und Schutzkleidung.
Sagenhaft ist das alkalische Rohrfrei®, das aber nur dann sein volles Gefahrenpotential entfalten kann, wenn man sich nicht an die Vorschriften hält und vielleicht sogar damit Schülerscherzchen treibt, also damit "herumdamelt". Zu diesem Thema haben wir einen Tipp des Monats.
Hier geht es vor allem um die sauren WC-Reiniger. Die waren früher in jedem Haushalt zu finden, liegen aber heute immer noch in vielen Waschküchen oder in Opas Schuppen herum. Sie enthalten saure Schwefelsäuresalze, vor allem Natrium- oder Kaliumhydrogensulfat. Die Formeln sind NaHSO4 oder KHSO4. Unmissverständlich warnen Gefahrstoffaufkleber, dass es sich hierbei um ätzende Chemikalien handelt. Sie sollen vor allem Kalkstein lösen.
Sie benehmen sich als saure Salze in Lösung wie eine Säure.
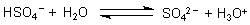
Genau genommen handelt es sich um eine schwache Säure, da ihre Dissoziation nach den Gesetzen des chemischen Gleichgewichts erfolgt. Ihr pKa-Wert liegt jedoch bei 1,9. Damit ist die zweite Stufe der Schwefelsäure saurer als die Ameisensäure! Das reicht aus, um eine Kalksteinprobe aufgrund des freigesetzten CO2 zum Sprudeln zu bringen (-> Versuch).
Diese sauren WC-Reiniger waren auch eine der Ursachen für das Domestosproblem.
Nicht jeder saure WC-Reiniger enthält Hydrogensulfat!
Das ist der Nachteil solcher alltagsbezogener Versuchsvorschläge, die mehr und mehr auftauchen ("Chemie
im Kontext" oder "Chemie im Supermarkt"): Die Produktzusammensetzung kann sich entsprechend der Anforderung
des Marktes oder auch unter dem Druck von gesetzlichen Vorschriften rasch ändern!
Moderne WC-Reiniger wie Sagrotan® sind völlig entschärfte Produkte. Sie enthalten neben Tensiden nur schwache organische Säuren wie die Citronensäure.
Weitere Texte zum Thema „Schwefel“