Klick mich an!
Bild 1: Zuckerrohr - so weit das Auge reicht!
GroŖe Felder auf Mauritius
(Foto: Daggi)
Schon allein aufgrund ihrer nicht zu aufdringlichen SŁŖe und ihrer relativ einfachen Herstellbarkeit
ist die Saccharose konkurrenzlos, so dass sie das im Haushalt gebršuchlichste Disaccharid geworden ist. Im
Haushalt dient sie vorwiegend als SŁŖungsmittel. Hinzu kommt (aufgrund
ihres osmotischen Effekts) die Nutzung zum Konservieren von Lebensmitteln: Sie entzieht Mikroorganismen das
Zellwasser, so dass die inaktiviert werden. Das hšlt z. B. Marmeladen und FrŁchte frisch. Durch
Erhitzen stellt man aus Saccharose Zuckercouleur und Karamell her.
Saccharose ist in fast allen FrŁchten und auch sonst in allen Pflanzensšften enthalten (Biosynthese). Allerdings ist ihre Konzentration in keiner Pflanze so hoch wie im Zuckerrohr oder in der ZuckerrŁbe. Diese stellen die Hauptlieferanten der Saccharose dar. Aber auch Palmen und SŁŖkartoffeln enthalten sehr viel davon.
Jeder kennt die Kristalle des Kandiszuckers
Die ĄKluntjesď haben schon viele Kinder zum Spielen und vielleicht auch zum Nachdenken angeregt.
Die Kristalle, Łbrigens ein Beispiel fŁr MolekŁlkristalle,
gehŲren der monoklinen Kristallklasse an, also der gleichen
wie der der Gipskristalle. Die Kristalle erinnern ein wenig an kleine Sšrge.

Bild 2: Vielfalt von Kandiszucker-Kristallen
(Foto: Daggi)
Ihre Vielfalt ist bemerkenswert. Unabhšngig von der GrŲŖe der Flšchen sind jedoch alle Winkel
identisch. An ihnen kann man im Unterricht deshalb sehr schŲn das Gesetz
von Steno von der Winkelkonstanz herleiten.
Chemischer Aufbau von Saccharose
Saccharose ist ein Disaccharid. Es besteht aus den Grundeinheiten a-D-Glucose
und Ŗ-D-Fructose. Bei dieser Art von VerknŁpfung handelt es sich um ein Vollacetal.
Seine Bildung erfolgt hierbei Łber eine (a-1 -> Ŗ-2)-glykosidische
Bindung. Weil beide Monosaccharide Łber ihre Ąaktivenď C-Atome miteinander verbunden sind, wirkt
Saccharose nicht reduzierend.
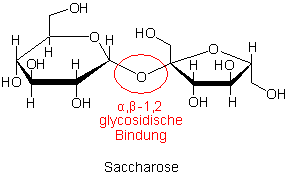
Es handelt sich hier also um eine glykosidische Bindung, die die reduzierenden funktionellen Gruppen maskiert. Saccharose reagiert deshalb nicht mit Fehling-LŲsungen.
Zu Verstšndnisschwierigkeiten bei der Konstruktion der Strukturformel der Saccharose lies auch Wie graphisch aus Glucose und Fructose Saccharose wird: Anmerkungen zu den gedrehten Strukturformeln.
Zuckerspaltung
Durch die hydrolytische Spaltung dieses Disaccharids erhšlt man Glucose und Fructose; gerade
letztere wird besonders aus Saccharose hergestellt. Das funktioniert in vitro (lat.
Ąim Glasď) nur unter Sšurekatalyse; man muss dazu die Saccharose mit einer verdŁnnten
Sšure erhitzen. Der Zucker wird aber auch im Darm (in vivo; lat. fŁr Ąim Lebendenď)
durch das Enzym ĄInvertaseď sehr leicht zerlegt. Man spricht von Rohrzucker-Inversion; die
Produktmischung heiŖt Invertzucker.
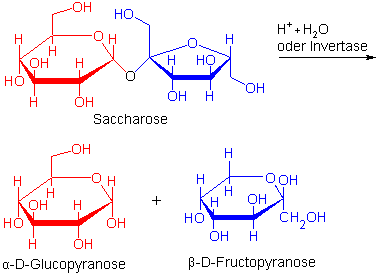
Interessant ist hierbei, dass Saccharose die ungewŲhnliche Ŗ-D-Fructofuranose enthšlt, nach der Spaltung allerdings Ŗ-D-Fructopyranose als normale Fructoseform entsteht.
Warum wird die resultierende Zuckermischung Invertzucker genannt? Die Inversion (ĄUmkehrungď) betrifft den Drehwinkel des polarisierten Lichtvektors. Saccharose weist eine spezifische Drehung [a]D = + 66,5į auf. Die durch Hydrolyse gebildete D-Glucose hat eine Drehung von [a]D = + 52,7į, die D-Fructose [a]D = - 92,4į. Daraus folgt fŁr die spezifische Drehung der resultierenden Produktmischung:
[a]D = + 52,7į + (- 92,4į) = - 19,8į
Wegen der Linksdrehung des polarisierten Lichts wird die Fructose auch als Lšvulose bezeichnet (lat. laevus, links).
Saccharose ist ein nachwachsender Rohstoff
Saccharose wird auch als nachwachsender Rohstoff
(ĄNon Food Materialď) industriell genutzt. So ist sie Ausgangsstoff fŁr diverse Kunststoffe. Sie
dient allerdings auch zur Herstellung von verschiedenen organischen Verbindungen wie Sorbit oder
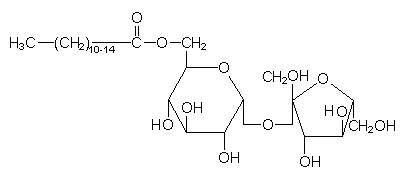
Zuckersšuren. In Form von Palmitinsšureestern wird sie sogar als nicht-ionisches, hautschonendes und
biologisch leicht abbaubares Tensid (z. B. im PRILģ enthalten) genutzt.
Durch Vergšrung von Saccharose stellt man ĄBioethanolď her, der weniger zum Trinken dient als zur Produktion von ĄBiospritď. Riesige Monokulturen von Zuckerrohr in Brasilien, fŁr die man sogar Regenwšlder gerodet hat, kŁnden von diesem uns als umweltgerecht angepriesenen Irrsinn.
Saccharose kann auch unerwartete BedŁrfnisse befriedigen. So kann man es zum Recyceln von Bleiakku-Schrott benutzen. Sie ist nšmlich in alkalischem Milieu in der Lage, schwerlŲsliche Bleiverbindungen unter Komplexbildung lŲslich zu machen.
