Prof. Blumes Tipp des Monats März 2015 (Tipp-Nr. 213)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Kreatin und Kreatinin
Immer wieder gibt es Anfragen wegen eines Nahrungsergänzungsmittels: Kreatin. Viele Sportler versuchen, damit ihre Muskeln aufzupeppen. (Die Wirkung ist wissenschaftlich allerdings sehr umstritten…) Entsprechende Präparate gibt es überall zu kaufen - vor allem auch im Internet. Folglich gibt es viele Bitten bezüglich der Hilfe bei Facharbeiten, die sich damit befassen.
Früher war Kreatin nur als Bestandteil einer Fleischbrühe bekannt (worin die Substanz auch entdeckt wurde): Was wäre eine Krankheit ohne die gute Kraftbrühe, die Mutter oder Oma zubereiteten? Kreatin wurde später auch direkt in frischem Fleisch nachgewiesen (griech. kreas, Fleisch). Kreatin ist unter anderem neben anderen Substanzen auch für den Geschmack von Fleisch mitverantwortlich. Es soll sogar appetitanregend sein.
Das Abbauprodukt des Kreatins heißt Kreatinin. Deshalb werden Kreatin und Kreatinin meistens zusammen genannt und dabei leider auch oft verwechselt.
Wie entsteht Kreatin im Körper?
Kreatin wird in der Leber synthetisiert. Dabei wird die Aminosäure Glycin zunächst mit der
Guanidogruppe des Arginins gekoppelt. Auf die so entstandene Guanidoessigsäure wird der Methylrest von Methionin übertragen. Die resultierende
Methylguanidoessigsäure wird Kreatin genannt.
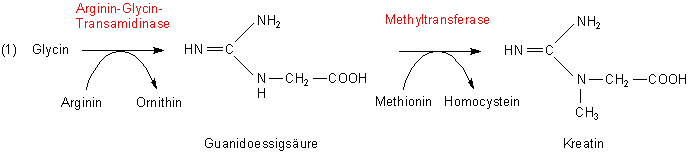
Kreatin gelangt über die Blutbahn aus der Leber in die Muskulatur.
Welche Rolle spielt Kreatin im Körper?
Es ist für die Energieversorgung der Muskulatur unerlässlich. Unmittelbar wirksamer Energieüberträger bei der Muskelkontraktion ist
eigentlich das ATP. Da bei anhaltender Muskeltätigkeit nicht immer ausreichend Sauerstoff
zur atmungsunterstützten ATP-Synthese vorhanden ist und die Glykolyse zu wenig ergiebig ist, muss der Muskel auf andere rasch verfügbare
Energiespeicher zurückgreifen. Das sind im Muskel immer Phosphatspeicher. Einer der wichtigsten Phosphatspeicher ist das
Kreatinphosphat.
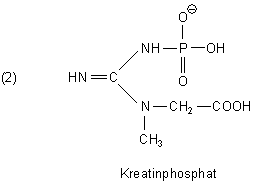
Es wird im Ruhezustand im Muskel unter Verbrauch eines ATP-Moleküls und Mitwirkung von Enzymen wie die Kreatinkinase
synthetisiert. Das Enzym heißt auch ATP-Kreatin-transphosphorylase.
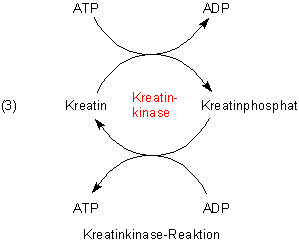
Kreatinphosphat dient zur Regenerierung von ATP. Denn die Reaktion ist reversibel. Wenn aufgrund hoher Muskelbelastung zuviel ATP in
ADP umgewandelt ist, läuft die Reaktion wieder in Richtung auf die Bildung von ATP. Dabei liegt das Gleichgewicht deutlich auf der ATP-Seite.
Kreatinphosphat kann im Körper aber auch spontan (d. h. ohne Beteiligung von Enzymen) unter Phosphatabspaltung direkt in Kreatinin umgewandelt werden.
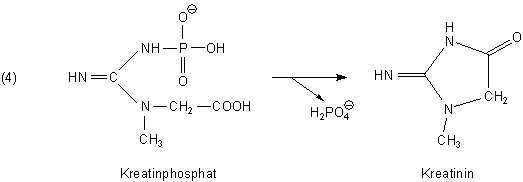
Das so entstandene Kreatinin kann im menschlichen Stoffwechsel nicht zurückverwandelt werden. Es wird deshalb über die Niere ausgeschieden.
Wie kann man (wie heute gewünscht) große Mengen an Kreatin gewinnen?
Die Extraktion von Fleisch ist zu mühsam. Deshalb stellt man Kreatin technisch her und zwar durch Addition von Cyanamid an Sarkosin
(N-Methyl-Glycin).
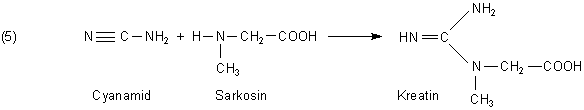
Für Kreatin gibt es mittlerweile auch biotechnologische Synthese-Methoden.
Chemische Eigenschaften
Kreatin ist wie schon erwähnt Methylguanidoessigsäure. Diese ist letztlich eine Aminosäure. Kreatinin ist deren zyklisches Amid, also ein
Lactam. Deshalb kann sich Kreatinin nicht nur aus Kreatinphosphat, sondern auch unter Abspaltung eines Wassermoleküls direkt aus Kreatin bilden.
Diese energetisch bevorzugte Cyclisierungsreaktion lässt sich durch Protonenkatalyse (z. B. durch Zusatz von Salzsäure) beschleunigen.
(Das wirft die interessante Frage auf, wie viel von dem Kreatin, das mit der Nahrung zum Muskelaufbau aufgenommen wird, überhaupt die Säureschwelle des
Magens überwinden kann…)
Lösungen von Kreatin reagieren neutral, die von Kreatinin dagegen deutlich alkalisch. Die Ursache:
Kreatin trägt eine basische und eine saure Funktion, die sich intramolekular absättigen. Deshalb liegt es wie alle Aminosäuren als Zwitter-Ion vor.
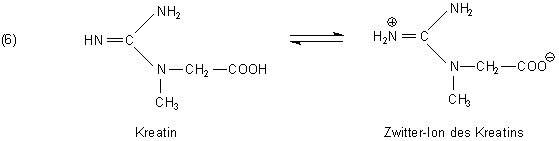
Kreatinin dagegen enthält als Lactam nur einen basischen Rest, der dem Wasser Protonen zu entziehen vermag. Die entstehenden
Hydroxid-Ionen sorgen für das alkalische Milieu.
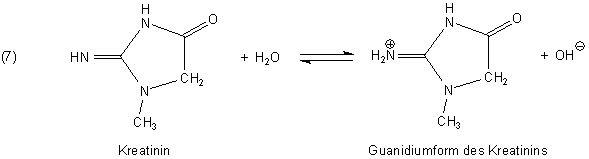
Guanidin ist ein Harnstoffderivat: Iminoharnstoff. Die Iminogruppe wirkt
stärker basisch als die im Ring gebundenen Aminogruppen. Sie schwächt sogar noch die Basizität der benachbarten Aminogruppen, da sie
stark Elektronen ziehend wirkt.
Was ist der Sinn von Nachweisen für Kreatin und Kreatinin?
Die Anwesenheit der beiden Guanidin-Verbindungen muss aus vielfältigen Gründen bekannt sein. Das schließt wenn möglich auch Kenntnisse über deren
Konzentrationen ein.
Einmal betrifft es lebensmittelchemische Untersuchungen, die zum Beispiel auch die Qualität des Fleisches betreffen.
In der Medizin ist der Nachweis von Kreatin unter anderem wichtig bei der Diagnose von Muskelerkrankungen (z. B. Muskeldystrophie) bzw. Muskelverletzungen.
Der Nachweis von Kreatinin spielt aber auch eine wichtige Rolle bei der Diagnose von Erkrankungen der Nieren. Der so genannte Kreatinin-Wert gibt Aufschluss über die Funktion der Niere. Er ist zum Beispiel unerlässlich bei Untersuchungen mittels MRT (früher Kernspin-Tomographie genannt). Dort werden zur Kontrastverstärkung Komplexe des Gadoliniums gespritzt, die leicht toxisch sind und deshalb rasch über die Nieren ausgeschieden werden müssen.
1. Klassische Nachweismethoden für Kreatin und Kreatinin
Es handelt sich um Farbreaktionen, die ab und zu noch genutzt werden.
Kreatin in Nahrungsergänzungsmitteln kann man indirekt nachweisen, indem man es durch kurzzeitiges Erhitzen einer salzsauren Lösung des Mittels in Kreatinin umwandelt, die Lösung neutralisiert und dann wie in den folgenden Versuchen beschrieben verfährt.
Kreatinin kann direkt im Harn, im Fleischextrakt (Brühwürfel) und auch im Blutserum nachgewiesen werden.
|
Versuch 1: Nachweis von Kreatinin mit der Jaffé-Reaktion [3]
|
Die Jaffé-Reaktion wird in einem Schullabor kaum durchzuführen sein, da Pikrinsäure nicht mehr vorhanden sein dürfte. Ein anderer Nachweis, die Weyl-Probe, kommt wohl ohne in der Schule verbotene Chemikalien aus.

Bild 1: Nachweise von Kreatinin.
(1) Analysenlösung. (2) Probe nach Jaffé. (3) Probe nach Weyl
(Foto: Daggi)
|
Versuch 2: Nachweis von Kreatinin mit der Weyl-Reaktion [3]
|
Die Jaffé-Reaktion wird wegen der Farbstoffbildung auch photometrisch durchgeführt. Dadurch sind auch quantitative Aussagen möglich.
2. Moderne Nachweismethoden für Kreatin und Kreatinin
Moderne Nachweisreaktionen erfolgen enzymatisch.
Zur Bestimmung von Kreatin wird dieses mit Hilfe der Kreatinkinase mit ATP phosphoryliert; die Konzentration des dabei entstandenen ADP wird durch eine weitere, gekoppelte enzymatische Hilfsreaktion ermittelt.
Kreatinin wird unter Einwirkung eines mikrobiologisch gewonnenen Enzyms (Kreatinin-amido-hydrolase) zunächst in Kreatin rückverwandelt. Dann wird die Konzentration des entstandenen Kreatins wie beschrieben bestimmt.
Literatur:
[1] H. Beyer: Lehrbuch der Organischen Chemie, S. Hirzel Verlag, Leipzig (neueste Auflage).
[2] E. Buddecke: Grundriss der Biochemie. Walter de Gruyter-Lehrbuch. Berlin 1971.
[3] Experimente nach: Physiologisch-Chemisches Praktikum. Manuskript des Physiologisch-Chemischen Instituts der Universität
Tübingen 1964.
[4] H.-D. Belitz, W. Grosch, P. Schieberle: Lehrbuch der Lebensmittelchemie; Springer-Verlag, 6. Auflage, Berlin Heidelberg
New York 2008.
Rüdiger Blume
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 26. Februar 2015, Dagmar Wiechoczek