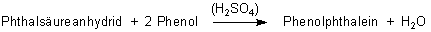
Synthese von Phenolphthalein
Experimente:
Versuch: Synthese von Phenolphthalein
Der Name Phenolphthalein weist darauf hin, dass die Substanz aus
Phenol und Phthalsäure
hergestellt wird.
Die in frischem Zustand farblosen Verbindungen Phenol und Phthalsäureanhydrid verbinden sich in einer Kondensationsreaktion (-> Versuch) in Gegenwart von Schwefelsäure zu einer zunächst roten Schmelze.
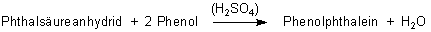
Die Schwefelsäure spielt bei der Kondensationsreaktion die Rolle eines Katalysators (genau genommen machen das ihre Protonen). Außerdem bindet Schwefelsäure das abgespaltene Wasser und sorgt so für Gleichgewichtsverschiebung. (Vergleiche die katalysierte Esterbildung.) Die Schwefelsäure sorgt aber auch für die anfänglich rote Färbung der Schmelze, die stark sauer ist. (Davon unten mehr.)

Links die Mischung der Edukte, rechts die heiße Schmelze des Produkts Phenolphthalein
(Foto: Daggi)
Wenn wir die rote Schmelze in viel Wasser gießen, wird sie weniger sauer und damit oftmals sogar fast farblos. Das macht Schüler oftmals ratlos: Dann ist doch wohl überhaupt kein Farbstoff entstanden!
Doch: Man muss nur Natronlauge zugeben. Dann färbt sich die Lösung rasch purpurfarben. Die Farbe hängt also vom pH-Milieu der Lösung ab. Deshalb ist Phenolphthalein ein Säure/Base-Indikator. Wegen seines ausgeprägten Farbwechsels ist er wohl auch der bekannteste aller Indikatoren.
Stoffe, die ihre Farbe mit dem pH-Wert ändern, zeigen das Phänomen der Halochromie.
Das nächste Bild zeigt den Ablauf der Synthese anhand der Strukturformeln.
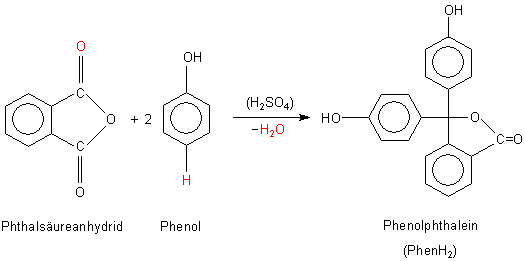
Synthese von Phenolphthalein
Bei diesem Versuch lernen wir, dass ein großes Farbstoffmolekül aus kleinen, farblosen Molekülen aufgebaut werden
kann. Im Folgenden lernen wir aber auch, dass die Farbigkeit einer Verbindung letztlich noch von
der Umgebung abhängt.
Weitere Texte zum Phenolphthalein