Prof. Blumes Tipp des Monats September 2003 (Tipp-Nr. 75)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Chemie des Tintenkillers
Viele Kinder benutzen bei den Schularbeiten Tintenkiller. Deshalb fragen sich auch die Eltern: Wie funktionieren sie und welche Stoffe sind darin enthalten? KŲnnen die nicht giftig sein?
Andererseits: Was wšre heute ein SchŁler ohne Tintenkiller? Der verhilft zu sauberem Aussehen der abgegebenen Klassenarbeit und stimmt erfahrungsgemšŖ den korrigierenden Lehrer milder. Wir frŁher mussten dagegen entweder textlich Misslungenes durchstreichen (dann sah eine Klassenarbeit furchtbar aus) oder wir versuchten es mit harten Radiergummis. Das fŁhrte oft genug zur DurchlŲcherung des Papiers. Ob Sie es glauben oder nicht: FrŁher gab es Lehrer, die das Radieren glatt untersagten. Man hatte stattdessen mit Lineal einen feinen Strich zu ziehen und das zu korrigierende Wort in SchŲnschrift (diesmal hoffentlich richtig) neu zu schreiben.
|
Versuch 1: Wirkungsweise eines Tintenkillers
|
Heute sind auch die zunšchst verpŲnten Tintenkiller so akzeptiert, dass manche Lehrer dazu sogar Facharbeiten ausgeben: Wie funktioniert ein Tintenkiller? Vor allem: Was steckt chemisch dahinter?
Kann man die Wirkung der Tintenkiller auch im Reagenzglas zeigen? Dazu mŁssen wir erst einmal wissen, was darin enthalten ist, was die Bleichsubstanz ist.
Chemische Untersuchung eines Tintenkillers
Wir haben eine Reihe von Fabrikaten gekauft, und wir haben sie alle ausprobiert.
Zur Untersuchung Ųffnet man einen Tintenkiller. Der farblose Filz enthšlt die
BleichlŲsung, der blaue die tintenkillerresistente Tinte zum Korrekturschreiben.
Dazwischen befindet sich ein farbloses KunststoffstŁck, um die beiden Filze auseinander zu halten.
Alle Produkte zeigten alkalische Reaktion.
Als Bleichsubstanzen kommen Natriumsulfit Na2SO3 oder Natriumdithionit
Na2S2O4 in Frage. Aus vielerlei GrŁnden beschršnken wir uns auf
das Natriumsulfit.
|
Versuch 2: Untersuchung der Bleichsubstanz eines Tintenkillers
|
HSO3- + H+ ———> H2O + SO2
|
Die Reaktion ist eine Nachweisreaktion fŁr Sulfit.
HSO3- + H2O + I2 ———> HSO4- + 2 I- + 2 H+
|
Sie reagiert alkalisch. Die alkalische Reaktion beruht darauf, dass Natriumsulfit als Salz einer schwachen Sšure mit Wasser eine Protolyse erleidet.
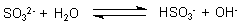
Es spricht also alles dafŁr, dass es sich bei dem Bleichmittel um Natriumsulfit-LŲsung handelt.
(Dem Vernehmen nach hat man dem Tintenkiller zur Verstšrkung der alkalischen Reaktion noch Soda hinzugefŁgt.)
Nun mŁssen wir erproben, ob auch das Natriumsulfit aus der Chemikaliensammlung mit Tinte reagiert.
|
Versuch 3: Entfšrbung von Tinte mit NatriumsulfitlŲsung
|
Was der Tintenkiller beim FarbstoffmolekŁl bewirkt
Tinten beruhen auf organischen Farbstoffen. Hierbei handelt es sich vor allem um Triaryl-methan-Farbstoffe
(auch Triphenyl-methan-Farbstoffe genannt). Bekannt fŁr diese Reihe ist zum Beispiel das
Kristallviolett, das auch als Stempelfarbe dient.
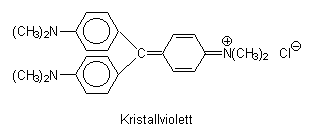
Die Triaryl-methan-Farbstoffe (zu denen auch die Schulklassiker Phenolphthalein oder Fluorescein gehŲren) haben alle eine šhnliche Struktur. Vor allem gibt es ein zentrales, ungesšttigtes C-Atom, an dem drei aromatische Reste hšngen. Diese Konstellation ist fŁr die Farbigkeit der Substanzen verantwortlich. Sie enthalten viele vagabundierende Elektronen, die sich Łber das ganze FarbstoffmolekŁl verteilen kŲnnen. Sie sind bereits durch sichtbares Licht leicht anregbar, absorbieren deshalb aus dem einstrahlenden Licht bestimmte Wellenlšngenbereiche (beim Kristallviolett zum Beispiel GelbgrŁn) und geben die Komplementšrfarbe unveršndert zurŁck. Voraussetzung fŁr die Beweglichkeit der Elektronen ist, dass das gesamte MolekŁl planar wie eine Scheibe ist.
Negativ geladene Teilchen (Anionen) wie das Hydroxid-Ion OH- oder das Hydrogensulfit-Ion HSO3- greifen am zentralen C-Atom an und werden addiert. Das zentrale C-Atom verliert so seinen ungesšttigten Charakter. Das kann man besonders schŲn am Kristallviolett zeigen.
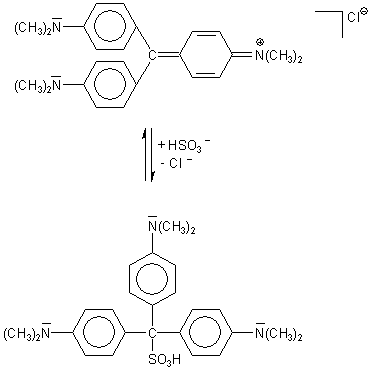
Durch die Addition des Anions wird die Geometrie des FarbstoffmolekŁls total
veršndert: Es verliert seine Planaritšt und nimmt die Form einer Pyramide an. (FŁr
Fachleute: Im Triaryl-methan-FarbstoffmolekŁl ist das zentrale Kohlenstoffatom
sp2-hybridisiert, im Additionsprodukt finden wir den sp3-Typ.)
Damit kŲnnen sich die Elektronen nicht mehr Łber das ganze MolekŁl verteilen; das
sichtbare Licht kann nicht mehr mit ihnen in Wechselwirkung treten. Der Farbstoff absorbiert
statt sichtbaren Lichts nun nur noch UV-Strahlung. Folglich wird der Stoff fŁr uns
farblos, er wird zum Leukofarbstoff.
Auf Grund ihrer negativen Ladung reagieren die Anionen vor allem mit solchen
Triaryl-methan-Farbstoffen, deren MolekŁle wie beim Kristallviolett (abgekŁrzt KV)
positiv geladene Ionen sind.
KV+ + HSO3- ———> KV-SO3H
|
Versuch 4: Entfšrben von KristallviolettlŲsungen
|
Grund ist, dass Wasserstoffperoxid (H2O2) den Sulfitrest im Kristallviolett-MolekŁl zu Sulfat oxidiert, was zum Zerfall des Additionsprodukts fŁhrt. Das RŁckfšrben erreicht man auch durch Liegenlassen der Korrektur an der Luft, was mit der Beobachtung Łbereinstimmt, dass gekillte Schrift irgendwann wieder lesbar wird.
Man kann die Entfšrbung auch durch Zusatz von Aldehyden wieder rŁckgšngig machen.
|
Versuch 5: RŁckfšrben von Kristallviolett mit Acetaldehyd
|

(Foto: Daggi)
Darauf beruht ein klassischer Aldehydnachweis, bei dem allerdings mit Fuchsin
gearbeitet wird (-> Schiff-Reagenz). Grund fŁr die
RŁckfšrbung ist, dass auch die Aldehyde mit Sulfit eine Additionsverbindung bilden,
zu deren Bildung sie das Sulfit-Ion dem LeukofarbstoffmolekŁl entreiŖen. Allerdings
wird nicht mehr die volle Farbtiefe erreicht, weil es sich um eine
Gleichgewichtsreaktion handelt.
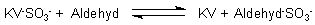
Das RŁckfšrben kŲnnen wir auch mit der entfšrbten, zuvor blauen Tinte zeigen.
|
Versuch 6: RŁckfšrben von gebleichter Tinte
Hinweis: Dieser Versuch funktioniert nicht mit allen Tintensorten! Deshalb mŁssen Sie den Versuch unbedingt vorher ausprobieren. |
Die Tintenkillerstifte sind, wenn man sie nicht gerade zum Mittagessen verspeist, gesundheitlich unbedenklich. Das gilt auch fŁr das bisschen Alkohol, das man dem Tintenkiller zur ErhŲhung seiner Wirksamkeit hinzugefŁgt hat.
Warum reagiert die Lehrertinte nicht mit Tintenkillern?
Das ist eigentlich genial und weise von der Natur eingerichtet. Die blaue Tinte der SchŁler
lšsst sich tilgen, die rote Kommentar- und Korrekturtinte der Lehrer dagegen nicht. Woran das liegt,
erfahren Sie auf einer besonderen Webseite.
÷kologische Tintenkiller
Ab und zu begegnen einem Tintenkiller, die als Ųkologisch unbedenklich gelten. So soll man statt
Natriumhydrogensulfit eine LŲsung von Natriumhydrogencarbonat oder Natriumcarbonat nehmen. Beide
reagieren schwach alkalisch, denn sie bilden mit Wasser OH--Ionen (Stichwort "Protolyse").
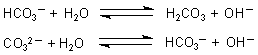
Diese Ionen addieren sich wie die Hydrogensulfit-Ionen am mittleren C-Atom des FarbstoffmolekŁls. Die Folge: Der Farbstoff entfšrbt sich. Probiert es mal aus!
Nur bildet sich bei Einwirkung von Luft die blaue Farbe leicht zurŁck. Der Grund ist, dass das darin enthaltene CO2 sich als Sšureanhydrid mit Wasser zu Kohlensšure umsetzt. Dazu reichen auch die leichten Feuchtigkeitsspuren im Papier aus. Die Protonen der Kohlensšure entziehen dem Leukofarbstoff die OH--Ionen, und so kommt es zur RŁckfšrbung der Tinte.
Zum guten Schluss etwas FšcherŁbergreifendes
Der Tintenkiller wirft aus philosophischer Sicht ein Problem auf, auf das Mike KrŁger in der
RTL-Sendung "7 Tage - 7 KŲpfe" aufmerksam gemacht hat: Wo eigentlich bleibt das gelŲschte Wort?
Wohin geht es? Was wird aus ihm?
Dank an Dr. Norbert Fischer von der Firma Pelikan!
Zur Chemie mit Wasserstoffperoxid haben wir eine groŖe
Webseitengruppe.
RŁdiger Blume
Diese Seite ist Teil eines groŖen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver fŁr Chemie.
Letzte ‹berarbeitung: 04. Januar 2011, Dagmar Wiechoczek