Weshalb einige Aromaten cancerogen sind
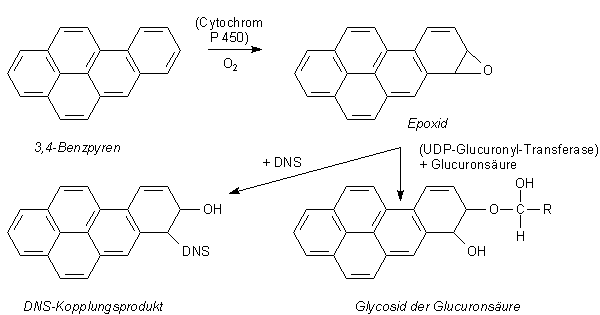
Stadtkinder weisen einen um 70 % höheren Benzolgehalt im Blut auf als Kinder in Reinluftgebieten. Dies liegt sicherlich am Aromatengehalt des Benzins. Wie man vor einigen Jahren erkannte, sind Benzol und einige seiner Substitutionsprodukte krebserregend. Von besonderer Bedeutung sind in diesem Zusammenhang polykondensierte Aromaten (PAK) wie das stark cancerogene 3,4-Benzpyren. Dieser Inhaltsstoff des Steinkohlenteers tritt aber auch in geringer Konzentration in Abgasen von Dieselmotoren, im Zigarettenrauch, im Schornsteinruß, in gegrillten und geräucherten Esswaren sowie in den Abgasen von Kraftwerken auf.

Bildung von Carcinogenen in der Zelle
Kondensierte Aromaten sind als inerte Substanzen nicht von vornherein cancerogen, sondern werden erst im Organismus in Cancerogene umgewandelt. Für das Verständnis der Wirkung von Aromaten im Organismus ist es notwendig zu wissen, wie diese als nicht verwertbare und wasserunlösliche Nahrungsbestandteile im Stoffwechsel zur Ausscheidung über den Harn vorbereitet werden. Dazu werden Aromaten durch spezifische Enzyme (unter Beteiligung von Cytochromen wie P-450) in Epoxide überführt und anschließend mit Zucker- oder Aminosäuren sowie Schwefelsäure verbunden und damit wasserlöslich gemacht. Die Bildung der beteiligten Oxidations- und Transfer-Enzyme wird durch die Aromaten über den so genannten Ah-Rezeptor stimuliert (-> Webseite Dioxin).
Aromatische Epoxide stellen im unveresterten Zustand eine Gefahr für das Lebergewebe, Lungengewebe und für die Harnblase dar. Der Grund ist, dass die Epoxide mit Basen der DNS irreversible Bindungen eingehen, wodurch Allergien und sogar Krebs entstehen können. Dies ist ganz besonders dann der Fall, wenn die Epoxide zur DNS diffundieren und ankoppeln, bevor sie eine entgiftende Esterbindung eingehen. Die Wahrscheinlichkeit hierzu steigt mit zunehmender Konzentration von Aromaten in der Zelle, also auch mit der Aufnahme dieser Substanzen. Damit erklärt sich auch, dass nicht nur aktive Raucher, sondern auch Passivraucher ein erhöhtes Krebsrisiko aufweisen.
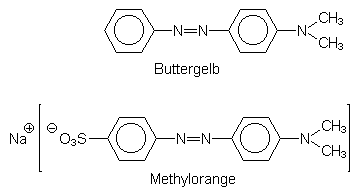
An dieser Stelle kann auch erklärt werden, warum der Azofarbstoff Buttergelb stark cancerogen und deshalb seit 1938 verboten ist, während die ähnlich gebaute Verbindung Methylorange nicht cancerogen ist und sogar im Schulunterricht als Indikator verwendet werden darf. (Achtung: Methylorange ist trotzdem giftig und trägt das Gefahrensymbol (T) - aber nur als Feststoff.) Der Grund für die fehlende Cancerogenität ist, dass Methylorange wegen der polaren Sulfogruppe von vornherein wasserlöslich ist und in den Harn gelangt, während Buttergelb als fettlöslicher Farbstoff erst die oben geschilderten oxidativen Prozesse durchlaufen muss, um wasserlöslich zu werden. Dabei wird er in ein akutes, epoxidisches Cancerogen umgewandelt.
Erinnert sei auch an den Austausch von a-Naphthylamin (Lunges Reagenz) in N-(1-Naphthyl)-ethylendiamin-hydrochlorid (Saltzmans Reagenz) in den Lösungen zur Bestimmung von Nitrit-Ionen bzw. von NOx.
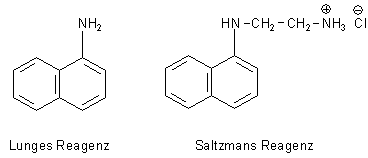
Während Lunges Reagenz nicht wasserlöslich und daher cancerogen ist, ist für Saltzmans Reagenz das Gegenteil richtig. Aus diesem Grunde weist man Nitrit-Ionen nur noch mit Saltzmans Reagenz nach.
Außerdem werden auch viele Terpene wie das aus dem Zitronenschalenöl stammende Limonen nach dem Epoxid-Mechanismus "entgiftet". Sie stehen deshalb im Verdacht, cancerogen zu sein. Zumindest sind sie starke Allergene.
Weitere Texte zum Thema „Auto“