Prof. Blumes Tipp des Monats Mai 2005 (Tipp-Nr. 95)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Wann der Bernstein schwimmt
Bald ist wieder Ferienzeit. Dann tummeln sich viele Leute am Strand der Ostsee. Dort wird eifrig nach angeschwemmtem Bernstein gesucht. Am besten sucht man nach einem kräftigen Sturm im Tang.

Bild 1: Alex bei der Bernsteinsuche
(Foto: Sonja)
Den Bernstein erkennt man an seiner gelben bis rötlichbraunen Farbe. Manche Stücke sind sogar durchscheinend klar!
Das sieht man aber meistens erst zu Hause, wenn man seine Schätze begutachtet.

Bild 2: Bernsteinausbeute von der Insel Mön
(Foto: Alex Blume)
Nun gibt es aber noch mehr Steine mit
dieser Farbe und Eigenschaft: Am häufigsten findest du die zylinderförmigen Bruchstücke
von Belemniten-Rostren, die überall herumliegen. Diese fossilen Spitzen der Innenpanzer
("Schulp") von großen Kreide-Tintenfischen nannten unsere Altvorderen "Donnerkeile"
("Donars oder Thors Keile") oder auch "Hexenfinger". Die stecken überall in der Schreibkreide
und sehen, wenn sie komplett sind, wie kleine Geschosse aus. Man meinte früher, dass sie
Reste von Blitzeinschlägen wären - daher die Bezeichnung Donars Keile.

Bild 3: Donnerkeile aus der Kreide (Belemnitella mucronata)
(Foto: Blume)
Dazu liegen an der Küste noch gelbbraune Feuersteine herum. Und vor allem gibt
es viel abgeschliffenes Braunglas, das von deutschen Bierflaschen stammt. Alles
sieht so aus wie Bernstein. Deshalb ist die Suche nach dem "Edelstein des
Nordens" für Anfänger ziemlich frustrierend. Glücklicherweise gibt es dann ja
noch die Souvenirläden. Aber ein selbst gefundener Bernstein macht viel mehr
Spaß und ist immer noch der schönste in der Sammlung!

Bild 4: Bernstein auf magnetithaltigem Ostseesand
(Foto: Blume)
Wie aber können wir den Bernstein von den anderen Steinen unterscheiden?
Schwimmt Bernstein - ja oder nein?
Wenn du schon einmal einen Bernstein in der Hand gehalten hast, wird dir
aufgefallen sein, dass er sich sehr leicht anfühlt. Die Wissenschaftler sagen,
dass er eine geringe Dichte hat. Der genaue Wert der Dichte liegt zwischen 1
und 1,1 g/cm3. Damit ist Bernstein geringfügig dichter als Wasser
mit 1 g/cm3. Deshalb ist zu erwarten, dass er zumindest im Wasser schwebt.
Probieren wir das einmal aus. Zuvor ein Hinweis: Bernsteine bekommst du billig
auf Mineralienbörsen oder in Mineralienläden. Oftmals handelt es sich um Abfall
der Bernsteinverarbeitung, den man zu neuen Steinen gepresst hat. Aber die
reichen für unsere Zwecke völlig aus.
|
Versuch 1: Schwimmt Bernstein?
|
Sei nicht enttäuscht: Der Stein geht unter. Nun müssen wir nachdenken. Liegt das vielleicht am Wasser? Richtig: Das Ostseewasser ist salzig, enthält also gelöstes Salz. Ändern wir den Versuch also ab.
|
Versuch 2: Bernstein schwimmt doch!
|
Woran liegt das? Durch das gelöste Salz ist das Wasser schwerer geworden. Besser gesagt: Seine Dichte hat zugenommen. Damit hat das Salzwasser mehr Auftrieb. Für den Auftrieb ist der Unterschied in den Dichten von Flüssigkeit und schwimmendem Körper verantwortlich: Je dichter das Wasser und je weniger dicht der Schwimmkörper ist, desto eher schwimmt der Körper oben.
Du meinst, so viel Kochsalz wäre gar nicht in der Ostsee? Dann kannst du den Versuch ja wiederholen, indem du schrittweise die Salzkonzentration im Wasser erhöhst. Dazu rührst du nach und nach immer mehr Salz hinein, während der Stein im Glas ist. Dann wirst du sehen, dass er bald anfängt, in der Lösung zu schweben.
Ein Tipp: Den meisten Bernstein findest du deshalb in den großen Algenkissen, die nach einem Sturm am Strand liegen.
Du kannst den Bernstein noch genauer untersuchen
Auf diese Weise kannst du Eigenschaften herausfinden, mit deren Hilfe du ihn von den anderen gelben
Stücken, die du am Strand aufgesammelt hast, unterscheiden kannst.
Prüfe zum Beispiel seine Härte.
|
Versuch 3: Härte von Bernstein
|
Bernstein lässt sich leicht mit einem harten Fingernagel oder mit einem Messer ritzen. Seine Härte beträgt 2-2,5 Einheiten auf der Mohs-Härte-Skala. Er ist damit so hart bzw. so weich wie ein Gipskristall. Mit Glas und Feuerstein lässt sich Bernstein ritzen. Feuerstein ritzt sogar Glas!
Bernstein ist darüber hinaus auch säureempfindlich. Lege ihn zum Beispiel in konzentrierte Salzsäure (C): Er färbt sich rasch dunkel; nach einigen Tagen ist er sogar schwarz geworden.

Bild 5 (Foto: Daggi)
Wenn es dem Bernstein zu warm wird
Du kannst auch versuchen, Bernstein zu erhitzen. Er schmilzt ab etwa 300 °C, wobei er sich dunkel
verfärbt und zersetzt.
|
Versuch 4: Schmelzen von Bernstein
|


Bild 6: Erhitzen von Bernstein
(Fotos: Daggi)
Es bilden sich rasch große Mengen an gelblichem Qualm. Dessen zunächst würziger Geruch erinnert an
Weihrauch. Der Hauptbestandteil von Weihrauch ist ein Baumharz. Das Harz stammt von einer besonderen
Akazienart, die im Jemen wächst. Sollte Bernstein etwas mit Baumharz zu tun haben? Das klären wir
gleich.
Mit zunehmendem Erhitzen wird der Geruch eher unangenehm. Was du jetzt riechst, ist der typische Brandgeruch, der vor allem auf ungesättigte Verbindungen wie Cyclohexen zurückzuführen ist.
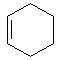
Cyclohexen
An der Glaswand bilden sich neben dem Rauch viele klare bis braune Tropfen von vielen Zersetzungsprodukten.
Diesen Versuch führte 1546 übrigens schon ein bekannter deutscher Alchimist durch, Georgius Agricola (also ein gewisser Georg Bauer) aus Sachsen. Dabei entdeckte er in den Zersetzungsprodukten eine Säure, die er Bernsteinsäure nannte. (Von der hören wir weiter unten mehr!)
|
Versuch 5: Verbrennen von Bernstein
|
Der Name Bernstein ist übrigens dem alten mittelhochdeutschen Wort barnsten oder bern(e)stein entlehnt, was soviel heißt wie "brennbarer Stein".
Warum überhaupt brennt Bernstein?
Bernstein ist kein anorganisches Mineral, sondern ein Mineral organischen Ursprungs. Er ist das
fossile Harz von Nadelbäumen (wie zum Beispiel von Pinus succinifer), die vor vielen Millionen
Jahren an der Ostsee wuchsen und die nach dem Umstürzen von Sand und Erde zugedeckt wurden. Das Harz
blieb weitgehend erhalten und hat sich chemisch nur wenig verändert, da es sehr stabil ist gegen
Umwelteinflüsse - auch solche, die über geologische Zeiträume hinweg einwirken.
Modernes Harz brennt sehr gut und rußt dabei ebenso wie Bernstein! Probiert das mal mit einem harzigen
"Kienspan" aus dem Wald aus.
Hier ist die Strukturformel eines typischen "Harzmoleküls".
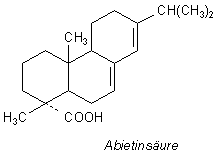
Der Bernstein hat elektrische Eigenschaften
Der griechische Name für Bernstein ist elektron. Dieser Name ist Programm!
|
Versuch 6: Elektrische Aufladung von Bernstein
|
Kein Wunder, dass man die in Versuch 6 demonstrierte Eigenschaft des Bernsteins "Elektrizität" nannte.
(Dahinter steckte der englische Physiker William Gilbert (1540-1603).)
Das war übrigens deutschtümelnden Sprachwissenschaftlern ein Dorn im Auge. Die
wollten bekanntlich alle Fremdwörter aus der deutschen Sprache verbannen. Als deutsches
Alternativ-Wort für "Elektrizität" hatten sie allen ernstes "Bern" im Angebot!
Und die gute Elektrolokomotive wollten sie tatsächlich in "Bernzieh" umtaufen! Kein Witz!
(Der Revolver sollte übrigens "Meuchelpuffer" heißen und die Nase "Gesichtserker".
Aus der Chemie kennen wir das „Auskreisen“ anstelle der Nutzung eines Soxhlet-Apparats.
Klicke hier und lies die Antwort auf die Frage
1725.)
Bernstein lädt sich beim Versuch 6 negativ auf. Glas hingegen lädt sich beim analogen Versuch positiv auf. Man unterschied deshalb lange Zeit zwischen der Harzelektrizität und der Glaselektrizität. Die heute gebräuchlichen Bezeichnungen negative Elektrizität (für erstere) und positive Elektrizität (für die zweite) führte erst 1747 der Amerikaner und geistige Weltbürger Benjamin Franklin (1706-1790) ein. Stellt euch vor, wenn er das umgekehrt definiert hätte. Dann wäre das Elektron heute positiv geladen...
Bernstein ist der vielleicht älteste Schmuckstein der
Menschheit
Das ist deshalb schon denkbar, weil er so leicht zu bearbeiten ist. In Museen gibt
es viele Schnitzereien zu bewundern. Jeder kennt wohl die Story um das
sagenhafte Bernsteinzimmer in St. Petersburg, das die Deutschen den Russen erst
geschenkt und später wieder geklaut haben.
Bernstein war wohl allgemein bekannt. Dafür spricht, dass es in vielen Sprachen
Bezeichnungen dafür gibt. Das griechische elektron haben wir schon kennengelernt.
Im Französischen spricht man von ambre; im Englischen von amber. Diese
aus dem Keltischen stammenden westeuropäischen Namen haben sich in der Wissenschaft allgemein
eingebürgert: Chemiker verwenden häufig einen Ionenaustauscher
mit dem Produktnamen Amberlite®. Dieser erinnert dem Aussehen nach an Bernstein.
Unter der Bezeichnung Ambroid ist ein aus Fertigungsabfällen gepresster Bernstein
im Handel - billig und ein vortreffliches Material für unsere Experimente.

Bild 7: Stark saurer Kationenaustauscher (Amberlite®)
(Foto: Blume)
Es gibt noch einen weiteren Wortstamm: Die Geologen nennen den Bernstein Succinit
- nach der lateinischen Bezeichnung succinum. Der oben erwähnte Baum pinus
succinifer heißt deshalb übersetzt: Der Nadelbaum, der Bernstein machte.
Woher kommt der Bernstein?
Bernstein wird weltweit überall gefunden. Denn er hat sich in den
verschiedensten Erdzeitaltern gebildet. Man kennt über 200 Millionen Jahre alte
Steine. Das europäische Vorkommen stammt wohl zum größten Teil aus der
Tertiärzeit und ist rund 32 bis 7 Millionen Jahre alt.
Wie gelangt der Bernstein ins Meer? Der Boden, in dem das fossile Harz liegt, wird nach und nach weggeschwemmt, und damit schwimmt auch der Bernstein bald in der Ostsee.
Es war vor allem der Ostsee-Stein, der in der Geschichte der Menschheit eine große Rolle spielte. Davon künden heute noch archäologische Funde - nicht nur in Europa, sondern auch in Vorderasien, Russland und Nordafrika. Viele Handelswege durch Europa basieren auf dem Bernsteinhandel. Das Sammeln und Fischen von Bernstein war früher ein eifersüchtig gehütetes Privileg. Schmuggel und Verbrechen waren deshalb an der Tagesordnung. Heute braucht man keine Angst mehr vor anderen Leuten zu haben, wenn man nach einer Sturmnacht am deutschen oder dänischen Ostseestrand sammeln geht.
Den meisten Bernstein gewinnt man heute im industriellen Tagebau. Sammler gehen auch gern an die Steilküsten und graben dort. Die bekanntesten Fundorte liegen in Ostpreußen und im Baltikum, im Samland. Man spricht hier sogar von der Bernsteinküste.
Wie man Baltischen Bernstein sicher erkennt, beschreiben wir in einem anderen Tipp des Monats.
Warum Bernstein so wichtig ist für Geologie und Biologie
Manche Bernsteinstücke sind glasklar durchsichtig. Wenn du dir so ein Stück anschaust,
erkennst du manchmal Einschlüsse, so genannte Inklusen oder Inklusionen. Das können sogar
Insekten oder kleine Wirbeltiere sein. Die sind häufig so gut erhalten, dass man sogar ihre
Art genau bestimmen kann.
Klick mich an!
Bild 8: Frisches Baumharz mit eingeschlossenen Insekten
(Foto: Blume)
Da es den Bernstein schon seit über 200 Millionen Jahren gibt, haben die Paläontologen hiermit
ein hervorragendes und kündigungssicheres Arbeitsfeld.
Was ist Bernsteinsäure?
Zum Bernstein liest man in einem (ansonsten sehr empfehlenswerten) Mineralienbuch*), dass er bei
350 °C schmilzt, "wobei er den typischen penetranten Geruch von Bernsteinsäure verströmt". Stimmt
das? In Betriebsanweisungen zum Umgang mit Gefahrstoffen findet man unter dem Eintrag "Bernsteinsäure":
"C4H6O4; Butandisäure, 1,2-Ethandicarbonsäure. Farbloses Pulver ohne Geruch".
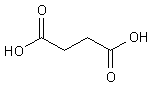
Bernsteinsäure
Die Säure ist bei Zimmertemperatur fest. Der Schmelzpunkt der schuppigen, farblosen Kristalle liegt bei 185 °C. Ihre Salze und Ester heißen Succinate. In England spricht man von succinic acid. Aus der Biochemie ist der Name des Salzes, das Succinat, bekannt. Denn beim physiologischen pH-Wert um 7 liegt die Bernsteinsäure als Anion vor.
Die Bernsteinsäure ist in unserem Körper weit verbreitet. Sie tritt vor allem an der zentralen Stelle im biochemischen Stoffwechsel auf, im bekannten Citronensäure-Zyklus. Hier ist sie nicht nur Zwischenprodukt bei der Endoxidation des Kohlenstoffs, sondern auch Mittler zwischen dem Stoffwechsel von Fettsäuren, Kohlenhydraten und Aminosäuren.
*) Marco Drago (etc.): Mineralien und Edelsteine; Der große Naturführer; Neuer Verlag Kaiser, Klagenfurt 1998.
Vorsicht beim Bernsteinsammeln: Es kann sich auch um weißen Phosphor handeln!
An Ostseestränden wird immer wieder weißer Phosphor angeschwemmt. Denn nach dem Krieg wurden
Phosphorkanister in der Ostsee versenkt. Die Metallbehälter korrodieren im Salzwasser und setzten auf diese Weise ihren
giftigen und brennbaren, in Wasser unlöslichen Inhalt frei. Das Gefahrenpotential verdeutlicht eine aktuelle Zeitungsmeldung
von 2014:
|
Ein Steinsammler hat an der schleswig-holsteinischen Küste einen Brocken weißen Phosphors für einen Bernstein gehalten und in die Hosentasche gesteckt. Nach kurzer Trocknungszeit entzündet sich der Phosphor und setzt die Kleidung des Manns in Brand. Der Mann wird schwer verletzt. Das Landeskriminalamt weist noch einmal ausdrücklich auf die Gefahren für Bernsteinsammler hin. |
Die weiße Modifikation des Phosphors ähnelt dem Bernstein:
- Mit einer Dichte von d = 1,82 g/cm3 ist sie vergleichsweise leicht.
- Obwohl man von weißem Phosphor spricht, ist er eher gelb und erinnert frisch geschnitten an festes Bienenwachs.
- Dazu ist weißer Phosphor im Allgemeinen wie Bernstein von einer grauen bis bräunlichen Rinde umgeben.
Übrigens sieht das linke Belemnitenbruchstück in Bild 3 aus wie das Stück einer Phosphorstange.
Bekannt ist er dafür, dass er sich in Kontakt mit Luft spontan entzündet. Deshalb wird er im chemischen Labor unter Wasser aufbewahrt. Seine niedrige Dichte sorgt dafür, dass er im Meerwasser unter der Wasseroberfläche treibt und sich somit nicht entzünden kann.
Rüdiger Blume
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 28. Januar 2014, Dagmar Wiechoczek
