Prof. Blumes Tipp des Monats Mai 2009 (Tipp-Nr. 143)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Schwefel im Wein
Experimente:
Versuch: Addition von Hydrogensulfit an Aldehyde
Versuch: Nachweis von Schwefeldioxid mit Iodpapier
Jetzt ist wieder die Zeit der Bowlenfeste. Nach dem Trinken von Maibowle
gibt es oftmals Probleme mit dem Kopf. Man sagt, das läge daran, dass im Wein Schwefel enthalten sei.
Und der mache eben Kopfschmerzen.

Nicht alle Winzer sind so ehrlich und schreiben auf das Etikett, was den Genuss und den
Genießer stören könnte... Das müssen sie auch nicht
(Foto: Blume)
Schwefel liegt im Wein natürlich nicht elementar vor, sondern als Verbindung.
In welcher Form liegt der Schwefel im Wein vor?
Genau genommen handelt es sich beim „Schwefel“ im Wein um alles, was das Gleichgewichtssystem
Schwefeldioxid/Wasser hergibt.
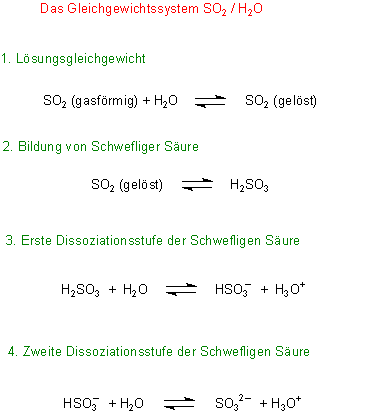
Im Allgemeinen spricht man nur von Sulfit. Bleiben wir also auch dabei.
Diese Substanzgruppe können wir mit Iod nachweisen.
|
Versuch: Nachweis von Sulfit in Wein
Ergebnis
Hinweis
|
Iod wirkt bei der Nachweisreaktion als Oxidationsmittel. Es oxidiert Sulfit zu Sulfat.
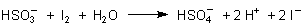
Für viele Weingenießer ist das Sulfit ein echtes Problem
Man kann die persönliche Sulfitaufnahme jedoch steuern: Denn die Konzentration von Sulfit variiert je nach
Art des Weins. Rotweine enthalten weniger als Weißweine. Die Konzentration wird vor allem aber auch vom Zuckergehalt
bestimmt. So genannt „liebliche“ Weine, Spätlesen und Eisweine enthalten mit über 300 mg/Liter am meisten Sulfit.
Ein Leser schreibt uns: „Selbst Biowein enthält Sulfit (schauen Sie doch mal auf die Rückseite des Flaschen-Etikettes; da steht das ganz klein und verschämt).“ Das stimmt. So enthalten Bioweine (mehr oder weniger unabhängig vom Zuckergehalt) mit 30 mg/Liter am wenigsten Sulfit.
Der Leser fragt weiter, warum man denn nicht auf den Zusatz von Sulfit verzichten kann oder ob es Ersatzstoffe gibt. Beides kann man gleich mit „Nein“ beantworten. Aber es gibt noch eine unerwartete Einschränkung für die naheliegende Bemühung, einen gänzlich sulfitfreien Wein zu machen.
Es ist gar nicht möglich, schwefelfreien Wein herzustellen !
Denn bei der alkoholischen Gärung entsteht als natürliches Nebenprodukt aus Sulfat und anderen im Traubensaft
enthaltenen Schwefelverbindungen Sulfit.
Das liegt an den im Most anaerob lebenden Hefen. Die haben nämlich ein echtes Überlebens-Problem, das sie mit Hilfe der Gärung lösen: Der Abbau von Kohlenhydraten wie Glucose erfolgt durch Oxidation, um Energie zu gewinnen. Könnten sie atmen, wären die Hefen fein heraus.
Primäre Oxidationsmittel sind biochemische Verbindungen wie NAD+, FAD oder FMN, wobei enzymatisch Wasserstoffverbindungen wie NADH/H+ oder FADH2 entstehen. Diese Oxidationsmittel sind in den klitze-kleinen Hefezellen aber nur begrenzt vorhanden. Sie müssen deshalb immer wieder freigesetzt werden, da sonst die Oxidation der Glucose zum Stillstand käme.
An der Luft ist das kein Problem. Dann wird der Wasserstoff von NADH/H+ oder FADH2 über die Atmungskette auf den Sauerstoff übertragen. Wir sprechen von „Atmung“.
Wenn aber kein Sauerstoff vorhanden ist, geht das natürlich nicht. Dann müssen die Oxidationsmittel ihren Wasserstoff, den sie von der Glucose abgespalten haben, anders entsorgen. Das nennt man „Gärung“.
Die mit Wasserstoff beladenen Verbindungen dienen bei der alkoholischen Gärung in erster Linie zur Reduktion von Acetaldehyd, wobei Ethanol entsteht.
An dieser Stelle muss gesagt werden, dass Hefen auch andere Moleküle reduzieren können. Und welche Moleküle das sind und was dabei entsteht, ist eine Frage der Umgebung: Traubensorte, Mineraliengehalt im Most, Hefeart und so weiter. So kommt es zu verschiedenen Geschmacksnoten der Weine.
Es entstehen sogar anscheinend exotische Verbindungen wie die „Önanthsäure“. Das heißt übersetzt „Weinsäure“. Die darf aber keineswegs mit der uns bekannten Weinsäure verwechselt werden. Bei der Önanthsäure handelt es sich nur um die Heptansäure.
Dabei bleibt es aber nicht: In einer weiteren Nebenreaktion vergären die Hefen sogar anorganisches Material wie Sulfat-Ionen - und dabei entsteht Sulfit.

[H] steht für die biochemischen Reduktionsmittel.
Unsere weinbildenden Saccharomyces-Hefen setzen auf diese Weise tatsächlich etwa 30 mg Sulfit pro Liter Wein frei - letztlich die Sulfitkonzentration der Bioweine. So ist sie halt, die echte Natur...
Warum überhaupt ist Sulfit für den Wein so wichtig?
Sulfit dient als Konservierungsmittel und stabilisiert deshalb den Wein. Wir müssen zwei
Wirkungsmechanismen unterscheiden:
1 Sulfit hemmt Mikroorganismen wie Hefen und Bakterien
Es reagiert nämlich mit Aldehyden und Ketonen, die im Stoffwechsel (leider auch im menschlichen...) reichlich
vorkommen. Denken Sie an die Glykolyse.
Aus diesem Grunde setzt man nicht nur dem fertigen Wein Sulfit zu, sondern schwefelt auch die Fässer vor der eigentlichen Gärung aus - um Fehlgärungen zu vermeiden. Dabei verbrennt man Schwefelfäden im feuchten Fass; das Oxidationsprodukt Schwefeldioxid sowie das daraus gebildete Sulfit wirken gegen unerwünschte Mikroorganismen.
Wenn man den fertigen Wein sulfitarm einstellt, hält er aus dem Grunde der „Verkeimung“ nicht lange. Er ist immer von Essigbakterien oder von wilden Hefen bedroht.
Vielleicht hat die Hefe es im Rahmen der Evolution „gelernt“, Sulfit zu erzeugen, um andere Mikroorganismen zu schädigen. Denn das sind ja Nahrungskonkurrenten.
Eine Frage wird immer wieder gestellt: Warum durch das Schwefeln nicht auch die „richtigen“ Weinhefen geschädigt werden. Das werden sie natürlich auch. Aber es gibt Hefearten, die gegen Sulfit unempfindlicher sind als die Wildarten.
2 Sulfit „verzehrt“ den Luftsauerstoff oder gelösten Sauerstoff
Im fertigen Wein ist immer Sauerstoff enthalten. Vor allem gelangt er beim Abfüllen hinein.
Zu viel Sauerstoff wirkt geschmacksverändernd. Einmal werden diejenigen empfindlichen Stoffe oxidiert, denen der Wein seine Aromanoten verdankt.
Hinzu kommt, dass manche der Oxidationsprodukte schlecht schmecken oder riechen. Nichts ist für einen Weinkenner unerwünschter als dieser so genannte „Luftton“ oder „Alterston“.
Deshalb will niemand so richtig das Sulfit vom Wein fernhalten. Denn es fängt den Sauerstoff ab, indem es ihn unter Sulfatbildung bindet.
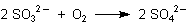
Kann man das Sulfit nicht wenigstens abtrennen?
Die Bestandteile des chemischen Sulfitsystems aus dem Wein zu entfernen, ist kaum möglich. Erschwerend ist,
dass ein Teil des zugefügten Sulfits sofort chemisch gebunden wird - unter anderem im fertigen Wein an
Carbonylverbindungen und Kohlenhydrate. Diese
Additionsverbindungen sind das Produkt von
Gleichgewichtsreaktionen und können das Sulfit leicht
wieder freisetzen.
Man könnte erwägen, SO2 durch Erwärmen oder durch „Strippen“, also durch Einleiten von heißem Wasserdampf, auszutreiben und so auch das Sulfit zu entfernen. Dann gehen dem Wein aber viele flüchtige Aromastoffe und letztlich auch der Alkohol verloren.
Das gilt auch für Membrantechnologien. Bei denen wird Wein durch poröse Röhren geleitet, die mit halbdurchlässigen Membranen ausgelegt sind. Gasförmiges SO2 kann gesteuert durch Druckminderung den Wein verlassen. Aber leider machen das auch andere leicht verdampfende Verbindungen, so dass ein „echt ungenießbares Gesöff“ entsteht. Das schmeckt dann so wie alkoholfreies Bier...
Natürlich kann man chemisch vorgehen, vor allem oxidieren. Das geht zum Beispiel mit Eisen(III)-Verbindungen. Dann hat man jedoch andere geschmacksverändernde Stoffe drin, wie z. B. Eisen(II)-Verbindungen.
Oder wollen Sie es gar mit Iod versuchen? Das kommt wohl kaum jemandem in den Sinn, denn Iod bildet mit Ethanol und anderen organischen Substanzen schon in Spuren nach Krankenhaus riechendes Iodoform - auch wenn keine Laugen dabei sind. Das dauert dann eben etwas länger, riecht aber genauso penetrant. Und das Iodid, das bei der Oxidation von Sulfit entsteht, bringt in zu großen Mengen den Stoffwechsel der Schilddrüse außer Takt.
Fazit
Wer empfindlich gegen Sulfit ist, sollte schlicht weniger Wein oder Bowle trinken. Das ist angesichts des
hohen Alkoholgehalts von 11-12 Vol% (und der ist bei der Bowle noch viel größer) sowieso gesünder.
|
Wasser ist für einen klugen Mann das einzige Getränk |
Rüdiger Blume
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 28. April 2009, Dagmar Wiechoczek