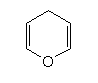
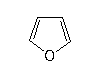
Halbacetalbildung - Furanose oder Pyranose?
Experimenteliste zu den Kohlenhydraten
Immer wenn man ³ber Kohlenhydrate redet, denkt man an Ringstrukturen. Manche machen daran sogar eine Definition des Begriffs äKohlenhydrateō fest: Nur solche Polyhydroxyl-carbonyl-Verbindungen sollten Kohlenhydrate hei▀en, die auch stabile Ringe bilden k÷nnen ¢ also nur die Hexosen und die Pentosen.
Doch liegen Kohlenhydrate nicht zwangslõufig immer in der Ringform vor. Sie stehen vielmehr in einem stetigen Gleichgewicht mit ihrer offenkettigen Form. Dar³ber hinaus gibt es auch noch verschiedene Ringformen, je nach dem, ob f³nf oder sechs Atome an der Bildung des Ringger³sts beteiligt sind: Furanosen und Pyranosen. Die Begriffe stammen von cyclischen Ethern, die entsprechende Strukturen aufweisen.

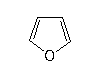
Pyran und Furan
Bildung von intramolekularen Halbacetalen
Kohlenhydrate besitzen sowohl OH- als auch C=O-Gruppen. Eine typische Reaktion von
Carbonylverbindungen und Alkoholen ist die Halbacetalbildung.
Da beide funktionellen Gruppen in einem Molek³l vorhanden sind, kann diese Reaktion auch intramolekular
vonstatten gehen. So bildet sich ein Ring.
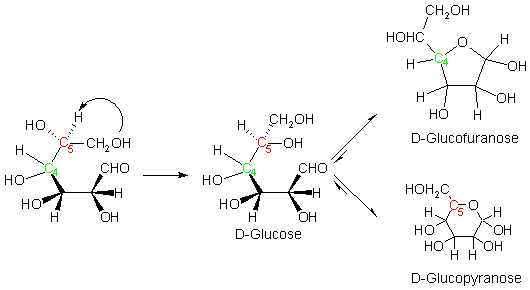
Bei der Reaktion zum cyclischen Halbacetal muss man sich zunõchst in Erinnerung rufen, dass die einzelnen Glieder der offenkettigen Form drehbar sind. Das bedeutet, dass sich bei der Ringbildung zunõchst die einzelnen Glieder um das C5-Atom so lange drehen, bis dessen Hydroxylgruppe in eine Position kommt, in der sie zu der endstõndigen Carbonylgruppe einen m÷glichst geringen Abstand besitzt. Beide reagieren nun in einer Additionsreaktion miteinander und es bildet sich ein sechsgliedriges Halbacetal (Pyranose). Einen F³nfring (Furanose) erhõlt man hingegen, wenn man nicht die an das C5-Atom, sondern die an das C4-Atom gebundene Hydroxylgruppe mit der Carbonylgruppe zur Reaktion bringt.
Welche Ringform wird bevorzugt?
Ob eine Furanose oder eine Pyranose gebildet wird, ist abhõngig vom jeweiligen Kohlenhydrat.
Bei der Glucose ³berwiegt der Anteil der Pyranoseform. Das gleiche gilt f³r die Fructose, wenn
sie sich in L÷sung oder im Kristall befindet. Denn ein Ring aus 6 Atomen garantiert mit seiner
vom Cyclohexan her bekannten Sesselform die spannungsfreiste und
damit energieõrmste Form. Der Anteil der Furanoseform ³berwiegt aber bei der gebundenen Fructose
¢ z. B. in der Saccharose.
Es kann demnach keine einfache Regel aufgestellt werden, ob die eine oder die andere Form
grundsõtzlich bevorzugt wird.
Anomerenbildung - Eine Folge des Ringschlusses und der
Mutarotation
Beim Betrachten des Produkts, das durch den Ringschluss aus der linearen Carboxylverbindung entsteht,
fõllt auf, dass aufgrund der rõumlichen Anordnung der neu gebildeten Hydroxylgruppe am C-Atom 1 zwei weitere
Isomere m÷glich sind. Diese nennt man Anomere. Man bezeichnet sie mit den griechischen Buchstaben
α und β: α-D-Glucose oder β-D-Glucose.
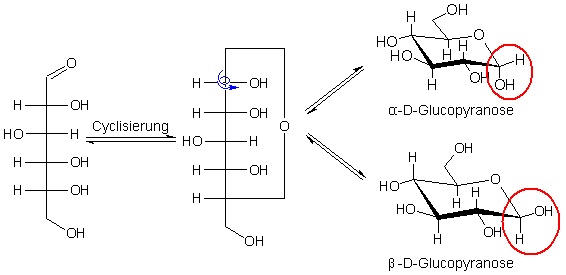
Bildung von Anomeren der D-Glucose
Die gesamte Reaktionsgruppe stellt ein chemisches Gleichgewichtssystem dar. Das hat zur Folge, dass sich auch zwischen den beiden anomeren Formen ein Gleichgewichtszustand einstellt.
Wenn man ein reines a- oder b-Anomeres in L÷sung gibt, stellt sich das Gleichgewicht zwischen den Anomeren spontan, wenn auch ziemlich langsam ein. Die Reaktion kann man durch Zugabe einer schwachen Base wie Soda oder Ammoniak beschleunigen. Denn dadurch wird die Ring÷ffnung gef÷rdert.
Man spricht hier von Mutarotation (lat. mutare, verõndern). Die chemische Reaktion lõsst sich mit Hilfe der Verõnderung der optischen Aktivitõt einer L÷sung verfolgen. Das a-Anomere hat eine spezifische Drehung [a]D = +112,2░, das b-Anomere dagegen nur +18,7░. Das sind auch die Anfangswerte der jeweiligen L÷sungen. Nach Erreichen des Gleichgewichtszustands misst man +52,7░. Das ist ³brigens auch der Drehwert, den man f³r eine Glucosel÷sung tabelliert findet.
Im Fall der Glucose wird die b-Form mit 64 % bevorzugt. Wovon es abhõngt, welche Form sich in erster Linie bildet, erklõren wir in einer anderen Webseite. Hierbei bringen wir auch die reaktionskinetischen Gleichgewichtsberechnungen. Dazu beschreiben wir noch, wie man die reinen Anomere herstellt.
Anomere sind ³brigens Beispiele f³r den Spezialfall der Stereochemie, die Diastereomerie.
Der Vollstõndigkeit halber sei gesagt, dass es von den oben gezeigten anomeren Formen noch weitere Konfigurations-Isomere gibt. Die Sesselform des Rings kann nõmlich umklappen. Im obigen Bild steht dann das C-Atom 1 nach oben, das C-Atom 4 nach unten. Das ist aber nur f³r das Verstõndnis einiger enzymatischer Reaktionen wirklich wichtig.
Weitere Texte zum Thema äKohlenhydrateō