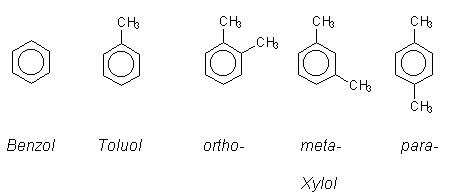
Alkylbenzole - die nächsten Verwandten des Benzols
Neben Benzol kommen noch einige weitere Aromaten im Erdöl vor. Die häufigsten sind das Toluol und die Xylole. Diese drei Verwandten werden auch als BTX-Aromaten zusammengefasst (Benzol, Toluol, Xylole).

Diese Alkylbenzole sind Homologe des Benzols.


Kalottenmodelle von Toluol und m-Xylol
(Fotos: Daggi)
In Verbrennungsmotoren bewirken die BTX-Aromaten wahre
Wunder
Teure Hochleistungskraftstoffe enthalten einen hohen Anteil an Alkylbenzolen. Sie verleihen dem
Kraftstoff eine extrem hohe Klopffestigkeit, da sie keine oder
kaum Wasserstoffradikale beim Erhitzen bilden. Alle BTX-Aromaten besitzen somit sehr hohe Oktanzahlen
(Benzol: 99, Toluol 110, o-Xylol 120, m-Xylol 118, p-Xylol 117). Die Oktanzahl des Formel 1-Benzins
liegt bei etwa 108. BTX-Aromaten katapultierten also auch Michael Schumacher auf seine
Renngeschwindigkeit.
Vorkommen und Darstellung des Toluols
Der Großteil des industriell verwendeten Toluols wird aus den Verfahren der Erdölveredelung (Cracken und Reforming) gewonnen. Ein
besonderes Reforming-Verfahren ist dabei das Platforming. Das Wort kommt von
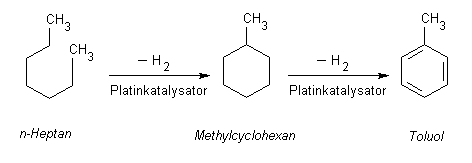
Platin-Reforming. Hierbei werden an kettenförmigen Kohlenwasserstoffen
wie n-Heptan Wasserstoffatome mit Platin als Katalysator abgespalten. Dadurch entstehen zuerst
Cycloalkane, die bei weiterem Entzug von Wasserstoff ein aromatisches π-Elektronensystem ausbilden können.
Auch im Steinkohleteer ist Toluol, wenn auch in geringeren Mengen, enthalten. Entdeckt wurde das Toluol jedoch auf ganz anderem Wege. Es ist nämlich ein Pflanzeninhaltsstoff eines mittel- und südamerikanischen Baumes, dem Tolubalsambaum (Myroxylon balsamum). Hierher hat das Toluol also auch seinen Namen. Aus dessem Harz wurde Toluol durch Destillation gewonnen. Chemisch lässt sich Toluol durch eine Friedel-Crafts-Alkylierung mit Benzol und Chlormethan herstellen.
Verwendung des Toluols
Toluol dient nicht nur als Treibstoffzusatz. Es ist gänzlich unpolar, also ein hervorragendes Lösungsmittel
für ebenfalls unpolare Stoffe. Es ist damit ein guter Ersatz für das giftige und krebserregende Benzol.
So findet man Toluol in vielen Lacken und Druck-Farben. Auch in den Farbpatronen vieler Drucker wird
Toluol mit hoher Wahrscheinlichkeit als Lösungsmittel enthalten sein. In Kunststoffen wird Toluol als
Weichmacher verwendet. Reines Toluol greift allerdings viele Kunststoffe an. Deshalb wird es im Labor
nur in Glasgefäßen aufbewahrt.
Chemisch ist das Toluol Grundsubstanz vieler Synthesen. Durch mehrfache Nitrierung entsteht der Sprengstoff TNT (Trinitrotoluol).
Durch Oxidation an der Seitenkette kann Toluol zu Benzoesäure umgewandelt werden (-> Versuch). Diese ist auch unter der Bezeichnung E210 als Konservierungsmittel zugelassen. In der Natur findet man sie in vielen Früchten.
Hierzu findet man auf der Webseite Reaktionen der Alkylbenzole mehr.
Weitere Texte zum Thema „Kohlenwasserstoffe“