Prof. Blumes Tipp des Monats Oktober 2011 (Tipp-Nr. 172)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Silberkristalle
Wenn man Silber mit einem normalen Reduktionsmittel aus seinen Salzen fällt, gibt es oft nur einen hellgrauen bis schwarzen Niederschlag. Das ist z. B. der Fall, wenn man eine anorganische Substanz wie Hydrochinon oder Ascorbinsäure nimmt.
Beim Experimentieren mit Silbernitrat Gummihandschuhe anziehen und für gute Unterlagen sorgen, da Silbernitrat hässliche Flecken verursacht.
|
Versuch 1: Reduktion von Silbernitratlösungen mit Ascorbinsäure
|
Die Reaktionsgleichung des Redoxprozesses ist:
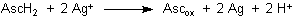
Als ähnlich wirkende Reduktionsmittel (Elektronendonatoren) können auch Zinn(II)-chlorid und andere anorganische Substanzen wie Eisen(II)-sulfat dienen:
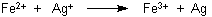
Das Produkt ist feinst verteiltes Silber. Es handelt sich u. a. um amorphes Silber, das noch nicht kristallisiert ist oder im Begriff ist zu kristallisieren. Natürlich sind auch feinste Kriställchen dabei. Alles führt zur Lichtabsorption sowie Totalreflektion und quasi zur Lichtauslöschung (= Schwärzung).
Eine andere schwarze Silberform kennen wir auch von der Schwarz-Weiß-Fotografie. Letztlich ist es ja ein Silberbild, das wir betrachten. Dass es so schwarz ist, rührt hier von den optischen Eigenschaften der fädigen Silberkriställchen her, die beim Entwicklungsprozess aus den Silberbromidkristallen wachsen.
Kann man auch deutlich kristallines Silber herstellen?
Das geht ganz einfach!
|
Versuch 2: Bildung von kristallinem Silber
|
Klick mich an!
Bild 1: Silberabscheidung auf Kupfer.
Links nach einer Stunde. Mitte nach einem Tag. Rechts nach zwei Tagen
(Fotos: Daggi)
Die Silber-Kristalle gehören übrigens der kubischen Kristallklasse an.
Das erkennt man auch sehr gut auf dem vergrößerten Ausschnitt des rechten Bilds oben, das den
Reaktionsverlauf nach zwei Tagen zeigt.

Bild 2: Silberabscheidung auf Kupfer.
Man erkennt durch den voluminösen Niederschlag hindurch die geometrische Anordnung der Silberkristallprismen
(Foto: Daggi)
Der Vorzug des Versuchs ist, dass man aufgrund der Kristallbildung und der Umfärbung der Lösung direkt auf den
Reaktionsablauf schließen kann.
Die den chemischen Vorgang beschreibende Reaktionsgleichung lässt sich deshalb leicht herleiten.
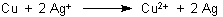
Der Versuch ist auch insofern interessant, als er zeigt, wie große Kristalle auf Kosten von primär entstandenen, kleinen Kriställchen wachsen können. Das ist in vielen Bereichen von Bedeutung, so z. B. bei der Technologie zur katalytischen Abgasreinigung: Hier will man ja besonders feine katalytisch wirkende Metallschichten herstellen, da diese eine besonders große Oberfläche haben, an denen die zu katalysierende Reaktion ablaufen kann. Dabei kämpft man jedoch mit dem Problem, dass sich die feinen Kristalle mehr oder weniger rasch zu groben Kristallen umlagern und so ihre katalytische Wirkung herabgesetzt wird.
Zum Schluss:
Wie man einen blanken Silberspiegel herstellt, zeigen wir hier. Da wird deutlich, dass auch
fein verteiltes Silber metallisch glänzen kann. Das Stichwort ist Inhibition der Kristallisation durch Zusatz bestimmter
Substanzen.
Rüdiger Blume
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 29. September 2011, Dagmar Wiechoczek
