Prof. Blumes Bildungsserver für Chemie
Tipp des Monats September 2017 (Tipp-Nr. 243)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Echt Biologische Waschmittel – selbst gepflückt
Rüdiger Blume
Gegenwärtig blüht in unserer ostwestfälischen Senne-Landschaft (und auch – wie ich gehört habe - in der sandigen Berliner Umgebung) eine wilde Nelken-Art. Die hat einen seltsamen Namen: Gewöhnliches Seifenkraut (Saponaria officinalis). Sie wird merkwürdigerweise auch Echtes Seifenkraut genannt. Dazu kommen Namen wie Seifen- oder Waschwurz. Klick mich an! Bild 1: Gewöhnliches Seifenkraut
Wie die Bezeichnungen schon sagen, enthält diese Pflanze Stoffe, die in ihren Eigenschaften den Seifen oder Tensiden ähneln und mit denen man sogar waschen kann. Der Zusatz officinalis kommt vom lat. officina, Geschäft (mit Bedeutungswandel zu den Begriffen Arztpraxis, Apotheke). Dies ist ein Hinweis darauf, dass man Seifenkraut auch in der Medizin verwendet, in diesem Fall als Hustenschleimlöser – was in gewissen Grenzen letztlich ja auch mit seiner Tensid-Wirkung zusammenhängt. Wohlgemerkt: Die Extrakte vieler Pflanzen schäumen. Ursache dafür sind im Allgemeinen Proteine oder Polysaccharide. Aber manche dieser Pflanzen enthalten als Schaumbildner zusätzlich seifenähnliche Substanzen. Diese Pflanzen hat man früher für die Wäsche genutzt - und macht es heute zunehmend wieder. Der „Promi“ unter den waschaktiven Pflanzen ist das Seifenkraut. Es enthält besonders viel der entsprechenden Seifen-Substanzen – 1 bis 2 Masse%. Besonders viel davon findet man in den ausläuferartigen, sehr harten Wurzelstöcken – 3 bis 5 Masse%. Das mit der Seife wollen wir untersuchen – wobei wir in der häuslichen Küche arbeiten können. Dieses ist ein Beispiel für Jedermanns „Küchen-Chemie“. Versuch 1: Herstellung von Seifenlösung aus Seifenkraut Etwa 10 g Wurzeln und Blätter von einer frischen Seifenkraut-Pflanze werden gut gesäubert und wirklich klein geschnitten. Dann wird der Feinschnitt mit der gleichen Menge an sauberem Sand vermischt. Das Ganze wird mit Hilfe eines Mörsers möglichst fein zerkleinert und mit 100 ml Wasser in ein Becherglas (500 ml) oder in ein anderes hitzebeständiges Glasgefäß eingespült. Das Gefäß wird abgedeckt; das Gemenge wird bis zum Kochen erhitzt und ca. 15 min am Köcheln gehalten. Achtung: Dabei kommt es von Anfang an zu einer starken Schaumbildung! Bild 2: Herstellen von Seifenkraut-Extrakt
Danach lässt man die Mischung bis zum Abkühlen ziehen. Zum Schluss wird in ein Becherglas filtriert. Das Filtrat sollte das vermutete Tensid enthalten.
(Foto: Blume)

(Foto: Blume)
Die Lösung ist wegen des Chlorophylls etwas grünlich gefärbt. Dass sie etwas trübe ist, liegt bereits an einem Tensideffekt: Tenside sind bekanntlich Emulgatoren.
Nun müssen wir prüfen, ob der Pflanzenextrakt sich tatsächlich wie eine Seifenlösung verhält. Aus Vergleichsgründen untersuchen wir parallel Lösungen von handelsüblicher Flüssigseife (w = 1 %) und den selbst hergestelltem Seifenkraut-Extrakt.
|
Versuch 2: Untersuchung des Seifenkraut-Extrakts 2.1 Wir pusten mit einem Trinkhalm in den Seifenkraut-Extrakt.
Bild 3: Schaumbildung bei Seifenkraut-Extrakt
2.2 Wir bedecken den Boden einer flachen Schale mit Wasser und bestreuen (z. B. mit Hilfe eines Teesiebs) die Wasseroberfläche mit feinstem Schwefelpulver (Schwefel-Sublimat, „Schwefelblume“). Statt Schwefelblume können wir auch Talkum oder Ruß (aus dem Ofen gekratzt!) nehmen. Dann tropfen wir etwas Seifenkraut-Extrakt auf die Oberfläche.
Bild 4: Ruß auf Wasser (links) und Wirkung des Seifenkraut-Extrakts (rechts)
2.3 Wir füllen in ein Reagenzglas etwa 5 ml Seifenkraut-Extrakt und halb so viel Pflanzenöl. Wir verschließen das Glas mit dem Daumen und schütteln kräftig.
Bild 5: Links der reine Seifenkraut-Extrakt; rechts Emulsionsbildung nach Zugabe von Pflanzenöl
|
Die Versuchsergebnisse sind allesamt Hinweise auf das Vorliegen von seifenartigen Substanzen, also von polaren Stoffen, die die Oberflächenspannung des Wassers beeinflussen - daher die Bezeichnung Tenside (lat. tentigo, Spannung; oder lat. tensus, gespannt).
Nun können wir die Ergebnisse von Versuch 2 erklären:
2.1 Die Schaumbildung beim Reinpusten resultiert aus der Tendenz zur Oberflächenvergrößerung. Hierbei versuchen die Tensid-Moleküle, Oberflächen zu besetzen. Wenn die gebotene Oberfläche nicht ausreicht, schaffen sich die Moleküle selbst eine – die Schaumblasen haben sogar eine Innen- und Außenfläche. Dazwischen befindet sich ein dünner Wasserfilm.
2.2 Bei der Besetzung von Oberflächen entwickeln die Moleküle eine bemerkenswerte Kraft – sie schieben deshalb Gegenstände, die auf dem Wasser schwimmen, einfach beiseite.
2.3 Emulsionen entstehen, indem die lipophile Seite der Tensid-Moleküle ins Fett, die hydrophile Seite dagegen ins Wasser ragt. Auch hier gilt wie bei der Schaumbildung: Es muss eine möglichst große Oberfläche geschaffen werden. Das bedeutet, dass aus der Fettschicht eine Unmenge Fett-Tröpfchen gebildet wird – mit der Folge einer starken Oberflächenvergrößerung.
Etwas zur Chemie des Tensids im Seifenkraut
Es handelt sich um Saponine (lat. sapo; Seife). Saponine sind Abkömmlinge der zyklischen Terpene; hier handelt es sich um ein 5-Ring-Terpen. Ein typisches Beispiel aus der vielfältigen Saponin-Gruppe des Seifenkrauts ist das Gypsogenin.
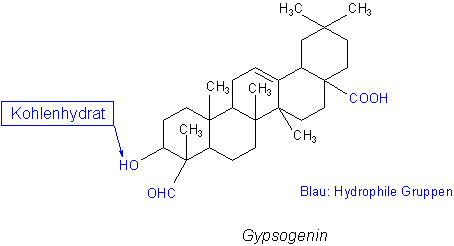
Gypsogenin ist eine stark polare Substanz. Die hydrophilen Gruppen sind diametral angeordnet. Dazwischen befindet sich ein großflächiger lipophiler Bereich. Die kompliziert gebaute Verbindung liegt dazu noch als O-Glykosid vor, also als Verbindung mit Kohlenhydraten. Der Kohlenhydratrest verstärkt die Löslichkeit. (Glykoside spielen auch eine Rolle bei anderen Naturstoffen wie beispielsweise Cumarin, dem Duftstoff des Waldmeisters, dem Kirschlorbeer-Gift Amygdalin oder den Blütenfarbstoffen, den Anthocyanen.)
Letztlich handelt es sich beim Gypsogenin um eine aliphatische Carbonsäure, die ein anionisches Tensid bilden kann. Denn die Carboxylgruppe liegt im neutralen bzw. im schwach basischen Milieu weitgehend als Carboxylat-Anion vor:
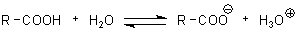
Damit ist Gypsogenin eine Seife im klassischen Sinne. Sie ist sogar eine besonders wirksame Seife: Bei der Besetzung einer Grenzfläche z. B. zwischen Wasser und Fett bzw. Wasser und Luft ragen die beiden diametralen hydrophilen Reste in die wässrige Phase. Die lipophile (also hydrophobe) Mittelfläche stellt den Kontakt zur lipophilen Phase her – wozu auch die Luft gehört.
In diesem Zusammenhang sei an eine andere Gruppe wichtiger biogener Emulgatoren erinnert, die ebenfalls zur Gruppe der zyklischen Terpene gehören, an die Chol- oder Gallensäuren.
Bleibt noch die Frage, zu welchem Zweck das Seifenkraut Gypsogenin produziert – und das dazu noch in so großen Mengen. Offenbar schützt es sich damit vor Fressfeinden.
Ein Hinweis zum Schluss
Auch wenn der Extrakt von Seifenkraut in der alternativen Medizin als Hustenlöser genutzt wird, muss darauf hingewiesen werden, dass zu viel davon hinsichtlich Beeinflussungen des Verdauungstrakts und auch Blutveränderung durchaus toxisch wirken kann. (Das gilt für alle Saponine.) Aber wer trinkt schon Waschmittel – auch wenn sie selbstgemacht und sogar „Bio“ sind…
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 27. August 2017, Fritz Meiners



