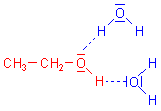
Die Molek³lstruktur des Wassers beeinflusst dessen stoffliche
Eigenschaften
Experimente:
Versuch: Umwandlungstemperaturen von Wasser
Versuch: Wasser als L÷semittel f³r Lebensmittel und anderes
Versuch: Sp³lmittel beeinflussen die Oberflõchenspannung von Wasser
Versuch: Wasser benetzt Oberflõchen
Versuch: Luft l÷st sich in Wasser
Versuch: ųl verschmutzt Wasser
Versuch: Volumenzunahme beim Gefrieren von Wasser
Versuch: Fl³ssigkeiten ben÷tigen beim Verdampfen Wõrme
Ein alter Lehrerschnack besagt: "Wasser ist nass und gewinkelt". Dahinter steckt
Wahres.
Auf all den Eigenschaften der Wassermolek³le und des Wassers als chemischen Stoff beruhen viele f³r das Leben oftmals segensreiche Effekte, die die Anwesenheit von Wasser zur Voraussetzung haben.
A Energetische Auswirkungen der Wasserstoffbr³cken-Bindungen
Wasserstoffbr³ckenbindungen haben eine Bindungsenergie von 15-40 kJ/mol. Das sind etwa
3 bis 5 % der Energie der kovalenten Bindung zwischen H und O (463 kJ/mol). Wasser hat deshalb
f³r eine Substanz, die aus sehr kleinen Molek³len aufgebaut ist, verglichen mit anderen
õhnlich aufgebauten Verbindungen wie Schwefelswasserstoff H2S, Ammoniak NH3
oder Methan CH4 extrem hohe Schmelz- und Siedetemperaturen und einen weiten Fl³ssigbereich
(-> Versuch und die Webseite "Ein
Blick ins PSE: Wenn Wasser wirklich nur H2O wõre"). Die damit verbundenen gro▀en Umwandlungswõrmen
werden beim Wechsel der Aggregatzustõnde im Wasser gespeichert oder bei der Umwandlung freigesetzt.
| Umwandlungsenthalpien und Wõrmekapazitõten | ||||
| Wasser | Schwefelwasserstoff | Ammoniak | Methan | |
| Schmelzwõrme kJ/mol | 6,00 | 2,38 | 5,65 | 0,94 |
| Verdampfungswõrme kJ/mol | 40,75 | 18,67 | 23,35 | 8,26 |
| Spezifische Wõrme J/K · mol | 75,15 | - | 35,52 | - |
Wegen des Aufbaus aus dreiatomigen gut schwingungsfõhigen Dipol-Molek³len weist Wasser in allen drei
Aggregatzustõnden eine sehr gro▀e Wõrmekapazitõt auf.
Aus diesen beiden Gr³nden ist Wasser ein sehr guter Energieabsorber und
ein sehr gutes Energietransportmedium, also auch ein Temperaturpuffer.
B Grenzflõchen und Flie▀verhalten
Wasser benetzt polare Oberflõchen. An der Grenze zu nicht benetzbaren Oberflõchen
wie Metall oder der Luft besitzt Wasser eine gro▀e Oberflõchen- oder Grenzflõchenspannung
(-> Versuch). Das r³hrt daher, weil die Molek³le des Wassers
durch Wasserstoffbr³cken vor allem an der Grenzschicht stark gebunden zusammenhõngen.
Weil die Wassermolek³le untereinander so stark gebunden sind, hat Wasser
verglichen mit anderen Fl³ssigkeiten eine hohe Viskositõt.
C Wasser als L÷semittel
Wasserstoffbr³cken-Bindungen werden auch zu anderen polaren Stoffen wie
Alkoholen oder Kohlenhydraten aufgebaut.

Zwischen Ionen und Wassermolek³len gibt es starke elektrostatische Wechselwirkungen.
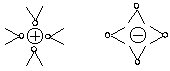
Wasserdipole umgeben in oktaedrischer Symmetrie die Ionen von NaCl.
(Die zwei au▀erhalb der Zeichenebene angeordneten Wasserdipole muss man sich dazu denken.)
Wasser ist deshalb ein hervorragendes L÷semittel gerade f³r polare Stoffe wie Salze
und die meisten Lebensmittel (-> Versuch).
Darauf beruht auch die Benetzung von polaren Oberflõchen und das nasse Gef³hl gegen³ber
Wasser (-> Versuch).
Makromolekulare Lebensmittel wie Stõrke oder Proteine quellen manchmal nur,
werden damit aber dem Angriff durch Verdauungsenzyme zugõnglich gemacht.
Aber auch weniger polare Gase l÷sen sich hervorragend in Wasser
(-> Versuch). Die Luft enthõlt Sauerstoff und Stickstoff
im Verhõltnis 1:4, Wasser dagegen 1:1,8. Deshalb k÷nnen Fische und andere Kiementiere
im Wasser atmen. Andere Gase reagieren mit Wasser weiter zu Sõuren. Darauf beruht der
saure Regen, aber auch die Ausgewogenheit der CO2-Bilanz der Atmosphõre
durch die Adsorptionskraft der Weltmeere.
Leider l÷sen sich aber auch v÷llig unpolare Stoffe wie L÷semittel (CKW), Diesel÷l oder Pestizide im Wasser,
wenn auch nur in Spuren (-> Versuch). Dabei werden die unpolaren Molek³le
mit Netzstrukturen aus Wassermolek³len umh³llt. Hier berichten wir dar³ber,
weshalb zum Beispiel Dieselkraftstoff wassergefõhrdend ist, obwohl er sich nach Meinung vieler Leute und Nachschlagewerke
gar nicht mit Wasser vermischt.
Fl³ssiges Wasser bildet auf diese Weise unter Druck eisartige Einschlussverbindungen mit Gasen, die so genannten Clathrate. Der Einschluss von Methan ist f³r uns besonders wichtig, denn er kann sich als die bedeutendste Quelle f³r Erdgas herausstellen und so vielleicht zu unserer Energieversorgung beitragen.
Obwohl fl³ssiges Wasser ein so gutes L÷semittel ist, bildet Eis normalerweise keine Mischkristalle. Auch aus Salzl÷sungen wie dem Meerwasser kristallisiert deshalb immer reines Wassereis aus. Es kann in seinen Gitterzwischenrõumen h÷chstens Gase einlagern.
D Die Struktur von Wassereis
Beim Gefrieren von Wasser bildet sich Eis, dessen Volumen um 1/11 oder 9 % gr÷▀er
ist als das von fl³ssigem Wasser (-> Versuch).
Dabei gruppieren sich die Wassermolek³le so, dass sie sehr viel Raum einnehmen. Eis bildet in seinen
Kristallen Sechsringe.
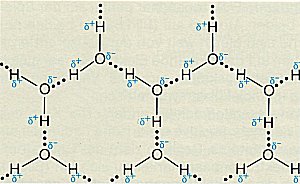
Zweidimensionale Struktur von Eis bei Normaldruck (Quelle: Cornelsen)
Die Ausbildung von Wasserstoffbr³cken in Wassereis.
Die vierte Bindung, die jeweils von den Sauerstoffatomen ausgeht, ist nicht gezeichnet.
Das Bild zeigt, dass die Elementarzelle eine sperrige hexagonale Struktur aufweist. (Damit erinnert
das Eisgitter an die Gitterstruktur des Quarzes.) Diese Struktur
spiegelt sich in den sechseckigen Schneesternen wieder. Dies ist ein sch÷nes Beispiel
daf³r, wie die Struktur im Bereich der kleinsten Teilchen die des Stoffes bestimmt.
Eine dreidimensionale Darstellung des Wassereis-Gitters sowie Bilder von Schneekristallen zeigen wir auf der Webseite zum Wassereis.
E Volumenverõnderungen beim Abk³hlen und Erwõrmen von Wasser
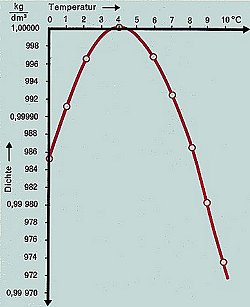
(Quelle: Cornelsen)
Beim Abk³hlen verhõlt sich Wasser anomal. Normalerweise nimmt beim Abk³hlen bei
allen bekannten Fl³ssigkeiten deren Volumen ab. Das beobachten wir zunõchst auch
beim fl³ssigen Wasser, um bei 4 ░C eine ▄berraschung zu erleben: Bei weiterem
Abk³hlen nimmt das Volumen wieder zu, die Dichte also ab. Denn das Volumen von
fl³ssigem Wasser hat also bei 4 ░C ein Minimum und nimmt danach wieder zu. Man
spricht von der Dichte-Anomalie des Wassers. Der Grund ist, dass sich bei dieser
Temperatur die Wassermolek³le zu sperrigen Strukturen zu ordnen beginnen, die in
die volumin÷sere Struktur von Eis m³nden.
Die Temperatur von Wasser bestimmt also dessen Dichte. Das gilt aber auch
umgekehrt: Unter hohem Druck (ab etwa 1,2 m Wassertiefe) bleibt die Temperatur des
Wassers bei 4 ░C stehen. Sie kann nicht steigen oder niedriger werden, denn das
w³rde immer eine Volumenzunahme zur Folge haben m³ssen.
Beim Erwõrmen nimmt im normalen Bereich der Volumen-Temperaturkurve des Wassers das Volumen zu. Das hat erhebliche Konsequenzen f³r die Auswirkungen des Treibhauseffekts. Denn bei Erwõrmung um 1 ░C steigt die Wasserh÷he der Meere weltweit um ca. 30 cm. Das scheint bei einer durchschnittlichen Wassertiefe von 1500 m nicht viel zu sein, hat aber Konsequenzen f³r viele Staaten. Das beschreiben wir in einer besonderen Webseite.
F Chemische Eigenschaften von Wasser
Wasser ist als Endprodukt einer stark exothermen Redoxreaktion ("Knallgasreaktion")
erstaunlich inert und reagiert in biologischem Milieu kaum mit anderen Substanzen, es
sei denn unter Mitwirkung von Katalysatoren (Enzymen).
Aufgrund seines polaren Molek³lbaus sind im Wassermolek³l die Bindungen zwischen
O und H gelockert. Deshalb bildet Wasser in gewissem Umfang Protonen, ist also eine
schwache Sõure. Es kann aber auch Protonen aufnehmen, also als schwache Base wirken.
Wasser ist somit zugleich Sõure und Base. Es ist also
amphoter. Damit kann es andere Sõuren und Basen abpuffern.
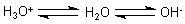
G Die Farbe von Wasser
Da Wasser kaum Licht absorbiert, erscheint es farblos, also sprichw÷rtlich "wasserklar".
Allerdings gibt es eine kleine Einschrõnkung, die zur blaugr³nen Farbe
dichter Wasserschichten f³hrt.
H Wasser absorbiert Infrarot-Strahlung
Die Wassermolek³le sind in sich hervorragend schwingungsfõhig. Darauf beruht ihre
starke Absorptionsfõhigkeit f³r IR-Strahlung. Das hat Folgen f³r das Klima
und f³r den Grund-Treibhauseffekt, der unseren Planeten Erde ³berhaupt bewohnbar macht.
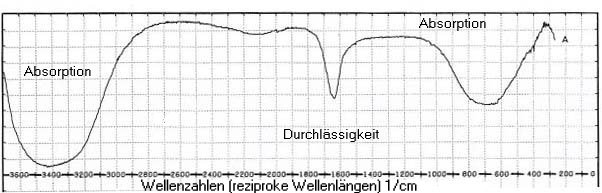 |
| Infrarotspektrum des Wassers |
Weitere Texte zum Thema äWasserō