 |
 |
 |
 |
| Kurze Fragen - Kurze Antworten
Aus dem E-Mail-Korb von Professor Blume |
2086
F: In einem Werk zum Klausur-Training für das Chemie-Abi wird behauptet, dass eine Aminosäure
als Zwitter-Ion (somit am Isoelektrischen Punkt) Pufferwirkung zeige. Das widerspricht aber den Aussagen in den Lehrbüchern und der
Titrationskurve des Glycins, die man auf Ihren Seiten finden kann. Können Sie mir da bitte Klärung verschaffen?
A: Sie haben Recht. Direkt am Isoelektrischen Punkt (IEP)
ist die Pufferwirkung der Aminosäure ausgereizt. Jede Änderung des Zwitter-Ion-Systems durch Zugabe einer Lauge/Base (betrifft R-NH3+)
bzw. einer Säure (betrifft R-COO-) hat eine starke Änderung des pH-Werts zur Folge, also das Gegenteil einer Pufferung.
Am höchsten ist die Puffer-Wirkung der Aminosäure in den Bereichen um die pH-Werte, die den pKa-Werten entsprechen. Das
kann man auch anhand der Steigungen der Titrationskurven festmachen.
2087
F: Bei meiner Recherche für meine Seminararbeit über "Die Farben rund ums Hühnerei" bin ich auf
eine Frage gestoßen.
In dem Text steht, dass es im Verlauf der Lagerung des Hühnerfutters zu Aktivitätsverlusten der Carotinoiden kommt. Der Grund hierfür
ist, dass Carotinoide sehr oxidationsempfindlich sind. Was genau passiert bei dieser Oxidation und wie kann man das mit Hilfe einer
Reaktionsgleichung darstellen. Über eine Antwort wäre ich wirklich sehr erfreut!
Mit freundlichen Grüßen
Renate Kitzinger
A: Carotine sind tatsächlich stark oxidationsempfindlich. Es bilden sich zunächst durch radikalische
Reaktionen Hydroperoxide. Von denen aus können einmal Vernetzungsprozesse zu anderen Molekülen ablaufen. Sie können aber auch die Doppelbindungen
spalten, wobei zunächst Aldehyde und dann Carbonsäuren entstehen. Das läuft so ähnlich ab wie die Autoxidation
von ungesättigten Fettsäuren.
2088
F: Nachdem wir letztens beim großen Wohnungsputz über den Hinweis "Nicht mit anderen Reinigungsmitteln
verwenden!" gestolpert sind, entbrannte zwischen mir und meinem Bruder ein kleiner Disput. Nachdem wir beide keine Chemiker sind (aber gerne
recht haben) und eine direkte Recherche im Internet leider erfolglos blieb, würden wir uns freuen, wenn Sie uns eine Antwort diesbezüglich
geben könnten.
Nach anfänglicher Recherche bezüglich des Hintergrunds des Hinweises (Bildung von Chlorgas) kamen wir nämlich zu der Frage: "Nur" Verwenden, oder Mischen? Dass beim Mischen eine deutliche Reaktion zu beobachten ist, ist evident. Die Frage ist nun: Reicht es aus, beide Flüssigkeiten getrennt von einander, aber "offen" (d.h. beide Flüssigkeiten teilen sich die Luft der Umgebung) zu lagern, um (toxisches) Chlorgas zu erhalten?
Ich behaupte, dass ein Nominalanteil tatsächlich reagieren würde (wenn auch so gering, dass dieser vernachlässigbar wäre?). Mein Bruder hält dagegen und meint, bei dem Übergang des Chlorreinigers in den gasförmigen Zustand (quasi das was man riecht) bereits zerfallen ist und eine Reaktion mit Chlor als Ergebnis nicht mehr möglich wäre. Wer hat Recht?
A: Zum so genannten Domestosproblem haben wir eine Webseite.
Die Reaktion ist letztlich diese:
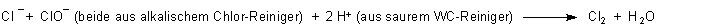
Bei den Reaktanden handelt es sich um nicht verdampfende Ionen. Auf dem Luftweg können sie deshalb sich nicht treffen oder zueinander
wandern. Was Sie beim alkalischen Chlor-Reiniger riechen, sind Spuren von Chlorgas, denn es handelt sich bei dieser Lösung um ein chemisches
Gleichgewichtssystem.
Sie müssen die Lösungen schon mischen, damit eine Reaktion eintritt.
2089
F: Mein Name ist (…), bin 14 Jahre alt und eine Schülerin des (…)-Gymnasiums in (…), 8. Klasse. Im
Fach Naturwissenschaft und Technik möchte ich ein Referat halten im Bereich Chemie Farbe und Licht über Glühwürmchen. Bei meinen Recherchen
bin ich auf die Tipps von Prof. Blume gestoßen und den Beitrag für August 2013. Dort wird erwähnt, dass man Leuchtkäfer gepulvert mit ATP
zum Leuchten bringen kann. Diesen Versuch würde ich gerne in mein Referat einbauen. Daher stellt sich für mich die Frage: Wo kann man
gepulverte Leuchtkäfer und ATP erwerben.
Über eine baldige Antwort würde ich mich sehr freuen, da ich mein Referat schon nächste Wochen halten werde.
A: Du meinst diesen Tipp des Monats.
Die Zutaten zu beschaffen ist nicht so einfach, da nur biochemische Spezialfirmen damit handeln. Außerdem sind die Chemikalien sehr teuer - so um die 100 € pro Gramm. Wenn du die Chemikalien hast, musst du noch genaue Versuchsvorschriften einhalten - wie z. B. den pH-Wert, die Konzentrationen, Temperatur und so weiter. Deswegen habe ich auch auf Vorschläge zu Experimenten verzichtet. Führe stattdessen (wie ich im Tipp vorschlage) den Luminolversuch vor.
Dabei wird dir dein Chemielehrer helfen können. Bei diesem Versuch ist alles analog zum Leuchtkäfersystem. Statt Luciferin Luminol, als Katalysator Rotes Blutlaugensalz statt Luciferase und als Oxidationsmittel Wasserstoffperoxid anstelle von Sauerstoff.
2090
F: Gerne lese ich Ihre informativen Beiträge. Vor kurzem bin ich auf ihren alten Artikel:
http://www.chemieunterricht.de/dc2/tip/07_99.htm gestoßen und habe mich gefragt, welche Verbindung
von Aminosäure und Glucose zu einem Röstgeruch wie bei frischen Kaffee führt. Sofern diese existiert wäre ich Ihnen sehr dankbar, Sie
könnten mir diese mitteilen.
A: Der Geruch nach frischem Kaffee beruht nicht auf Produkten von Maillard-Reaktionen, sondern
auf Schwefelverbindungen. Deshalb erinnert viele Leute der Geruch, der beim Öffnen einer Packung frisch gemahlenen Kaffees frei wird,
an „verliebten Kater“. Am Kaffeearoma sind übrigens um die 500 Verbindungen beteiligt.