Brennbare Stoffe und Brennstoffe
I. Entzünden und Löschen brennbarer Stoffe
II. Brennstoffe
III. Energieumwandlung und Umweltbelastung
I. Entzünden und Löschen brennbarer Stoffe
Brennbare Stoffe kommen in unterschiedlichen Aggregatzuständen vor.
So lassen sich einige Feststoffe (z. B. Wachs, Papier und Streichholzköpfe),
Flüssigkeiten (z. B. Spiritus, Petroleum und Benzin) und Gase (z. B. Erdgas,
Feuerzeuggas und Campinggas) entzünden. Um diese Stoffe zu entzünden,
brauchen sie Luft und eine bestimmte Temperatur, die Entzündungstemperatur,
die für jeden Stoff unterschiedlich ist. Bei Erreichen der Entzündungstemperatur
bilden die brennbaren Stoffe (mit Ausnahme der brennbaren Gase) Dämpfe, die dann mit
der Luft entflammbare Gemische bilden. Die niedrigste Temperatur, bei der ein solches Gemisch
entflammt, bezeichnet man als Flammpunkt. Er kann durch eine offene Flamme, einen
elektrischen Funken oder einen besonders heißen Gegenstand als Zündquelle
ausgelöst werden.
Verbrennungsvorgänge sind Oxidationsreaktionen mit Luftsauerstoff und
verlaufen immer exotherm. Die entstehende Energie wird zum größten Teil in Form
von Wärme frei, die zur weiteren Bildung von Dämpfen führt und somit den
Verbrennungsvorgang unterhält.
Versuche:
Untersuchen von Brennstoffen auf die Elemente Kohlenstoff und Wasserstoff
Nachweis von Kohlenstoff in Grillkohle
Untersuchen der Flammpunkte verschiedener Brennstoffe
Friteusenbrand (Modellversuch)
Bau einer Öl- und Petroleumlampe
Wirkung eines Ölbrenners in der Ölheizung (Modellversuch)
Identifizieren von Camping-Gas durch quantitative Verbrennung
Dichtebestimmung eines Gases am Beispiel von Feuerzeuggas
Explosionsbereich eines Benzin-Luft-Gemisches
Aus diesen Bedingungen für Verbrennungsvorgänge lassen sich zwei grundlegende Maßnahmen zur Brandbekämpfung ableiten. Zum einen können die brennenden Stoffe bis unter ihre Entzündungstemperatur abgekühlt werden. Dies geschieht häufig durch Löschen mit Wasser, eine Maßnahme, die bei feuergefährlichen Flüssigkeiten nicht angewendet werden sollte, da sie häufig nicht mit Wasser mischbar sind. Solche Flüssigkeiten brennen dann auf der Wasseroberfläche unter Bildung gefährlicher Stichflammen weiter. Brände können aber auch durch Verhinderung einer weiteren Luftzufuhr zum Feuer gelöscht werden. Dieses Ersticken des Brandes wird häufig mit Schaum- oder Pulverlöschern und im Fall kleinerer Brände mit Hilfe von Decken, Sand oder Erde durchgeführt. Zur Brandvorsorge wird z. B. Holz mit luftundurchlässigen Stoffen überzogen.
Versuche:
Bau eines Kohlendioxid-Schaumlöschers (Modellversuch)
Wirkung von Wasserglas als Flammschutzmittel
II. Brennstoffe
Brennstoffe bezeichnen brennbare Stoffe, die zur Energieumwandlung herangezogen werden.
Weltweit wird der Energiebedarf zu einem großen Teil durch Verbrennungsreaktionen gedeckt,
weshalb geeignete Brennstoffe ohne großen Aufwand herstellbar und in großen Mengen
verfügbar sein müssen. Weiterhin müssen sie unter Freisetzung von viel Wärme
verbrennen und dabei vor allem Gase und nur wenig feste Verbrennungsprodukte bilden.
Auf viele organische Stoffe, deren Moleküle aus den Elementen Kohlenstoff und
Wasserstoff aufgebaut sind, treffen diese Bedingungen zu. Diese fossilen Brennstoffe sind
in den Vielstoffgemischen Kohle, Erdöl und Erdgas enthalten und
verbrennen überwiegend zu Kohlendioxid (CO2) und Wasser(dampf).
Angesichts immer knapper werdender Ressourcen fossiler Brennstoffe, versucht man zur Deckung des zukünftigen Energiebedarfs die Nutzung regenerativer Energieträger (z. B. Pflanzenöle) stärker einzubeziehen.
Versuche:
Fraktionierte Destillation von Erdöl
Cracken von Edöldestillaten (Modellversuch)
Herstellen von Stadtgas (Modellversuch)
Unterschiede beim Entgasen von Stein-, Braun- und Holzkohle
III. Energieumwandlung und Umweltbelastung
Die Moleküle fossiler Brennstoffe enthalten neben Kohlenstoff und Wasserstoff
auch geringe Anteile weiterer Elemente, wie Stickstoff und Schwefel. Aus diesem Grund
enthalten die Abgase fossiler Brennstoffe eine Reihe von Luftschadstoffen, die
Oxidationsprodukte dieser Elemente sind. Hierzu gehören die Stickstoffoxide
(Stickstoffmonoxid und Stickstoffdioxid) und das Schwefeldioxid. Durch unvollständige
Verbrennung von Kohlenstoff entsteht zudem giftiges Kohlenmonoxid.
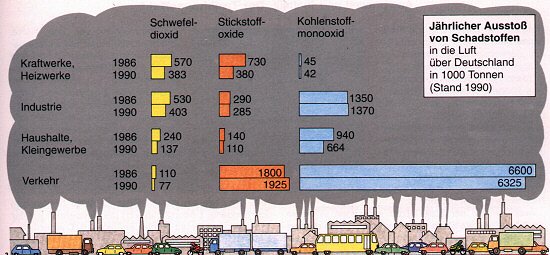
Wer diese Emissionen von Luftschadstoffen verursacht, zeigt folgende Abbildung:

(Quelle: Cornelsen)
Versuch:
Modellversuch zum sauren Regen
Modellversuch zur Kohleentgasung und Nachweis von Aromaten im Kondensat
In Kraftwerken und Industriebetrieben werden inzwischen Verfahren zur Reinigung der Abgase und damit zur Reinhaltung der Luft angewendet.
| Abgasreinigung: Informationen und Versuche |
Bei der Verbrennung von Biomasse, wie z. B. Holz, ist die Luftbelastung erheblich, da in Pflanzen mehr Stickstoff und Schwefel gebunden sind als in Erdgas oder Erdöl. Deshalb ist die Menge an entstehenden Stickstoff- und Schwefeloxiden größer. Außerdem entsteht ein großer Teil an Kondensaten und Teer, die giftige und zum Teil krebserregende Stoffe enthalten.
Versuch:
Trockene Destillation von Holz und Nachweis der Kondensat-Bestandteile
Ein weiterer Luftschadstoff in der Troposphäre (der erdnächsten Luftschicht der Atmosphäre) ist das Ozon. Bei direkter Einwirkung auf Lebewesen wirkt es als Schadstoff. Es entsteht unter Einwirkung von Sonnenstrahlen und katalytisch wirkenden Stickstoffoxiden der Abgase.
| Ozon: Informationen und Versuche |
Weitere Texte zum Thema „Chemie im und ums Haus“