Prof. Blumes Tipp des Monats Mai 2008 (Tipp-Nr. 131)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Allerlei ums Lichtmachen
Aus gutem Grund fürchtet man die Dunkelheit: Denn da waren früher die Raubtiere unterwegs; heute sind es eher die bösen Buben.
Auf der Erde ist Licht also etwas, was man stets benötigt. Denn die Erde dreht sich nicht nur einmal im Jahr um die Sonne, sondern einmal in 24 Stunden um sich selbst. Dadurch befindet sich immer eine Hälfte der Menschheit für einen halben Tag („nachts“) in Dunkelheit. Aber auch tagsüber ist es finster - in Höhlen und Kellern.
Die „Herstellung von Licht“ ist eine lehrreiche Geschichte, mit der man vieles aus Chemie, Physik und sogar auch aus der Biologie lernen kann. Es handelt sich um ein wahrhaft fächerübergreifendes Thema, das dazu noch den oft vermissten Alltagsbezug aufweist.
Vorneweg
Licht entsteht immer als ein Produkt von Energieumwandlungen: Eine potentielle
Energie wird umgewandelt in andere Energieformen wie Licht. Meistens ist damit
auch die Freisetzung von Wärme verbunden. Dass auch das Licht
tatsächlich eine Energieform ist, kann man leicht zeigen. (Klicke
hier.)
Am Anfang leuchtete das offene Feuer
Früher griff man zur Beleuchtung auf offene Flammen
wie Lagerfeuer, Fackeln oder Öllampen zurück.

Bild 1 (Foto: Blume)
Dazu kamen dann noch die Kerzen oder Petroleumlampen. Zur Voraussetzung für all das brauchte man die Kunst des Feuermachens. Die Entdeckung des Phosphors war nur eine Randerscheinung auf der Suche nach Licht…
Auf welchen chemischen Tatsachen beruht Feuer? Die chemische Energie des Brennstoffs wird in Gegenwart eines Oxidationsmittels wie Sauerstoff in die Energieformen Wärme und Licht umgewandelt.
So blieb es über Tausende von Jahren.
Glühlampen
Schließlich kam es im 19. Jahrhundert zur Nutzbarmachung des elektrischen Stroms. Dessen
Randerscheinungen - Hitze und Glühen - führte direkt zur Erfindung der Glühlampe. Das war nichts
anderes als ein Glühfaden, eingeschlossen in ein luftdichtes, evakuiertes („luftleeres“) birnenförmiges Glasgefäß.
(Daher rührt die Bezeichnung „Glühbirne“, was aber die Techniker nicht so gern hören…)
Das Licht entsteht dadurch, dass elektrische Ladungen durch einen Leiter wandern. Dabei wird elektrische Energie zum Teil in Wärme umgewandelt. Das Aufheizen kann so weit gehen, dass der Draht zu glühen beginnt. Die Atome werden angeregt, geben Elektronen ab und nehmen wieder welche auf. Dabei senden sie Licht aus. Das Licht ist umso heller, je heißer der Faden ist.
Das Fernhalten der Luft war ganz besonders wichtig: Denn glühendes Material hat die Eigenschaft, sich sofort mit Luftsauerstoff zu verbinden, also zu verbrennen. Man hätte natürlich auch ein anderes Gas einfüllen können – aber die Edelgase gab es zunächst noch nicht. Stickstoff war noch nicht rein genug und enthielt zuviel Sauerstoff.

Bild 2: Glühlampe mit Glühfaden
(Foto: Blume)
(Wie fotografiert man überhaupt einen Glühfaden? Man sorgt für genügend Umgebungslicht - stellt z. B. die Lampe in helles Sonnenlicht.)
Kohlefaserlampen
Der Glühfaden war zunächst ein Kohlefaden, erhalten durch Ausglühen eines Fadens aus Bambus und anderem
pflanzlichen Fasermaterial. Genau genommen war das kein Kohlefaden, sondern ein Graphitfaden, denn er muss
ja den elektrischen Strom leiten. Letztlich ist das das gleiche wie heute eine Kohlefaser, die bei
den modernen Verbundstoffen eine so große Rolle spielt. Die freien
Fasern waren aber mechanisch sehr anfällig. Solche Glühlampen brannten rasch durch. Deshalb kam es bald zur Einführung
von metallischen Glühfäden.
Glühfäden aus Metall
Als es dann gelang, Glühfäden aus dem besonders hochschmelzenden Wolfram (Schmelztemperatur
3410 °C) herzustellen, war das Leuchtglück schon fast perfekt. Man konnte die Glühlampen größer bauen und die Entwicklung von
mehr Hitze erlauben. Die Lichtausbeute war folglich beträchtlich. Übrigens verwendete man auch das Platinmetall
Osmium (Schmelztemperatur 3050 °C). Daran wird man beim Firmennamen „Osram“ erinnert: Das Wort
ist aus Osmium und Wolfram zusammengesetzt.
Hier noch eine Begriffsklärung: In der Autotechnik kennt man vor allem das Bilux-System. Der Name beschreibt die Lampenkonstruktion. Es gibt in der Glühlampe zwei Glühfäden: Einen für Fern- und einen für Abblendlicht.
|
Versuch 1: Analyse eines Metallfadens aus einer Glühlampe
Die Fäden werden mit Hilfe einer oxidierenden Schmelze zersetzt. Dazu werden sie mit Kaliumhydroxid und Kaliumnitrat vermischt. Diese Mischung wird erhitzt (am besten in einem abgedeckten Platintiegel). Man lässt abkühlen und löst den Schmelzkuchen in wenig Wasser. Gegebenenfalls wird filtriert. Dann gibt man Zink in Form einer Granalie oder als frisches Pulver hinzu und säuert vorsichtig mit verdünnter Salzsäure an. Den pH-Wert prüfen! Es stellt sich langsam eine Blaufärbung ein, die auf das Vorliegen von Wolfram hinweist. Als Reduktionsmittel kann man auch Zinn(II)-chlorid oder Ascorbinsäure verwenden. |
Zur Erklärung der chemischen Abläufe sollte man sich an den Reaktionen von Chrom orientieren, denn im PSE findet man Wolfram in der Chromgruppe.
Hier ist ein formales Reaktionsschema für die Reaktionen von Wolfram. Zunächst bildet sich aus dem Metall durch Oxidation Wolframtrioxid(VI).
W + 3 [O] ———> WO3
Dieses wird mit KOH zu Wolframat(VI) umgesetzt.
WO3 + 2 KOH ———> K2WO4 + H2O
Wolframat(VI) reagiert unter Einwirkung von Reduktionsmitteln zu Wolframblau („W2O5“). Dabei handelt es sich um ein Mischoxid, in dem Wolfram in den Oxidationsstufen +IV, +V und +VI vorliegt.
Aber wie wird überhaupt ein Metallfaden aus Wolfram hergestellt? Denn man kann das Metall kaum schmelzen und zu Fäden ziehen. Man erhält den Faden, indem man Metallpulver zunächst in die entsprechende Form presst und es anschließend durch Glühen sintert. Das macht das Ganze aber zu einer ziemlich bröseligen Angelegenheit, was wir merken, wenn wir einen Glühfaden aus einer geöffneten Glühlampe herausnehmen wollen.

Bild 3: Wolframglühspirale (Foto: Blume)
Warum überhaupt ist ein Glühdraht als Spirale geformt? Dadurch verlängert man den Draht. Das hat zur Folge,
dass die glühende Fläche und somit die Lichtausbeute vergrößert wird.
Leider wird das Abstrahlen von Licht von starker Hitzeentwicklung begleitet. Je heller das Licht ist, desto
heißer wird auch der Glühdraht. Man spricht hier von einem schwarzen Strahler. Das Licht, das der
abstrahlt, ist ein kontinuierliches Spektrum.

Bild 4: Kontinuierliches Spektrum einer Glühlampe
|
Versuch 2: Betrachten eines kontinuierlichen Spektrums mit einem Prisma
|
Mit steigender Hitze verschiebt sich das Spektrum vom Infrarot über Rot in Richtung auf Weiß und ins UV. Je mehr das Licht dem Sonnenlicht ähneln soll, desto weißer muss es sein und desto höher muss auch die Temperatur des Glühkörpers sein. So versucht man, sich immer mehr dem Sonnenlicht mit seiner Temperatur von über 5000 °C anzunähern.
Die Kryptonlampen
Leider hat bei dieser Hitze auch das Wolfram einen Nachteil: Es sublimiert. Das heißt, dass beim Betrieb der
Glühlampe ständig etwas Metall vom Glühfaden abdampft und sich auf der kühleren Glaswand der Glühlampe niederschlägt.
Dadurch wird die Lampe dunkler, das Licht gelber und der Faden dünner – bis er dann durchbrennt. Bekanntlich ist der
elektrische Widerstand eines Leiters direkt proportional zu seinem Querschnitt.
Der Sublimation kann man entgegenwirken, indem man ein Gas einfüllt, das die Sublimation der Wolframatome durch Stöße verhindert. Je schwerer die Atome des Gases sind, desto wirksamer sind sie. Außerdem darf das Gas nicht mit dem heißen Wolfram reagieren. Diese Eigenschaften waren die Stunde der schwereren Edelgase, hier die Stunde des Kryptons. Kryptonlampen sind auch heute noch der Renner unter den Glühlampen.

Bild 5: Kryptonlampe (Foto: Blume)
Da die Kryptonlampen auch einen gehörigen Anteil an UV abstrahlen, helfen die Pigmente, wie bei den Neonröhren
(siehe unten) die Lichtausbeute zu erhöhen. Die Pigmente sollen also nicht nur das Licht streuen, wie man oft meint.
Die Halogenlampen
Es gibt aber noch einen anderen Trick, die Wolframdrähte zu schonen: Man lässt sie sich einfach während des Betriebs
selbst reparieren. Dazu gibt man in die Glühlampe etwas Halogen, vor allem Iod. Das verdampft und bildet
ab 500 °C mit den herumfliegenden Wolframatomen Iodid.
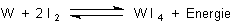
Wenn das so entstandene Wolfram-Iodid an die glühende, 1300 °C heiße Glühwendel stößt, zerfällt es wieder und gibt das Wolframatom ans Metall zurück.
Dieses Verfahren ist eigentlich aus der Metallurgie bekannt. Man stellt auf diese Weise hochreine, hochwertige Metalle her. Es handelt sich um das so genannte Aufwachsverfahren (Van Akel-de Boer-Verfahren). Bei diesem Verfahren werden Metalle durch thermische Zersetzung ihrer flüchtigen Halogenide hochgereinigt.
Damit schränkt man die Sublimation des Wolframs stark ein und verhindert die zunehmende Verdunkelung der Glaswand der Glühlampe. Deshalb erkannte man diese Halogenlampen an ihrem Licht, das gegenüber den bisherigen „gelben Funzeln“ besonders hell und weiß erschien.
Gasentladungslampen
Wer nun meint, dass damit nun das Ende der Entwicklung erreicht wäre, irrt. Denn es gibt noch andere
Möglichkeiten zur Lichterzeugung als das Glühen von Kohle oder Metall.
Man muss statt der Atome von Festkörpern Gasatome anregen, Elektronen abzugeben. Wie kann man ohne elektrische Leitung Energie auf Atome übertragen? Das kann man z. B. durch Stoß mit anderen, schnelleren Teilchen erreichen. Oder durch Einwirkung eines starken elektrischen Felds. Wenn die entstandenen Ionen die Elektronen wieder aufnehmen, senden sie die Ionisierungsenergie als Licht aus.
Da geladene Teilchen entladen werden, spricht man von Gasentladungslampen. Im Unterschied zu den oben erwähnten schwarzen Strahlern, also den klassischen Lampen mit glühenden Festkörpern, wird kein kontinuierliches Spektrum abgestrahlt, sondern ein diskontinuierliches Spektrum, ein Linienspektrum.
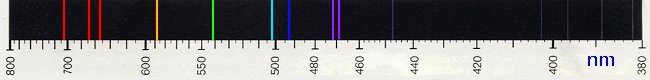
Bild 6: Linienspektrum eines Edelgases (Helium)
|
Versuch 3: Betrachten eines Linienspektrums
Gasentladungslampen gibt es in vielen Ausfertigungen: Man erkennt sie oft an ihrer typischen Lichtfarbe. Bekannt sind die Natriumdampflampen, die an Gefahrenpunkten wie Straßenkreuzungen zu sehen sind. Sie strahlen das intensiv gelbe Natriumlicht ab. Nun haben diese Lampen einen Nachteil. Das Linienspektrum sorgt nicht für gleichmäßige Energieverteilung. Die kann man erreichen, indem man die Gase unter hohem Druck einfüllt. Durch die Stöße der Atome und Moleküle kommt es zu Verbreiterungen der Spektrallinien und sogar zur Bildung breiter Banden. Man kann aber auch Gase mischen und so für die Abdeckung eines möglichst breiten Bereichs des Spektrums sorgen. Solche Beispiele beschreiben wir in den folgenden Abschnitten. |
Neonröhren
Als Lampenfüllung nimmt man besonders gern Edelgase, weil die leicht zum Leuchten angeregt werden können und
außerdem nicht mit dem Lampenmaterial chemisch reagieren. Bekannt sind die Neonröhren mit ihrem
weißen Licht. Nun muss man wissen, dass Neon eigentlich rotes Licht ausstrahlt. Aber durch kleine Tricks kann man
die Lichtfarbe beeinflussen. Man füllt etwas Quecksilber hinein. Beim Betrieb wird auch der Quecksilberdampf zum
Strahlen angeregt. Er sendet ein grünbläuliches Licht aus. Außerdem ist in der Strahlung auch ein nicht unbeträchtlicher,
nicht sichtbarer UV-Anteil vorhanden. Der reagiert mit speziellen Pigmenten, die man auf der Innenseite der Glühröhren
anbringt, zu weißem Licht.
Das alles macht die Neonröhren zu Sonderabfall. Denn auch die Pigmente enthalten oftmals Schwermetallverbindungen.
Früher fand man darin sogar Cadmium. Das hat man wie folgt nachweisen können:
|
Versuch 4: Analyse der Farbpigmente einer alten Neonröhre
|

Bild 7: Cadmiumsulfid (Foto: Daggi)
Energiesparlampen
Die sind nichts anderes als „aufgewickelte oder gefaltete“ Neonröhren. Nun gut, sie sollen länger halten, und es gibt dazu
noch einiges an elektronischem Schnick-Schnack, zum Beispiel das schnellere Zünden.
Aber mit diesen Lampen schafft man sich neue Umweltprobleme: Das der Quecksilberverseuchung. Denn wer glaubt ernstlich, dass die Leute diese Lampen nach Gebrauch brav zur Sondermüllentsorgung bringen? Darum haben sich dann die Filterspezialisten der Müllverbrennungsanlagen zu kümmern.
Xenonlampen
In letzter Zeit fallen nachts immer wieder grellweiß leuchtende Autolampen auf. Es handelt sich hierbei um Lampen, die mit
dem Edelgas Xenon und mit Spuren von Quecksilber und Halogenen bzw. Halogeniden gefüllt sind. Der Innendruck der Leuchtkörper
beträgt etwa 20 bar.
Zur Funktion: Zunächst wird zwischen zwei Wolframelektroden ein elektrischer Lichtbogen gezündet. In diesem werden die gasförmigen Inhaltsstoffe zum Leuchten angeregt.
Da die Ausbeute dieser Anregung umso größer ist, je schwerer die Atome des angeregten Gases sind, kann bei Verwendung von Xenon der Leuchtkörper sehr klein gebaut werden. Er ist tatsächlich nur so groß wie ein Streichholzkopf. Hinzu kommt aber auch eine bislang unerreicht hohe Temperatur: Sie beträgt nahezu 4000 °C.
Die emittierte Strahlung gleicht in der spektralen Zusammensetzung dem Tageslicht. Dagegen erscheint sogar das Licht der Halogenlampen gelblich.
Die exakte Bezeichnung der Autolampen ist Bi-Xenon-Lampen. Damit trägt man einem besonderen Konstruktionsmerkmal Rechnung: Um beim Dauerbetrieb zwischen Abblend- und Fernlicht schalten zu können, wird eine Blende zwischen Lichtquelle und Linse verschoben.
Ein Nachteil der Xenonlampen ist, dass die Zeitspanne zwischen Zünden und maximaler Helligkeit noch einige Sekunden beträgt, so dass man zum Betätigen der Lichthupe am Tage zusätzlich doch noch eine klassische Halogenlampe benötigt.
In der Zukunft nur LEDs?
Der neueste Trend sind Lampen auf der Basis von LEDs. Die Abkürzung steht für Light Emitting
Diodes. Man spricht auch von Leuchtdioden oder Lumineszenzdioden.
Bemerkenswert ist die Zusammensetzung des Diodenmaterials; hier findet man so exotische Metalle wie die dem Aluminium verwandten Elemente Indium oder Gallium, die mit Stickstoff, Phosphor oder Arsen verbunden sind. Kenner horchen auf, denn hier handelt es sich um typische Halbleiterdioden, die aus (III)- und aus (V)-Elementen (dazu noch dotiert mit (IV)-Elementen wie Silicium) zusammengesetzt sind. Erste sind so genannte „p-Leiter“, die anderen „n-Leiter“. Kommt es durch Anlegen einer Spannung in Durchlassrichtung zu einem n->p-Übergang, wird durch den Ladungsausgleich zwischen den negativen Elektronen und positiven „Löchern“ im Bereich des Übergangs spontan Lumineszenz erzeugt.
Je nach Diodenmaterial geben diese Leuchtkörper Licht mit verschiedenen Farben ab. Durch geschickte Kombination verschiedener LEDs erhält man nach den Prinzipien der additiven Farbmischung weißes Licht, das dem Tageslicht ähnelt. Dessen Intensität wird durch eine Vervielfachung der LED-Zahl gesteigert. Aufgrund der niedrigen Temperatur ist die Lichtausbeute hoch, und die Dioden halten deshalb auch wesentlich länger als die anderen Lampensysteme.
Auch Lebewesen können leuchten
Jeder kennt die Leuchtkäfer, die in den warmen Mai- und Juninächten herumschwärmen (Männchen) oder am Boden sitzen
(Weibchen). Aber auch das Meeresleuchten kennen viele: Am Strand liegender Tang verwandelt sich nachts, wenn man drauf tritt,
in eine leuchtende Spur. Hier sind Leuchtbakterien am Werk.
Zum Leuchten haben die Organismen einen ausgefeilten Enzymapparat entwickelt.
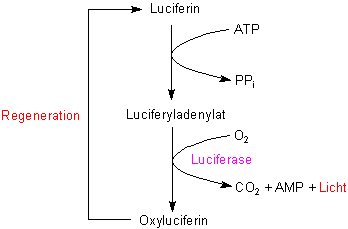
Luciferase-System
Die Energie wird als ATP ins System eingespeist. Der Reaktionsablauf ist so präzise, dass man damit auch geringste
ATP-Konzentrationen ermitteln kann. Man braucht bloß die Lichtblitze zu zählen.
Das Spannende ist außerdem, dass der Verlust durch Entwicklung von Wärme gering ist. Es wird also chemische Energie direkt in Lichtenergie
umgewandelt. Man spricht von Biolumineszenz. Das erinnert an den Luminolversuch,
der hier modellhaft hingehört. Im letzteren Fall spricht man von Chemolumineszenz.
Blitzlichtlampen
Historisch wird wohl der natürliche Blitz derjenige gewesen sein, der (wenn auch nur äußerst kurzfristig) für den Menschen die
Nacht zum Tage machte. Vom Blitzschlag stammte wohl auch das erste Feuer, das die Menschen nutzen konnten.
Ein Lichtblitz hat aber auch noch andere Vorteile, weshalb auch heute noch zur Erzeugung von kurzfristig leuchtenden, aber dafür umso intensiverem Licht technisch alles versucht worden ist – von der Chemikalienzündung bis zu elektronisch gesteuerten Blitzen. Zu diesem Thema haben wir eine besondere Webseite.
Ins Nachhinein
Was steuert die Entwicklung von Lichtquellen?
Erstens ist das die Suche nach immer stärkerem Licht.
Zweitens möchte man die Lichtausbeute erhöhen. Es geht um mehr Licht und weniger Wärmeentwicklung. Das heißt, es geht
um die Erhöhung des Wirkungsgrads. Wir wollen es zwar hell haben, aber es soll
verlustfrei und billig sein.
Da ist allerdings das Leben mit seiner Art und Weise der Lichtproduktion ungeschlagen: Erstens ist der Wirkungsgrad wegen geringer Wärmeabgabe sehr hoch, und außerdem wird das Lichtsystem ständig recycelt.
Rüdiger Blume
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 27. November 2011, Dagmar Wiechoczek