Prof. Blumes Tipp des Monats Mai 2015 (Tipp-Nr. 215)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Chemie mit dem Granatapfel

Bild 1: Granatapfel
(Foto: Blume)
Man sieht ihn an der Obsttheke im Laden, aber man traut sich nicht so richtig heran: Der Granatapfel
(Punica granatum) (lat. punicus, phönizisch; granum, Korn).
Denn viele Leute fragen sich, wie man den Apfel überhaupt zum Essen öffnet. Dabei geht es ganz einfach: Man muss die Frucht halbieren, durch Drücken etwas „weichknuddeln“, um das Innere zu lockern, und dann mit einem Kochlöffel oder einem anderen harten Gegenstand die vielen Samenkörner samt Saft durch kräftiges Klopfen herausschlagen - am Besten in eine große Schale.
Was soll man dann überhaupt essen? Man zerkaut und verzehrt die Samenkörner (ist gewöhnungsbedürftig!) und schleckt dazu den Saft auf. Die Samen schmecken herrlich frisch-sauer. Der Saft dagegen ist von einer erstaunlichen Süße und Klebrigkeit.
Der Granatapfel ist eine biochemische Stoffsammlung
Deshalb lädt er förmlich zum Experimentieren im Schullabor ein.
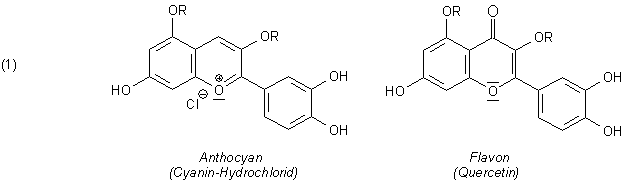
Er enthält zunächst einmal größere Mengen von farbigen Anthocyanen wie Cyanin und Flavonoiden wie Quercetin.
|
Versuch 1: Nachweis von Anthocyanen
|

Bild 2: pH-Reihe vom Granatapfelsaft
(Foto: Blume)
Weitere Inhaltsstoffe des Granatapfels sind Polyphenole wie Gallussäure und Ellagsäure.
Man spricht auch von Phenolsäuren.
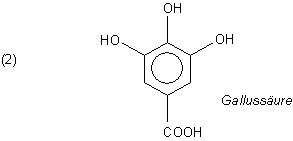
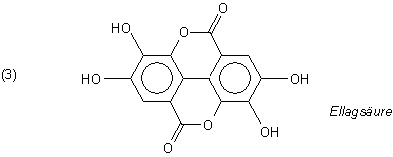
Ellagsäure ist eine dimere Gallussäure. Wegen ihres adstringierenden Geschmacks, der an den von Tanninen
erinnert, wird sie auch zu den Gerbstoffen gezählt. Ihre Polymere heißen Ellagitannin.
Zum Nachweis führen wir die Probe mit Eisen(III)-chlorid durch, die wir auch bei der Herstellung von Eisengallustinte kennengelernt haben.
|
Versuch 2: Nachweise von Tanninen im Granatapfel
|

Bild 3: Phenolnachweis im Granatapfelsaft
(Foto: Blume)
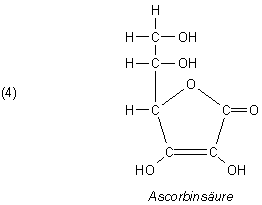
Der Granatapfel enthält natürlich auch Vitamin C (Ascorbinsäure). Der Nachweis gelingt
auf zweierlei Art und Weise.
|
Versuch 3: Nachweise von Vitamin C im Granatapfelsaft
Bild 4: Nachweis von Ascorbinsäure im Granatapfelsaft
|
Die Klebrigkeit und Süße des Granatapfelsafts beruhen auf großen Mengen an Glucose und Fructose. 100 g Granatapfel enthalten davon insgesamt etwa 15 %.
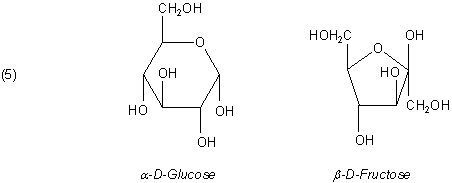
Beide Zucker sind Reduktionsmittel und zeigen deshalb eine positive Fehlingsche Reaktion - allerdings
erst beim Erhitzen. Das gilt auch für die schon erwähnten Polyphenole.
|
Versuch 4: Nachweis von weiteren reduzierenden Stoffen (Polyphenole und Zucker) im Granatapfelsaft
|
Es gibt jedoch auch spezifische Nachweisreaktionen für Glucose und Fructose.
|
Versuch 5: Nachweis von Glucose im Granatapfelsaft
|

Bild 5: Nachweis von Glucose im Granatapfelsaft
(Foto: Blume)
Ein bekannter Nachweis von Fructose erfordert leider einen Giftstoff, Selenige Säure.
|
Versuch 6: Nachweis von Fructose im Granatapfelsaft mit Seleniger Säure
|
Es gibt noch eine weitere Probe auf Fructose (Seliwanoff-Probe), bei der man die Lösung mit Salzsäure und Resorcin behandelt. Im Falle der Anwesenheit von Fructose erhält man eine intensiv rote Färbung. Dieser Nachweis ist zwar sehr schön, ist aber wegen der Eigenfarbe des Granatapfelsafts vor allem im Sauren (-> Versuch 1) nicht zu empfehlen.
Rüdiger Blume
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 15. April 2015, Dagmar Wiechoczek
