Prof. Blumes Tipp des Monats Dezember 2009 (Tipp-Nr. 150)
Beim Experimentieren den Allgemeinen Warnhinweis
unbedingt beachten.
Chemie der Zimtsterne
Was wäre Weihnachtszeit ohne leckeres Gebäck? Besonders beliebt sind die weiß glasierten Zimtsterne.

Bild 1: Schon ab September gibt es im Supermarkt Zimtsterne zu kaufen...
(Foto: Blume)
Heute kann man sie kaum noch mit reinem Gewissen essen, denn man hat zu viel über
Acrylamid und andere schädliche Substanzen
gelesen, die beim unsachgemäßen Backen entstehen. Die gesetzlich vorgeschriebenen Grenzwerte
werden von den Großbäckereien heute im Allgemeinen eingehalten.
Dem Vernehmen nach backen immer mehr umweltbewusste Familien ihre Zimtsterne selbst, um dem
Acrylamid zu entgehen. Ob sie dabei aber die Temperaturbedingungen genau einhalten können, bezweifle
ich angesichts vieler hartgebrannter Objekte, die ich bei diversen Einladungen verdrücken musste…
Es gibt aber noch andere Themen um die Zimtsterne. Was ist zum Beispiel Zimt, und was ist im Zimt enthalten? Was verursacht diesen typischen Geschmack? Kann man den Aromastoff auch künstlich herstellen? Wie ist es mit der Glasur?
Zimt
Zimt ist das Produkt des Zimtbaums (Cinnamomum), einem Verwandten des
Lorbeerbaums. Ein anderer, etwas altbackener Name für dieses Gewürz ist Kanehl oder Kaneel
(lat. canna, Röhre). Zur Gewinnung entrindet man frische Äste oder dünne Stämmchen, schabt das Innere der
Rindenstücke ab und trocknet die dünne äußere Schicht, die sich dabei papierartig zusammenrollt.
Wie ein geschälter Zimtbaum aussieht, zeigen wir hier.
Man lässt das Ganze noch etwas fermentieren, wobei aufgrund der Wirkung von Phenoloxidasen
wie bei Blättern im Herbst) die braune Farbe entsteht. Man schneidet die getrocknete Rinde in kleine Stück.
Diese Quills kann man beim Kaufmann als „Zimtstangen“ erstehen. Sie können aber auch noch
gemahlen werden.

Bild 2: Zimtzubereitungen (Foto: Blume)
Zimt enthält zu 1-4 % ätherische Öle. Man spricht von Zimtöl.
Die folgende Tabelle gibt Aufschluss über die ungefähre Zusammensetzung des Zimtöls.
| Zimtaldehyd
Eugenol Safrol Spuren von Linalool und Campher |
50-80 %
0-11 10-15 |
Es handelt sich bei diesen Inhaltsstoffen um Terpene. In der Lebensmittelchemie versteht man darunter eine Reihe von meist angenehm aromatisch riechenden Substanzen (griechisch terpein, erfreuen) mit einem Gerüst, das meistens aus etwa 10 C-Atomen besteht.
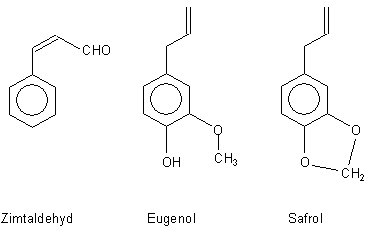
Bild 3: Wichtige Inhaltsstoffe des Zimtöls
Diese Substanzen machen in summa den typischen Zimtgeschmack aus. Dieser ist
genauso genommen kein Geschmack, sondern ein Geruch.
Eugenol ist bekannt als Inhaltsstoff der Gewürznelken. Dieses Terpen ist uns schon begegnet als Grundstoff zur technischen Vanillinsynthese. Safrol ist benannt nach dem nordamerikanische Sassafras-Baum („Fenchelbaum“), der ebenfalls ein Lorbeergewächs ist. Er enthält das früher für kosmetische Zwecke wichtige Sassafras-Öl, mit dem man aber auch Kautabak und Kaugummi aromatisierte. Diese Substanz ist auch in Lorbeer, Fenchel oder Muskatnuss enthalten und riecht fenchelartig.
In großen Mengen genossen sind die meisten Terpene eher ungesund; manche (wie das Safrol) stehen auch im Verdacht, cancerogen zu sein. Aber wer trinkt schon gerne die „Mutter aller Terpene“, Terpentin?
Was verbindet Zimtaldehyd, Eugenol und Safrol?
Das ist ihre Biosynthese; die geht von der Aminosäure Phenylalanin aus.
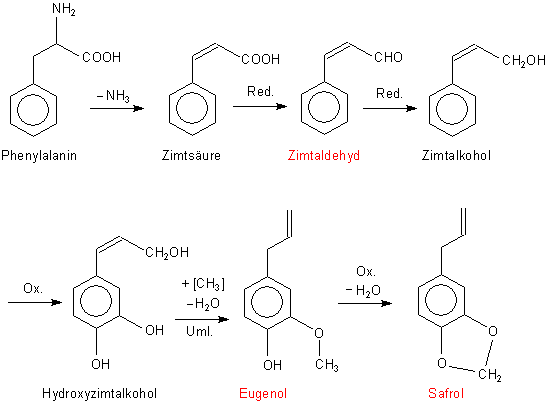
Bild 4: Biosynthese der Zimtöl-Inhaltsstoffe
Es stellt sich nun die Frage: Stellen die Pflanzen ihre Terpene nicht aus dem ungesättigten C5-Kohlenwasserstoff
Isopren her? Das ist auch hier so, denn letztlich wird das Kohlenstoffgerüst der aromatischen Aminosäure aus
Isoprenbausteinen zusammengesetzt. (Auf Isopren beruht unsere Kautschukproduktion.)
Alle Terpene kann man natürlich auch synthetisch herstellen. Man spricht dann von naturidentischen Produkten.
Welche biologische Rolle spielt die Zimtsäure?
| - | Wenn Zimtaldehyd oxidiert wird, entsteht Zimtsäure, ebenfalls ein Aromagrundstoff. In der Natur kommt eigentlich nur die cis-Form vor. (In vielen Büchern und Webseiten findet man stattdessen oft die Strukturformel der trans-Form gezeichnet.) |
| - | Zimtsäureethylester ist der sortenspezifische Aromastoff des Muskateller Weins. |
| - | Die Monohydroxyzimtsäure heißt auch Cumarinsäure. Sie geht wegen ihrer cis-Konfiguration spontan in ihr Lacton über, in das nicht nur im Waldmeister enthaltene Cumarin. |
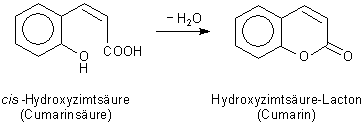
Bild 5: Biosynthese von Cumarin
| - | Einige Derivate der Dihydroxyzimtsäure sind unter dem Begriff Chlorogensäuren bekannt. |
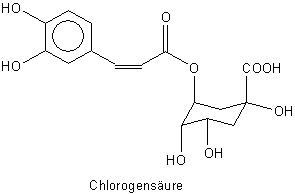
Bild 6: Eine typische Chlorogensäure
Sie spielen eine wichtige Rolle bei der Chemie des Kaffees. Chlorogensäuren binden
nicht die Base Coffein, sondern sind als Polyphenole zugleich wichtige Antioxidantien.
Zur Chemie der Glasur der Zimtsterne
Wie der Name schon sagt, handelt es sich bei der Glasur nicht um kristallinen Zucker, sondern um
Zuckerglas.
|
Versuch 1: Wie man die Glasur macht
|
Titandioxid färbt nicht nur Wände weiß, sondern auch Glasuren
Titandioxid ist als Edelstein Rutil wegen seines hohen Brechungsindex geschätzt. Deshalb wirkt auch das
feingemahlene Pulver so leuchtend weiß. Das macht man sich zum Färben der Glasur von Zimtsternen zunutze.
Zum Nachweis von Verbindungen des Titans gibt es ein Experiment. Dass dieser Nachweis auch mit der weißen Glasur von gekauften Zimtsternen gelingt, hat uns der Lehrer P. W. mitgeteilt.
|
Versuch 2: Nachweis von Titan in der weißen Glasur
|
Titandioxid ist übrigens ein völlig ungiftiger Stoff. Deshalb ist er als Lebensmittelzusatzstoff unter der E-Nummer 171 zugelassen. Das heißt aber nicht etwa, dass man Wandfarbe aus dem Baumarkt („Binderfarbe“) in die Glasurmischung einrühren darf!
Rüdiger Blume
Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Blumes Bildungsserver für Chemie.
Letzte Überarbeitung: 11. Januar 2015, Dagmar Wiechoczek