
Fette und fette Öle
I. Gewinnung und Eigenschaften von Fetten und fetten Ölen
II. Der chemische Aufbau von Fetten und fetten Ölen
III. Gesättigte und ungesättigte Fettsäuren
IV. Emulsionen
V. Verderben von Fetten
VI. Weitere Verwendung von Fetten
I. Gewinnung und Eigenschaften von Fetten und fetten Ölen
Fette sind bei Raumtemperatur feste oder halbfeste Stoffe (z. B. Palmin®
und Schweineschmalz). Liegen sie bei Raumtemperatur in flüssiger Form vor, so nennt
man sie fette Öle (z. B. Olivenöl). Fette und fette Öle können
sowohl pflanzlicher als auch tierischer Herkunft sein und werden durch Pressen, verschiedene
Extraktionsverfahren oder durch "Auskochen" gewonnen.
Versuche:
Gewinnen von Öl durch Kaltpressen
Gewinnen von Pflanzenöl durch Kalt-Extraktion
Gewinnen von Pflanzenöl durch Heiß-Extraktion
Fette und fette Öle werden auch als Lipide bezeichnet. Ihre Schmelztemperaturen liegen in der Regel zwischen - 20 °C und + 40 °C (s. Tab. 1). Die Dichte der meisten Lipide beträgt ca. 0,9 g/cm3. Sie ist geringer als die Dichte von Wasser, weshalb Fette auf der Wasseroberfläche schwimmen. Aus alltäglichen Erfahrungen mit Fetten wissen wir, dass diese nicht in Wasser löslich sind (z. B. Fettaugen auf Suppen). Dagegen lösen sich die Lipide gut in so genannten lipophilen (fettfreundlichen) Lösungsmitteln (z. B. Reinigungsbenzin).
Versuche:
Untersuchung der Löslichkeit von Speiseöl
Löslichkeit von lipophilen Stoffen in Fetten
Aufgrund der hohen Siedepunkte von Lipiden hinterlassen sie bleibende, durchscheinende Flecken auf Papier. Diese so genannte Fettfleckprobe dient als einfache Erkennungsmethode für Lipide, die jedoch nicht spezifisch ist, da auch Mineralöle solche Fettflecken auf Papier hinterlassen.
Versuche:
Die Fettfleckprobe als Nachweis von Fetten
Unterscheidung von fettem Öl und Mineralöl
Lipide sind gut brennbar. Wenn sie verbrannt werden, wird viel Energie frei, so dass man von einem hohen Heizwert der Fette spricht. Damit ein Fettbrand ausgelöst wird, muss dem Fett zunächst eine bestimmte Menge Energie in Form von Wärme (Aktivierungsenergie) zugeführt werden, da nur die Fettdämpfe und deren Zersetzungsprodukte sich entzünden lassen. Die Entzündlichkeit von Fetten entspricht damit dem allgemeinen Verhalten von brennbaren Stoffen.
Versuche:
Friteusenbrand (Modellversuch)
Bau einer Öl- und Petroleumlampe
II. Der chemische Aufbau von Fetten und fetten Ölen
Fettmoleküle sind Ester (Bild 1) aus
Glycerin mit jeweils drei Fettsäuren
(Carbonsäuren)
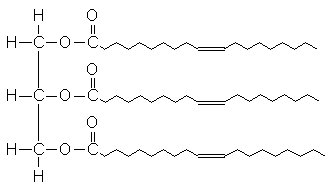
Bild 1: Typisches Triglycerid des Sonnenblumenöls
Diese so genannten Triglyceride können hydrolysiert
(verseift) werden und reagieren so zu Glycerin und den Salzen der Fettsäuren, den
Seifen.
Folgende Versuche geben einen Einblick in das Reaktionsverhalten von Lipiden, deren chemischen
Aufbau und Nachweis:
Versuche:
Untersuchung von Fett auf die Elemente Kohlenstoff und Wasserstoff
Thermische Zersetzung von Fetten
Unterscheidung von fettem Öl und Mineralöl
Nachweis von Glycerin nach der Verseifung eines Fettes
Nachweis von Buttersäure in Butter
In Fetten sind pro Molekül unterschiedliche Fettsäuren gebunden, so dass eine große Anzahl unterschiedliche Fettmoleküle existieren. Zudem sind natürliche Fette Gemische dieser unterschiedlichen Fettmoleküle, weshalb keine genaue chemische Formel für ein bestimmtes Fett (z. B. Olivenöl) angegeben werden kann. Aus diesem Grund gibt man für die einzelnen Fette den prozentualen Anteil der vorkommenden Fettsäuren an der Gesamtmasse des Fettes an:
|
|
|
|
|
|
|
|
|
|
| gesättigte | ||||||||
| Buttersäure (C3H7COOH) |
|
|
|
|
|
|
|
|
| Laurinsäure (C11H23COOH) |
|
|
|
|
|
|
|
|
| Palimitinsäure (C15H31COOH) |
|
|
|
|
|
|
|
|
| Stearinsäure (C17H35COOH) |
|
|
|
|
|
|
|
|
| andere Fettsäuren |
|
|
|
|
|
|
|
|
| ungesättigte | ||||||||
| Ölsäure (C17H33COOH) |
|
|
|
|
|
|
|
|
| Linolsäure (C17H31COOH) |
|
|
|
|
|
|
|
|
| Linolensäure (C17H29COOH) |
|
|
|
|
|
|
|
|
| andere Fettsäuren |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
III. Gesättigte und ungesättigte Fettsäuren
In Fetten und fetten Ölen sind zwei unterschiedliche Arten von Fettsäuren
gebunden. Die gesättigten Fettsäuren besitzen in der Kohlenwasserstoffkette
nur Einfachbindungen, während die ungesättigten Fettsäuren mindestes
eine Doppelbindung in der Kohlenwasserstoffkette enthalten. Weisen Fettsäuren mehrere
Doppelbindungen auf, spricht man von mehrfach ungesättigten Fettsäuren.
Versuche:
Nachweis von C-C-Doppelbindungen in Fetten mit Bromwasser
Nachweis von C-C-Doppelbindungen in Fetten mit Baeyer-Reagenz
Lipide mit hohen Anteilen ungesättigter Fettsäuren haben einen geringen Schmelzbereich. Sie kommen verstärkt in pflanzlichen Rohstoffen vor, weshalb man auch mehr fette Öle aus pflanzlichen Rohstoffen gewinnt (Tabelle 1). Um dem Konsumentenbedürfnis nach pflanzlichen, streichfähigen Fetten nachzukommen, werden fette Öle durch die Fetthärtung zu festen Fetten verarbeitet.
Versuch:
Härtung von fetten Ölen (Modellversuch)
IV. Emulsionen
Fette Öle sind mit Wasser nur für kurze Zeit mischbar. Es entsteht eine
Emulsion, die sich nach kurzer Zeit, aufgrund der unterschiedlichen Dichte beider
Flüssigkeiten, wieder trennt. Durch Emulgatoren, die lipophile
("fettfreundliche") und hydrophile ("wasserfreundliche")
Molekülbestandteile besitzen, können Emulsionen stabilisiert werden.
Hierzu ordnen sich die Emulgatoren an der Phasengrenze zwischen Öl und Wasser an.
Je nach Mengenverhältnis zwischen Öl und Wasser bilden sich "Öl in
Wasser"-Emulsionen (O/W-Emulsionen) oder "Wasser in Öl"-Emulsionen
(W/O-Emulsionen). Viele Lebensmittel, wie z. B. Milch, Mayonnaise, Butter und Margarine,
aber auch eine Reihe von Kosmetika sind stabile Emulsionen. Eine typische O/W-Emulsion
ist die Milch. Butter und
Margarine sind dagegen W/O-Emulsionen.
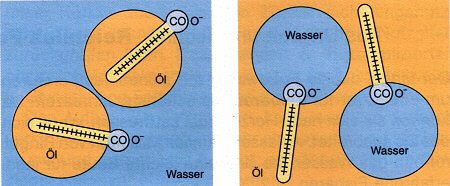
Bild 2: Anordnung von Emulgatoren in O/W- und W/O-Emulsionen
(Quelle: Cornelsen)
Versuche:
Herstellen von Margarine (Modellversuch)
Herstellen von Mayonnaise
Zerstören von W/O-Emulsionen durch Erhitzen
Emulsionen spielen auch bei der durch Enzyme katalysierten Spaltung von Fetten im menschlichen Körper (Fettverdauung) eine wichtige Rolle.
Versuch:
Verdauung von Fetten
V. Verderben von Fetten
Ein großer Teil der Lipide wird in Lebensmitteln verarbeitet. Je nach
Verwendung können die Fette langsam oder schnell verderben. So altert häufig
erhitztes Fett (z. B. Frittierfett) relativ schnell, aber auch Butter wird nach einiger
Zeit ranzig. Inzwischen gibt es Verfahren, um z. B. Frittierfett zu recyclen.
Versuche:
Nachweis von freien Fettsäuren im Altfett
Nachweis von Peroxiden im Altfett
VI. Weitere Verwendung von Fetten
In Kosmetika (Cremes und Lotionen) werden Fette als Emulsionen verwendet. Des Weiteren dienen sie
als Rohstoffe für die Herstellung von Seifen verwendet.
Fette verwendet man aber auch als Rohstoffe für die Herstellung von anderen Produkten, wie z. B. Ölfarben und Linoleum. Rizinusöl kann aufgrund vorhandener OH-Gruppen durch Polykondensation zu Polyester-Kunststoffen verarbeitet werden.
Versuche:
Trocknende Öle
Herstellen eines Polyesters aus Citronensäure und Rizinusöl
Weitere Texte zum Thema „Chemie im und ums Haus“